Clear Sky Science · pl
Defekty strukturalne we włóknach amyloidu-β napędzają nukleację wtórną
Dlaczego drobne wady białek mózgu mają znaczenie
W chorobie Alzheimera i pokrewnych schorzeniach mózgu niektóre białka zlepiają się w długie, nitkowate struktury nazywane włóknami amyloidowymi. Włókna te nie tylko są znakiem choroby; pomagają też powstawać nowym, wysoce toksycznym cząstkom białkowym, które mogą uszkadzać komórki mózgowe. W badaniu zadano proste, lecz istotne pytanie: czy rzadkie strukturalne „wady” wewnątrz włókien amyloidowych działają jako główne ogniska zapalające tworzenie nowych szkodliwych struktur? Odpowiedź może wskazać nowe sposoby spowolnienia lub zatrzymania tych zaburzeń poprzez celowanie w zaledwie kilka krytycznych miejsc zamiast całej powierzchni białka. 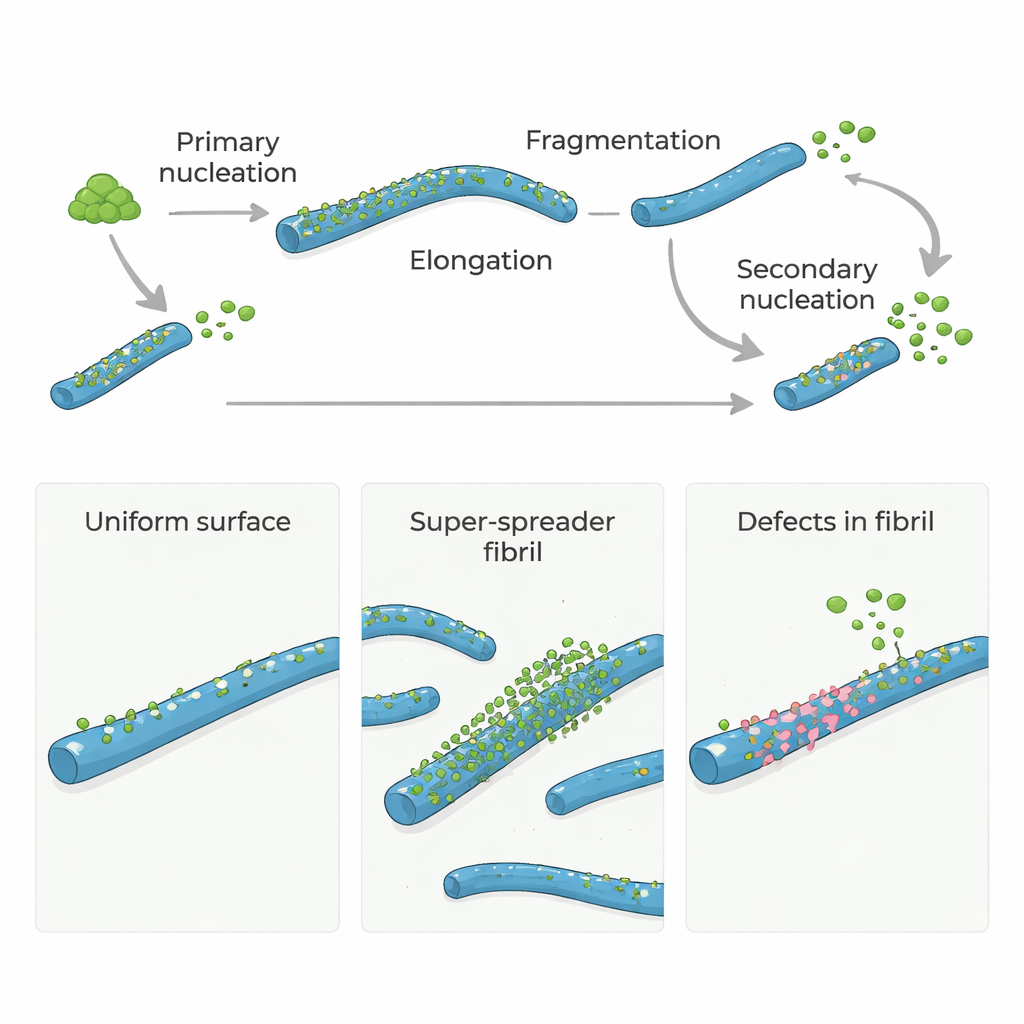
Od spokojnego białka do reakcji łańcuchowej
Białka amyloidu-β (Aβ), kluczowe w chorobie Alzheimera, zwykle nie tworzą szybko skupisk samoczynnie. Aby rozpocząć proces, kilka monomerów musi powoli złożyć się w pierwsze, drobne włókna — etap zwany nukleacją pierwotną. Gdy te początkowe włókna już istnieją, szybko rosną przez przyłączanie kolejnych monomerów na końcach. Jeszcze ważniejsze jest to, że istniejące włókna mogą wywoływać pojawienie się nowych włókien na swoich powierzchniach w procesie znanym jako nukleacja wtórna. Ten powierzchniowy krok może zalewać system nowymi włóknami i małymi, toksycznymi oligomerami, przekształcając powolny dopływ w gwałtowną reakcję łańcuchową.
Czy wszystkie powierzchnie włókien są równie niebezpieczne?
Wiele modeli zakładało, że cała powierzchnia włókna amyloidowego równie dobrze katalizuje nukleację wtórną. Jednak niedawne eksperymenty zasugerowały, że aktywna jest tylko niewielka część powierzchni. Aby to zbadać, autorzy użyli naturalnego molekularnego „chaperonu” o nazwie Brichos, znanego z hamowania nukleacji wtórnej Aβ40 i Aβ42 (dwóch kluczowych form amyloidu-β). Poprzez precyzyjne mierzenie, ile fluorescencyjnie znakowanego Brichosa wiąże się z włóknami, stwierdzili, że wiązanie jest silne, lecz liczbowo bardzo rzadkie: około jednego cząsteczki Brichos na każde 100–150 cząsteczek Aβ we włóknie. Mimo to taka skąpa pokrywa wystarczyła, by stłumić ponad 90% nukleacji wtórnej, co oznacza, że dominującą rolę w produkcji nowych toksycznych zespołów odgrywają rzadkie, lokalne miejsca, a nie cała powierzchnia.
Badanie roli ukrytych defektów
Te wyniki sugerowały, że kluczowe miejsca nukleacji mogą być defektami strukturalnymi — drobnymi nieregularnościami powstającymi w miarę wzrostu włókien, takimi jak źle dopasowane warstwy czy częściowo odsłonięte jądra wewnętrzne. Aby przetestować ten pomysł bezpośrednio, badacze hodowali włókna Aβ40 w dwóch różnych warunkach. Jeden zestaw, „kontrolny”, powstał w typowych, silnie przesyconych warunkach sprzyjających szybkiemu wzrostowi i utrwalaniu defektów kinetycznych. Drugi zestaw wytworzono przy użyciu powolnego, kontrolowanego temperaturowo procesu wyżarzania: włókna rosły przy bardzo niskiej efektywnej sile napędowej, blisko granicy rozpuszczalności, gdzie nieprawidłowe struktury mogą się rozpuścić lub naprawić zanim zostaną trwałe. Mikroskopia krioelektronowa o wysokiej rozdzielczości wykazała, że oba zestawy włókien były pod względem kształtu i skrętu zasadniczo identyczne, co wskazuje, że proces wyżarzania nie zmienił podstawowej morfologii. 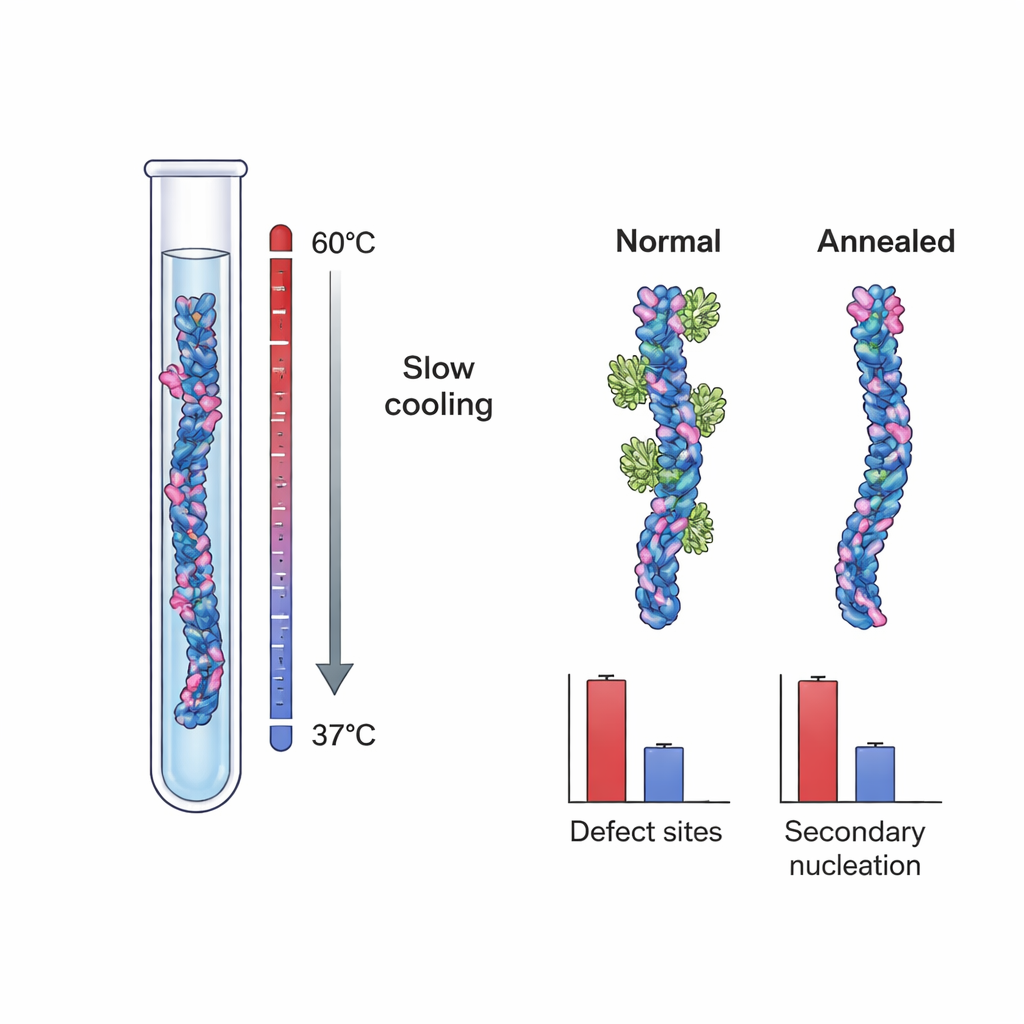
Mniej wad, mniej niebezpiecznych miejsc wzrostu
Gdy zespół zmierzył wiązanie Brichosa do tych dwóch typów włókien, odkrył uderzającą różnicę. Włókna kontrolne Aβ40 miały około jednego miejsca wiązania Brichosa na ~100 monomerów, co ponownie wskazywało na rzadkie, ale istotne miejsca. Włókna wyżarzone miały jednak tylko około jednego miejsca na ~800 monomerów — niemal 90% redukcję częstości miejsc. W oddzielnych testach, gdy te włókna dodawano jako „nasiona” do świeżych roztworów Aβ40, włókna wyżarzone były znacznie mniej skuteczne w wywoływaniu nowej agregacji, nawet gdy ich całkowita masa była dopasowana do masy włókien kontrolnych. Szczegółowe modelowanie kinetyczne wykazało, że spadek mocy nasienienia nie da się prosto wyjaśnić różnicami w długości włókien. Zamiast tego ilościowo pokrywał się on ze zmniejszoną liczbą miejsc wiążących Brichos, co mocno wspiera tezę, że defekty wzrostu działają jako główne silniki nukleacji wtórnej.
Ogólna zasada o obiecaniach terapeutycznych
Łącząc argumenty termodynamiczne, ponowną analizę wcześniejszych prac i porównania między kilkoma białkami tworzącymi amyloid, autorzy twierdzą, że rzadkie defekty wzrostu prawdopodobnie odgrywają kluczową rolę w nukleacji wtórnej w wielu układach, nie tylko w związanych z Aβ w chorobie Alzheimera. Defekty te częściowo odsłaniają ściśle upakowane wewnętrzne jądro włókna, oferując gotowy szkielet, na którym nowe oligomery i włókna mogą tworzyć się znacznie łatwiej niż na gładkiej powierzchni. Uznanie tych defektów za głównych sprawców otwiera nowe drogi projektowania leków. Zamiast próbować blokować wszystkie możliwe interakcje na powierzchni włókna, terapie mogłyby dążyć do osłaniania lub naprawy tylko tych rzadkich miejsc defektowych albo do ograniczania warunków, które je tworzą. W praktyce może to oznaczać obniżenie efektywnego stężenia białek tworzących amyloid w mózgu lub projektowanie cząsteczek, inspirowanych przez Brichos, które rozpoznają i neutralizują gorące punkty nukleacji napędzane defektami. Jeśli się to powiedzie, takie strategie mogłyby odciąć główne źródło toksycznych oligomerów i spowolnić postęp chorób związanych z amyloidem.
Cytowanie: Hu, J., Scheidt, T., Thacker, D. et al. Structural defects in amyloid-β fibrils drive secondary nucleation. Nat Commun 17, 1933 (2026). https://doi.org/10.1038/s41467-026-69377-1
Słowa kluczowe: włókna amyloidowe, choroba Alzheimera, nukleacja wtórna, agregacja białek, chaperon Brichos