Clear Sky Science · pl
Konkurujące porządki wiązań wodorowych napędzają anomalną napięcie powierzchniowe wody
Dlaczego powierzchnia wody jest bardziej dziwna, niż się wydaje
Powierzchnia wody pozwala owadom chodzić po stawach, nadaje kształt kroplom deszczu i kontroluje, jak tworzą się i pękają pęcherzyki. Jednak gdy naukowcy mierzą, jak „ciasna” jest ta powierzchnia — czyli napięcie powierzchniowe — okazuje się, że w miarę ochładzania się woda zachowuje się zaskakująco dziwnie, zwłaszcza gdy jest schłodzona poniżej normalnego punktu zamarzania. Ten artykuł wykorzystuje zaawansowane symulacje komputerowe, aby ujawnić, w jaki sposób ukryta organizacja cząsteczek wody na powierzchni tłumaczy tę długoletnią zagadkę.
Dwa ukryte typy ciekłej wody
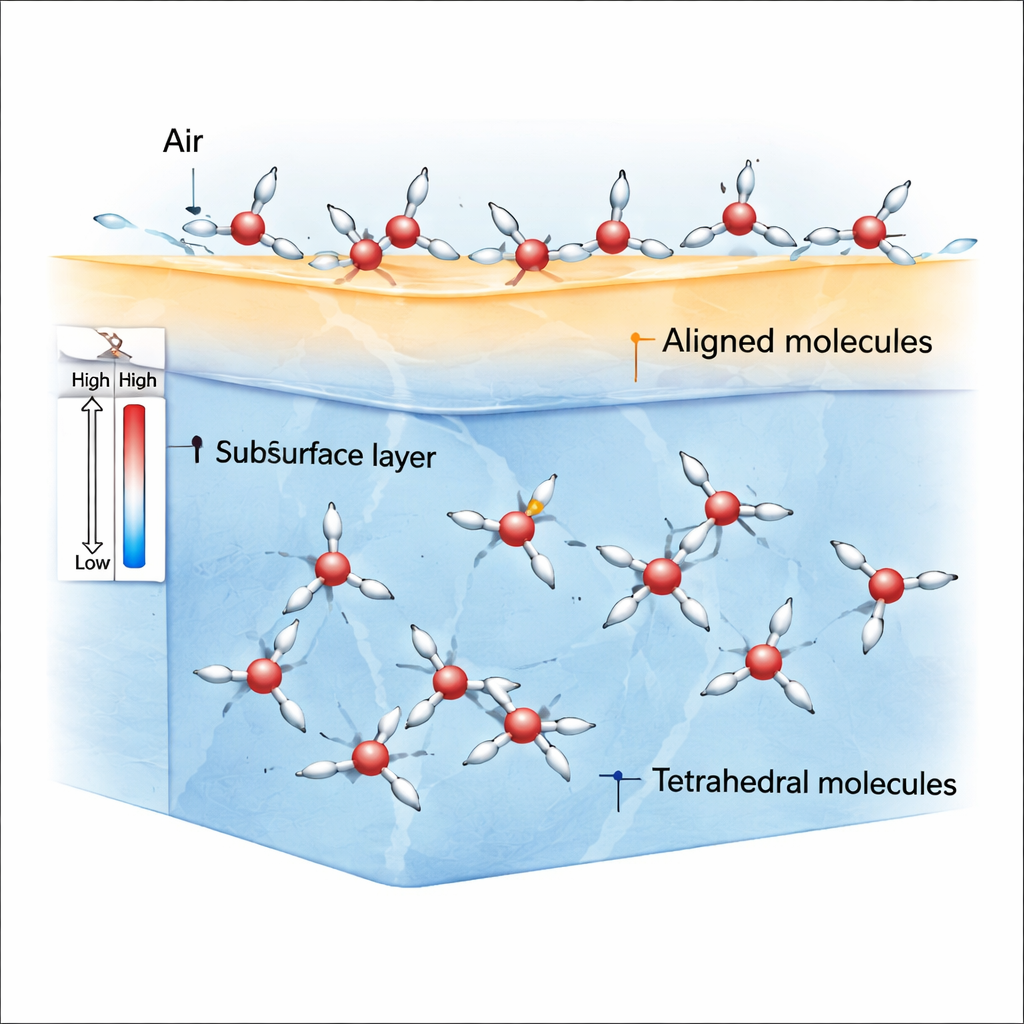
Chociaż doświadczamy wody jako prostej, jednorodnej cieczy, jej cząsteczki mogą lokalnie układać się na dwa kontrastujące sposoby. Jedne ułożenie jest gęstsze i bardziej nieuporządkowane; autorzy nazywają je stanem ρ. Drugie jest bardziej otwarte i symetryczne, z każdą cząsteczką otoczoną w przybliżeniu czterokierunkowym, tetraedrycznym wzorem; nazywa się to stanem S. Wcześniejsze prace sugerowały, że równowaga między tymi dwoma lokalnymi wzorcami pomaga wyjaśnić wiele dziwnych właściwości objętościowych wody. Tutaj autorzy pytają, jak ten sam dwustanowy obrazek przejawia się na granicy powietrze–woda, gdzie rodzi się napięcie powierzchniowe.
Jak powierzchnia ustawia cząsteczki w szeregu
Na styku powietrza i wody cząsteczki nie odczuwają już równych pociągów we wszystkich kierunkach. Ta złamana symetria faworyzuje cząsteczki w stanie ρ, których atomy wodoru i dipole molekularne łatwo mogą odchylić się w preferowanym kierunku. Symulacje pokazują, że w pobliżu temperatury pokojowej i nieco poniżej bardzo wierzchnia warstwa wody staje się wypełniona tymi uporządkowanymi cząsteczkami ρ, podczas gdy cząsteczki w stanie S są częstsze tuż pod powierzchnią i w objętości. Ponieważ cząsteczki ρ silnie się ustawiają, tworzą one nierównowagę sił — anizotropię naprężeń — która generuje stosunkowo wysokie napięcie powierzchniowe w porównaniu z zwykłymi cieczami, takimi jak benzen.
Dlaczego ochładzanie najpierw spowalnia, potem przyspiesza usztywnianie powierzchni
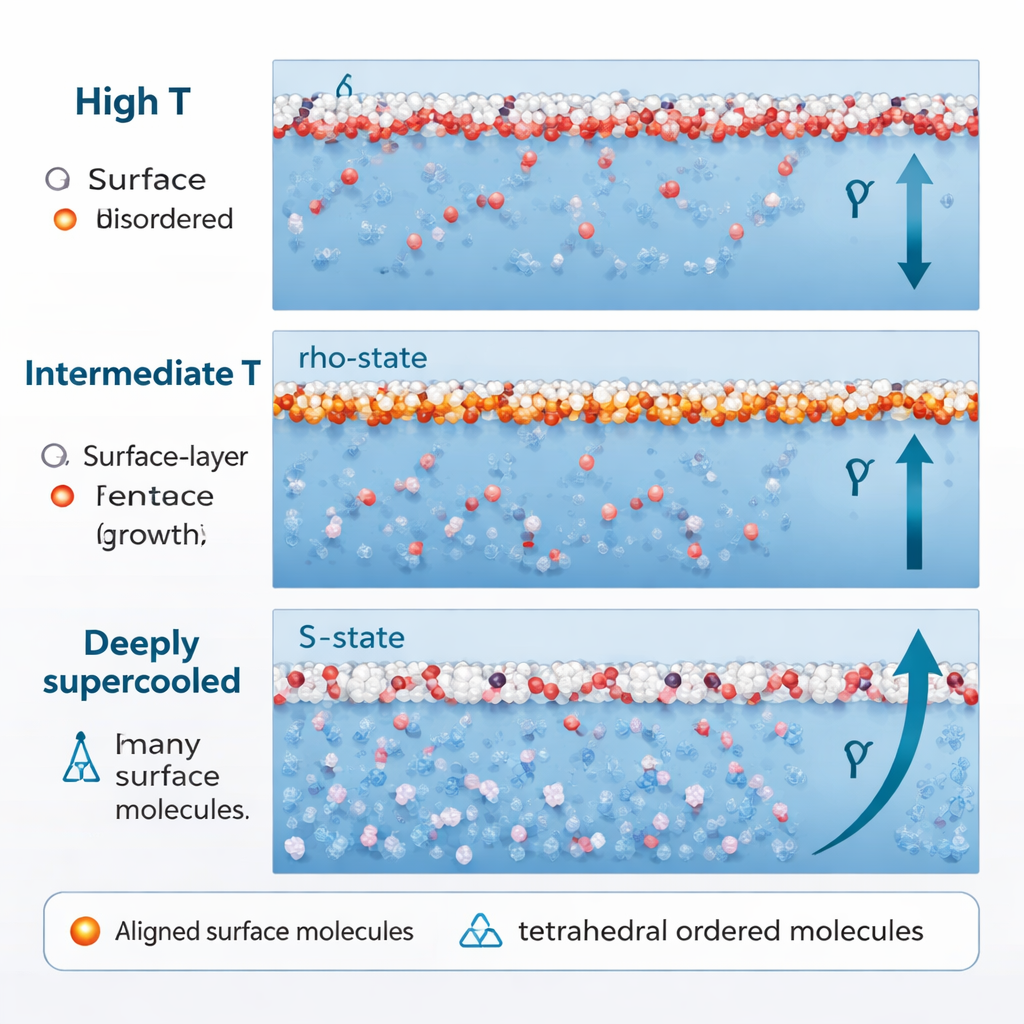
W większości prostych cieczy ochładzanie stopniowo usztywnia powierzchnię, powodując niemal liniowy wzrost napięcia powierzchniowego. Woda robi to tylko w wyższych temperaturach. Gdy ochładza się w kierunku około –0,15 °C (275 K), wzrost napięcia powierzchniowego zaczyna zwalniać. Symulacje pokazują, że to spowolnienie dzieje się dlatego, że cząsteczki ρ na powierzchni osiągnęły już maksymalne ustawienie; dalsze ochładzanie ledwie zmienia ich wkład. Jednocześnie cząsteczki S w podsufitowej warstwie pozostają w większości losowo zorientowane, więc niewiele przyczyniają się do zwiększenia naprężenia powierzchniowego. Efektem netto jest rodzaj plateau: temperatura nadal spada, ale napięcie powierzchniowe rośnie tylko nieznacznie.
Głębokie przechłodzenie wywołuje drugie usztywnienie
Gdy woda jest schładzana znacznie dalej, daleko poniżej normalnego punktu zamarzania, w głęboko przechłodzonym reżimie (około 250 K i niżej), jej zachowanie znowu się zmienia. Udział struktur typu S, tetraedrycznych, gwałtownie rośnie, nawet w pobliżu powierzchni. Co kluczowe, te cząsteczki S przestają już wskazywać w losowych kierunkach. Ich dipole zaczynają ustawiać się wzdłuż kierunku prostopadłego do powierzchni, napędzane interakcjami między sąsiednimi dipolami molekularnymi oraz obszarem ujemnego ciśnienia tuż pod powierzchnią. Gdy to nastąpi, woda w stanie S, która wcześniej zmiękczała napięcie powierzchniowe, zaczyna je wzmacniać. Ten dodatkowy, uporządkowany wkład powoduje odnowiony, szybszy wzrost — „reentrancyjny” wzrost — napięcia powierzchniowego przy niskich temperaturach.
Od zagadek powierzchni po lód i dalej
Te same tetraedryczne skupiska w stanie S, które usztywniają powierzchnię w niskich temperaturach, przypominają także wczesne cegiełki pewnych form lodu, a symulacje znajdują ich wzbogacenie w pobliżu interfejsu. Oznacza to, że granica powietrze–woda może działać jak kolebka formowania lodu, co pomaga wyjaśnić, dlaczego zamarzanie często zaczyna się na powierzchniach. Szerzej, praca dostarcza konkretnego, molekularnego związku między tym, jak cząsteczki wody się układają i orientują, a tym, jak silnie powierzchnia ściąga do wnętrza. Ten strukturalno-mechaniczny obraz nie tylko rozwiązuje zagadną krzywą temperatury napięcia powierzchniowego wody, ale też oferuje mapę drogową do zrozumienia i kontrolowania zjawisk międzyfazowych w innych cieczach tworzących sieć, od przechłodzonej wody w chmurach po materiały stosowane w technologii i biologii.
Cytowanie: Yuan, J., Qiu, K., Sun, G. et al. Competing hydrogen-bond orders drive water’s anomalous surface tension. Nat Commun 17, 1498 (2026). https://doi.org/10.1038/s41467-026-69356-6
Słowa kluczowe: napięcie powierzchniowe wody, wiązania wodorowe, przesycone superchłodzenie wody, struktura cieczy, nukleacja lodu