Clear Sky Science · pl
STING współdziała z TOX, hamując ekspresję HO-1, by wywołać ferroptozę w naciekających nowotwór limfocytach CD8+ i powodować oporność na immunoterapię
Dlaczego te badania są istotne dla leczenia raka
Nowoczesne immunoterapie przeciwnowotworowe działają przez uwolnienie własnych „zabójczych” limfocytów T organizmu, jednak wiele guzów nadal potrafi je unieszkodliwiać. Badanie odkrywa ukryty mechanizm autodestrukcji wewnątrz limfocytów CD8+, którego wykorzystania dokonują guzy, i pokazuje, że wyłączenie tego mechanizmu może znacznie zwiększyć skuteczność immunoterapii.
Ukryta ścieżka śmierci w limfocytach walczących z guzem
W obrębie guza limfocyty CD8+ powinny polować na komórki nowotworowe i je niszczyć. W praktyce bywają jednak nieliczne, o obniżonej aktywności i krótkotrwałe. Autorzy skupili się na dwóch cząsteczkach w limfocytach — STING, detektorze uszkodzeń DNA, i TOX, białku powiązanym z wyczerpaniem T-komórek. Zmodyfikowali myszy, których limfocyty CD8+ nie miały STING, TOX lub obu tych czynników, a następnie wszczepili różne typy guzów. Ku zaskoczeniu, myszy z limfocytami pozbawionymi STING lub TOX znacznie lepiej zwalczały guzy. Guzy rosły wolniej, zawierały znacznie więcej limfocytów CD8+, a te produkowały większe ilości cytotoksycznych molekuł, takich jak interferon‑gamma i granzyme B. Wskazywało to na wewnętrzny program, który po cichu sabotuje limfocyty w obrębie guza.
Jak żelazem napędzana śmierć komórki osłabia odporność
Analizując aktywność genów w naciekających guza limfocytach, naukowcy odkryli, że normalne limfocyty w guzie są przygotowane do specyficznej formy śmierci zwanej ferroptozą. W przeciwieństwie do apoptozy, ferroptoza jest wywoływana przez nadmiar żelaza i gromadzenie uszkodzonych lipidów w błonach komórkowych. W zwykłych limfocytach CD8+ eksponowanych na komórki nowotworowe włączono geny promujące akumulację żelaza i uszkodzenia lipidów, a wyciszono geny ochronne. Natomiast limfocyty pozbawione STING lub TOX wykazywały odwrotny wzorzec: wyższe ekspresje enzymów ochronnych HO-1 i GPX4, niższe poziomy żelaza, mniejsze peroksydowanie lipidów, zdrowsze mitochondria i oporność na ferroptozę. Testy laboratoryjne potwierdziły, że chemiczne blokowanie ferroptozy utrzymywało przy życiu normalne limfocyty, podczas gdy usunięcie STING lub TOX uczyniło je naturalnie odpornymi.
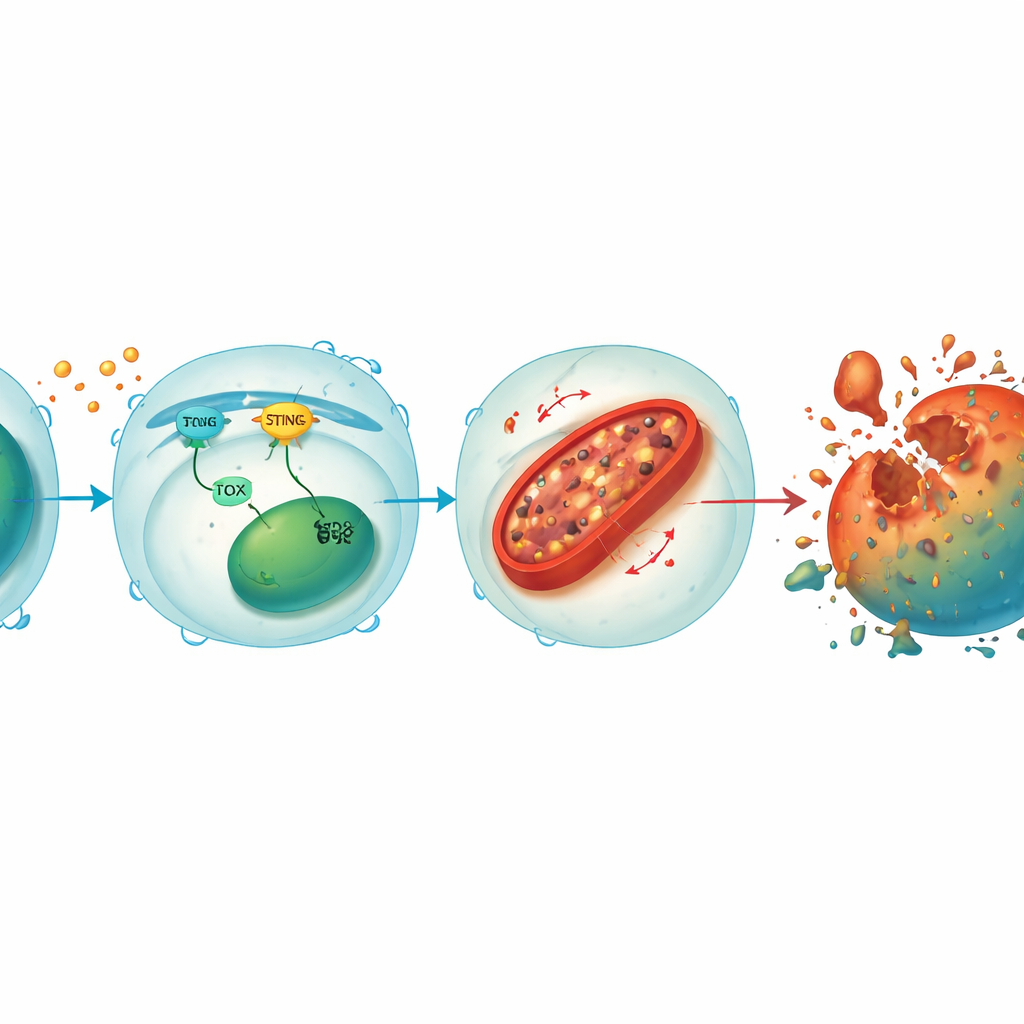
Obieg łączący sygnały stresu z uszkodzeniem mitochondriów
Głębiej wnikając w mechanizmy, zespół odkrył, że STING i TOX tworzą wzmacniającą się pętlę wewnątrz limfocytów CD8+. Gdy sygnały związane z guzem lub wirusem aktywują STING, uruchamia on czynniki zwiększające TOX, a TOX z kolei pomaga podtrzymać aktywność STING. Razem tłumią HO-1, enzym, który zwykle pomaga kontrolować żelazo komórkowe. Przy zahamowanym HO-1 żelazo gromadzi się w mitochondriach — „elektrowniach” komórki — prowadząc do zwiększenia reaktywnych form tlenu i utleniania lipidów błonowych. To uszkodzenie mitochondriów wyczerpuje produkcję energii i ostatecznie skłania limfocyt do ferroptozy. Przywrócenie STING lub TOX w komórkach knockout odwrotnie powodowało ponowną akumulację żelaza i śmierć komórek, podczas gdy dalsze obniżenie HO-1 uczyniło nawet chronione limfocyty podatnymi, podkreślając rolę HO-1 jako centralnej „hamulcowej” tej destrukcyjnej ścieżki.
Jak mleczan produkowany przez guz pociąga za spust
Mikrośrodowisko guza jest bogate w mleczan, produkt uboczny zmienionego metabolizmu nowotworu. Badanie pokazuje, że mleczan nie jest tylko odpadem metabolitycznym — aktywnie pomaga przełączyć ferroptozy w limfocytach. W porównaniu z innymi komórkami limfocyty CD8+ były szczególnie wrażliwe na mleczan. Gdy mleczan wnikał do komórek przez specyficzne transportery, powodował akumulację żelaza, kurczenie mitochondriów, utratę DNA mitochondrialnego i większe uszkodzenia oksydacyjne. Jednocześnie mleczan zwiększał aktywność STING i TOX oraz dodatkowo hamował HO-1. Limfocyty pozbawione STING lub TOX były znacznie bardziej odporne na uszkodzenia wywołane mleczanem. Zablokowanie kluczowego transportera mleczanu lekiem (AZD3965) chroniło limfocyty CD8+ przed ferroptozą u myszy, zwiększało ich obecność w guzach i spowalniało wzrost nowotworów, naśladując korzyść z genetycznego usunięcia STING w limfocytach.
Przekształcenie słabości w przewagę terapeutyczną
Te mechanistyczne wnioski mają praktyczne implikacje. Gdy badacze użyli terapii adoptacyjnej — przetoczyli myszy limfocyty aktywowane w laboratorium — okazało się, że limfocyty zaprojektowane bez STING lub TOX dawały znacznie lepszą kontrolę nad guzem niż normalne limfocyty. Co więcej, łączenie tych „odpornych na ferroptozę” limfocytów z istniejącymi terapiami, takimi jak inhibitory punktów kontrolnych PD-1 lub TIM-3, chemioterapia cisplatyną czy lek aktywujący STING, przyniosło wyraźnie lepsze zmniejszenie guzów niż każda z terapii osobno. Wreszcie w próbkach guzów od pacjentów z rakiem szyjki macicy wyższy poziom TOX i niższy HO-1 w naciekających limfocytach korelował z gorszym przeżyciem, sugerując, że ta ścieżka wpływa również na kliniczne wyniki u ludzi.
Co to oznacza dla przyszłej opieki onkologicznej
Mówiąc prosto, badanie ujawnia, że guzy mogą zmuszać nasze najsilniejsze limfocyty przeciwnowotworowe do „rdzewienia” od środka przez wywoływanie żelazem napędzanej formy śmierci komórkowej. Obwód mleczan–STING–TOX obniża ochronę zapewnianą przez HO-1, uszkadza mitochondria i prowadzi do ferroptozy, przerzedzając szeregi efektywnych limfocytów CD8+. Zakłócenie tego obwodu — przez inżynierię limfocytów pozbawionych STING lub TOX, zwiększenie HO-1 lub blokowanie wejścia mleczanu — utrzymuje limfocyty przy życiu, pełne energii i gotowe do ataku. Praca ta wskazuje drogę do następnej generacji immunoterapii, łączącej modyfikacje metaboliczne i genetyczne limfocytów z istniejącymi lekami, aby przełamać oporność i dostarczyć trwalszą kontrolę nowotworową.
Cytowanie: Zhu, Q., Zhang, Jb., Nie, Cp. et al. STING synergizes with TOX suppressing HO-1 expression to trigger ferroptosis in tumor-infiltrating CD8+ T cell and immunotherapy resistance. Nat Commun 17, 2543 (2026). https://doi.org/10.1038/s41467-026-69350-y
Słowa kluczowe: immunoterapia przeciwnowotworowa, limfocyty CD8, ferroptoza, mikrośrodowisko guza, szlak STING TOX HO-1