Clear Sky Science · pl
Seq-Scope-eXpanded: przestrzenna omika poza rozdzielczością optyczną
Widzieć komórki w ostrzejszym detalu
Nasze ciało zbudowane jest z niezliczonych maleńkich komórek, z których każda tętni aktywnością, której zwykle nie dostrzegamy nawet za pomocą silnych mikroskopów. W artykule opisano Seq-Scope-X — technologię pozwalającą badaczom przyjrzeć się wewnętrznej organizacji tkanek z bezprecedensową klarownością, mapując, które geny i białka są aktywne w precyzyjnych punktach wewnątrz i między komórkami. Taki poziom szczegółu może zmienić sposób badania rozwoju, układu odpornościowego oraz chorób, takich jak nowotwory czy uszkodzenia wątroby.
Dlaczego mapować cząsteczki in situ?
Komórki nie działają w izolacji: żyją w sąsiedztwach, tworzą warstwy i wyspecjalizowują się w zależności od położenia. Tradycyjne metody sekwencjonowania rozdrabniają tkanki, tracąc ten kontekst przestrzenny. Nowsze narzędzia „omiki przestrzennej” utrzymują cząsteczki na miejscu, ale wiąże się to z kompromisami. Metody oparte na obrazowaniu widzą bardzo drobne szczegóły, lecz zwykle śledzą ograniczoną liczbę genów. Metody sekwencjonowania mogą odczytać prawie każdy gen naraz, lecz rozmywają drobne cechy, często rozpraszając sygnał na kilka mikrometrów — więcej niż wiele struktur podkomórkowych. Autorzy postawili sobie za cel zamknięcie tej luki: zachować bogaty, nieobciążony wyborem zapis sekwencyjny przy jednoczesnym osiągnięciu, a nawet przewyższeniu ostrości nowoczesnych mikroskopów.
Rozciąganie tkanki, by pokonać ograniczenia optyczne
Główna idea Seq-Scope-X jest pozornie prosta: delikatnie powiększyć samą tkankę, tak by każdy pierwotny nanometr struktury stał się łatwiejszy do rozróżnienia. Zespół najpierw zakotwicza cząsteczki RNA — lub specjalne znaczniki DNA przyczepione do przeciwciał — w miękkim hydrożelu utworzonym wokół plastra tkanki. Następnie usuwa się pierwotną tkankę enzymatycznie i pęcznieje żel w roztworze solnym, fizycznie rozciągając wszystko około trzykrotnie przy zachowaniu względnych pozycji. Rozszerzony żel nakłada się na bardzo gęsty chip do sekwencjonowania pokryty sondami chwytającymi. Poprzez ostrożne podgrzanie konstrukcji, zakotwiczone cząsteczki są uwalniane z żelu i ponownie przyłączane do chipa, który następnie poddaje się sekwencjonowaniu, aby ujawnić, które geny lub białka znajdowały się w każdej maleńkiej współrzędnej. 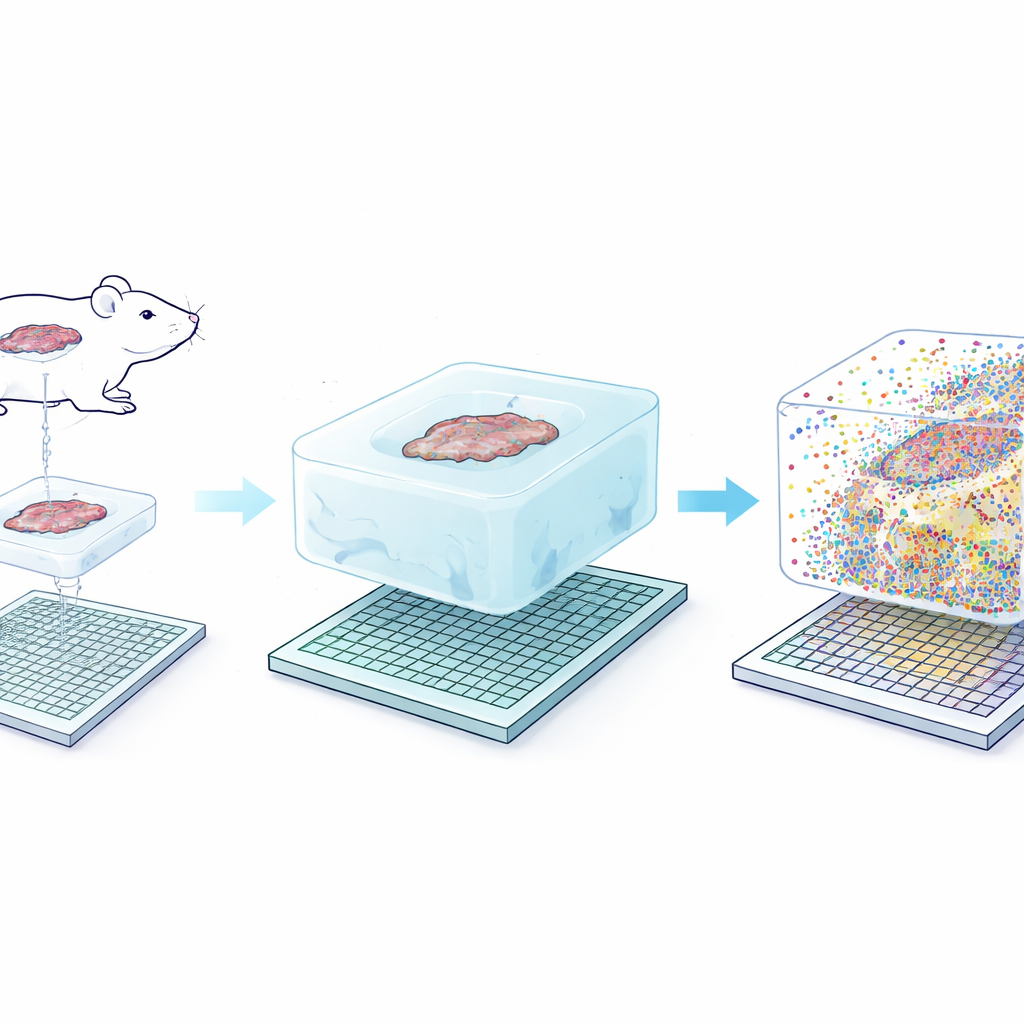
Od zamazanych komórek do map podkomórkowych
Gdy badacze zastosowali Seq-Scope-X do wątroby myszy, odkryli, że metoda poprawiła rozdzielczość przestrzenną z około 0,6 mikrometra do około 0,2 mikrometra i zwiększyła liczbę mierzalnych pozycji na milimetr kwadratowy niemal dziesięciokrotnie. W praktyce to, co wcześniej wyglądało jak nieostre plamy sygnału, teraz rozdzielało się na wyraźne zarysy pojedynczych komórek. Co jeszcze bardziej uderzające, skupiska RNA, które nie zostały jeszcze w pełni przetworzone (niezmontowane), układały się ciasno wokół jąder, podczas gdy dojrzałe RNA (zmontowane) przebiegało w otaczającej cytoplazmie. Pozwoliło to autorom wyznaczać granice komórek używając jedynie RNA oraz oddzielać jądrowe i cytoplazmatyczne odczyty genów dla niemal każdego hepatocytu w tkance — coś, do czego poprzednie metody sekwencjonowania mogły jedynie się domyślać.
Komórki o podzielonej tożsamości
Dzięki tej nowej klarowności zespół odkrył nieoczekiwany rodzaj molekularnego „podwójnego życia” wewnątrz komórek wątroby. Wzdłuż dobrze znanego gradientu od naczyń krwionośnych po stronie portalnej płacika wątrobowego do naczyń po stronie centralnej, hepatocyty wyspecjalizowane są w różne zadania metaboliczne. Seq-Scope-X pokazał, że w wielu komórkach profil genów w jądrze nie zgadzał się z profilem w otaczającej cytoplazmie. Około jedna trzecia hepatocytów wydawała się mieć profil jądrowy zgodny z jedną strefą, a profil cytoplazmatyczny zgodny z sąsiednią strefą. Niezależne metody obrazowania, w tym MERFISH i pojedynczocząsteczkowe testy fluorescencyjne RNA, potwierdziły, że indywidualne transkrypty mogą koncentrować się albo w jądrze, albo w cytoplazmie. Wspólnie wyniki te sugerują, że hepatocyty mogą dynamicznie zmieniać swoje role metaboliczne w czasie, gdzie jądro przygotowuje przyszły stan, podczas gdy cytoplazma odzwierciedla stan aktualny. 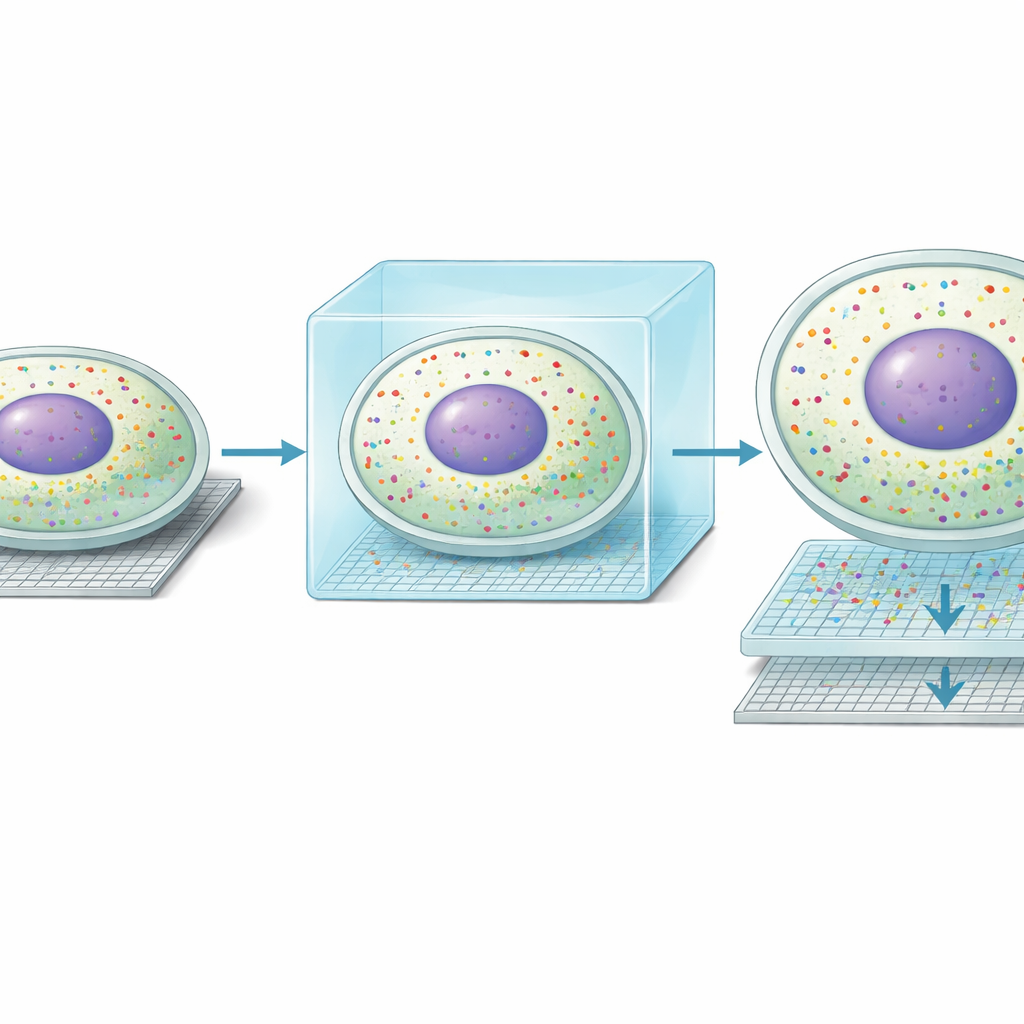
Powyżej wątroby: mózg, jelito i tkanki odpornościowe
Autorzy następnie sprawdzili, czy Seq-Scope-X działa w innych narządach. W mózgu metoda wyraźnie odróżniła różne typy neuronów i komórki wspierające oraz ujawniła podkomórkowe wzory RNA wokół jąder. W jelicie grubym rozróżniła podtypy komórek kubkowych i warstwy koloniocytów wzdłuż osi gruczoł — powierzchnia, ponownie wychwytując sygnatury jądrowe. Być może najbardziej spektakularnie zespół zaadaptował metodę do białek, używając przeciwciał opatrzonych kodami DNA w śledzionie myszy i migdale ludzkiej. Seq-Scope-X potrafił jednocześnie zmapować ponad sto różnych markerów powierzchniowych komórek w rozdzielczości pojedynczej komórki, rozróżniając gęsto upakowane podzbiory limfocytów T i B oraz komórki mieloidalne. Przechodząc na chemię żelu o większej zdolności do rozszerzania, osiągnęli efektywną rozdzielczość zbliżoną do prawdziwej skali nanometrycznej, przy jednoczesnym zachowaniu architektury tkanki wystarczająco dobrze do szczegółowego mapowania.
Co to oznacza na przyszłość
Seq-Scope-X pokazuje, że fizyczne powiększanie tkanek przed sekwencjonowaniem może pokonać długo utrzymywane ograniczenia rozdzielczości, dostarczając niemal mikroskopowego poziomu szczegółu, a jednocześnie odczytując tysiące genów lub znaczników białkowych naraz. Dla obserwatora niezwiązanego ze specjalnością naukową oznacza to, że naukowcy mogą teraz budować „atlasy molekularne”, które nie tylko informują, gdzie znajdują się poszczególne komórki, lecz także ujawniają, co dzieje się w różnych częściach każdej komórki. Takie mapy mogą pomóc wyjaśnić, jak tkanki reagują na uraz, jak komórki odpornościowe organizują się w narządach limfatycznych i guzach, albo jak subtelne przesunięcia wewnątrz komórek zapowiadają chorobę. Chociaż potrzebne są dalsze udoskonalenia, by zwiększyć zasięg i poprawić niektóre panele znakowań, Seq-Scope-X otwiera potężne nowe okno na mikroskopijne krajobrazy leżące u podstaw zdrowia i choroby.
Cytowanie: Anacleto, A., Cheng, W., Feng, Q. et al. Seq-Scope-eXpanded: spatial omics beyond optical resolution. Nat Commun 17, 2564 (2026). https://doi.org/10.1038/s41467-026-69346-8
Słowa kluczowe: transkryptomika przestrzenna, powiększanie tkanki, omika pojedynczych komórek, proteomika przestrzenna, zonacja wątroby