Clear Sky Science · pl
IPA pochodzące od mikrobioty chroni przed zapaleniem jelita, regulując jelitową ketogenezę pośredniczoną przez HMGCS2, aby ułatwić gojenie błony śluzowej
Dlaczego bakterie jelitowe mają znaczenie dla uszkodzonego jelita
Gdy wyściółka jelita zostaje uszkodzona, jak w zapalnych chorobach jelit (IBD) lub po agresywnych zabiegach medycznych, organizm musi szybko naprawić tę wewnętrzną „skórę”, aby zapobiec przedostawaniu się szkodliwych treści do krwiobiegu. W badaniu tym wyjaśniono, jak pojedyncza cząsteczka wytwarzana przez korzystne bakterie jelitowe może pomóc jelitu w samonaprawie, wskazując na nowe sposoby leczenia przewlekłych zaburzeń jelit bez szerokiego tłumienia układu odpornościowego.
Pomocny sygnał od przyjaznych mikroorganizmów
Naukowcy zaczęli od porównania chemicznych odcisków palców (profilów metabolitów) ze próbek stolca osób z IBD i zdrowych ochotników oraz z kilku modeli mysich zapalenia jelita. Spośród setek cząsteczek wyróżniła się jedna: kwas indolopropionowy (IPA), produkt rozpadu aminokwasu tryptofanu wytwarzany przez niektóre bakterie jelitowe. Poziomy IPA były konsekwentnie niższe u osób z chorobą Leśniowskiego-Crohna i u myszy z zapaleniem jelita niż u zdrowych odpowiedników. Sugerowało to, że utrata IPA może być częścią tego, co idzie nie tak, gdy wyściółka jelita ulega zapaleniu i nie potrafi się zregenerować.
Wzmacnianie ochronnej bariery jelita
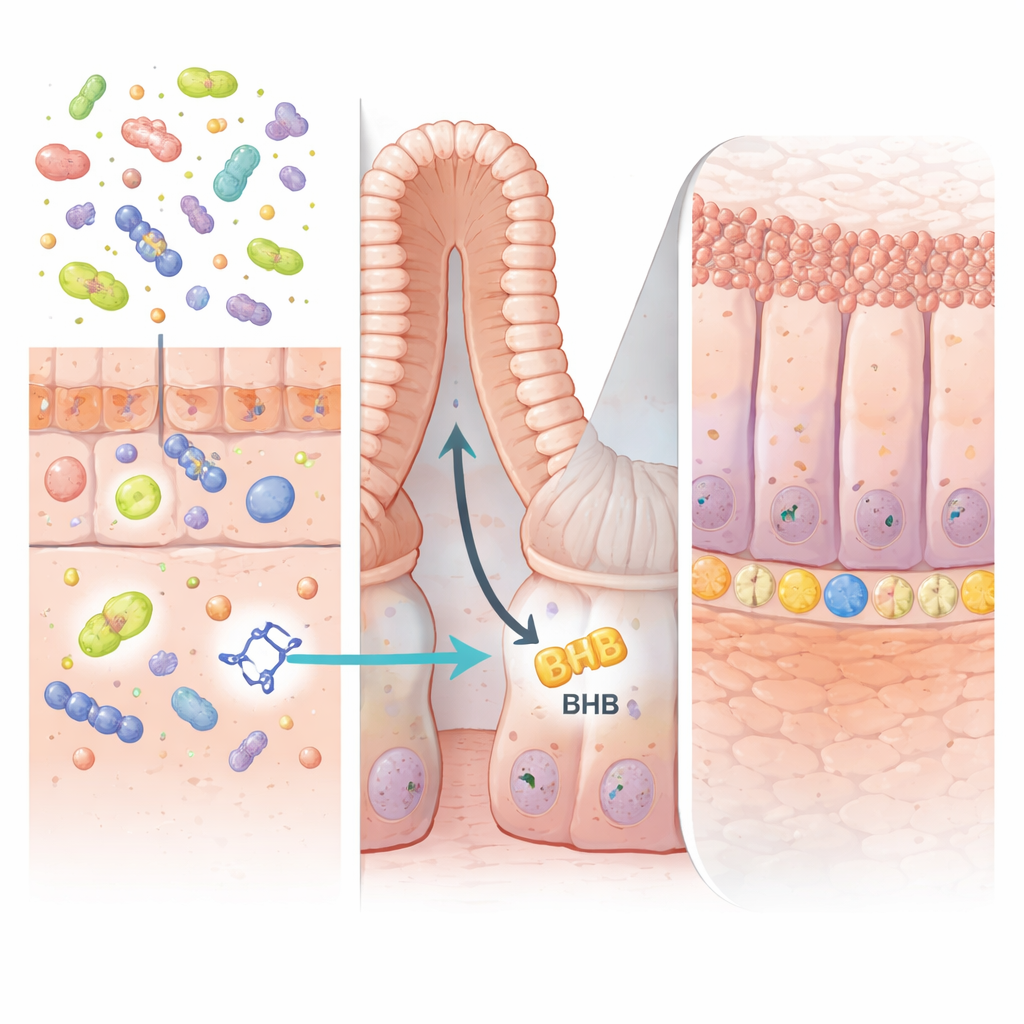
Aby sprawdzić, czy IPA jedynie towarzyszy chorobie, czy rzeczywiście chroni przed nią, zespół podawał IPA myszom przed wywołaniem różnych rodzajów uszkodzeń jelit, w tym chemicznego zapalenia jelita i uszkodzeń przez promieniowanie. Myszy otrzymujące odpowiednie dawki IPA miały dłuższe, zdrowsze jelita grubego, mniej zmian zapalnych w obrazie mikroskopowym oraz grubszą warstwę śluzu z ciasniejszymi połączeniami międzykomórkowymi. Przepuszczały mniej markerów zapalnych i miały więcej komórek kubkowych, które produkują ochronną powłokę śluzową. Co istotne, korzyści te obserwowano nawet u myszy wolnych od drobnoustrojów (germ-free), które nie mają populacji mikrobiomu, co pokazuje, że gdy IPA jest obecne, może działać bezpośrednio na wyściółkę jelita bez potrzeby obecności innych drobnoustrojów.
Zasilanie komórek macierzystych specjalnym rodzajem energii
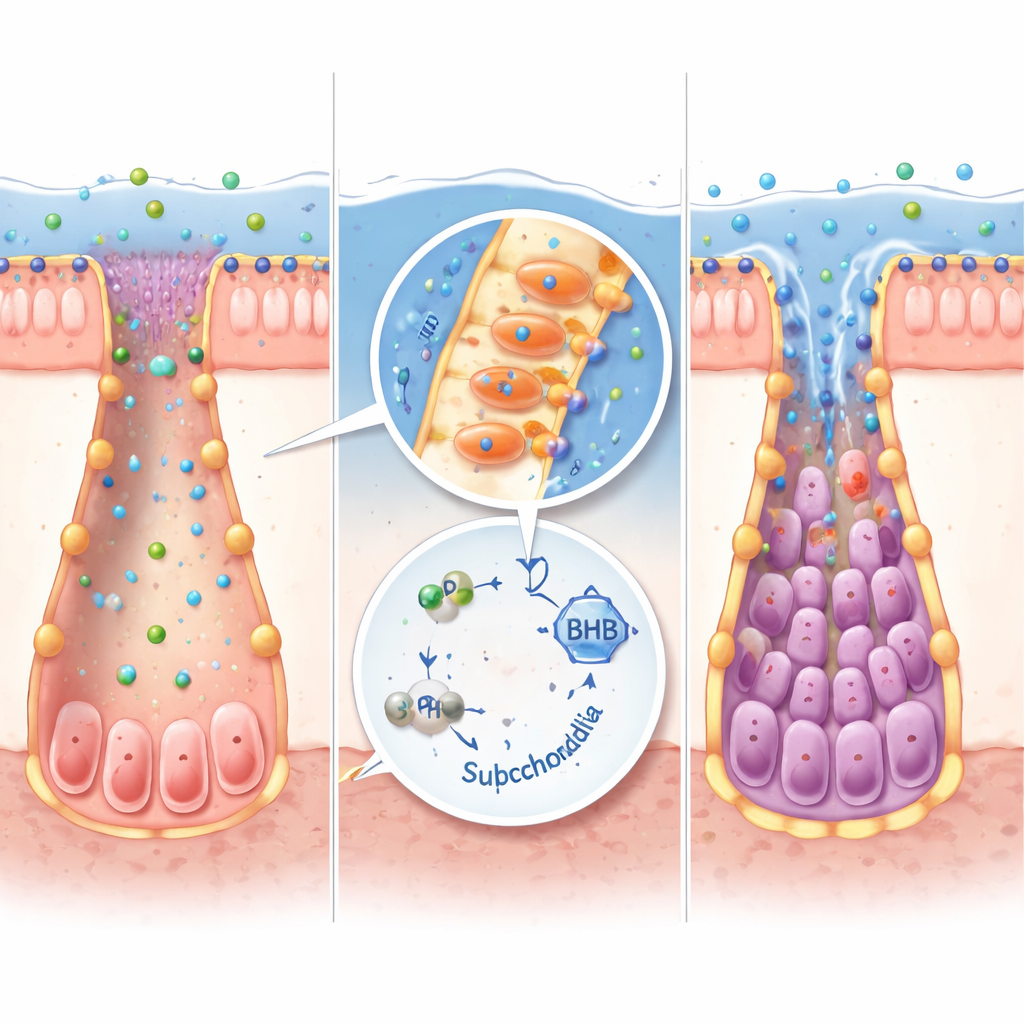
Klucz działania IPA leżał głęboko w jelitowych „kryptach” — małych kieszonkach, w których siedzą komórki macierzyste i stale odnawiają wyściółkę. Autorzy wykazali, że IPA aktywuje białko zwane PPARα w komórkach nabłonka jelitowego. To z kolei zwiększa produkcję enzymu HMGCS2, który napędza ketogenezę — proces wytwarzania wysokoenergetycznej cząsteczki β-hydroksymaślanu (BHB). Podwyższony poziom BHB w ścianie jelita pobudzał komórki macierzyste LGR5-dodatnie do ekspansji i szybszej regeneracji uszkodzonej tkanki. Kiedy enzym HMGCS2 lub PPARα został selektywnie usunięty z komórek jelitowych myszy, IPA nie mogło już zwiększać aktywności komórek macierzystych ani chronić przed zapaleniem jelita, co potwierdza, że ta droga produkcji ketonów jest niezbędna.
Od bakteryjnych „fabryk” do ludzkich tkanek
Nie wszystkie bakterie jelitowe potrafią wytwarzać IPA. Reanalizując duże zbiory danych mikrobiomu, badacze zidentyfikowali Peptostreptococcus russellii jako kluczowego producenta IPA, którego brakuje w kilku kohortach IBD. W hodowlach laboratoryjnych ten szczep efektywnie przekształcał tryptofan w IPA. Gdy myszy wolne od drobnoustrojów zostały skolonizowane P. russellii, ich poziomy IPA wzrosły, geny związane z produkcją ketonów zostały włączone, markery komórek macierzystych zwiększyły się, a ciężkość zapalenia jelita zmalała w porównaniu z myszami otrzymującymi ogólny przeszczep mikrobioty. Ta sama ścieżka IPA–ketony działała w miniaturowych organoidach jelitowych hodowanych z tkanek mysich i ludzkich, gdzie dodanie IPA lub BHB pomagało komórkom macierzystym odbudować się po uszkodzeniach zapalnych, jednocześnie tłumiąc sygnały prozapalne.
Co to może znaczyć dla przyszłego leczenia
Podsumowując, praca tę przedstawia prosty, lecz silny ciąg zdarzeń: niektóre bakterie jelitowe przekształcają dietetyczny tryptofan w IPA; IPA uruchamia metaboliczny przełącznik w komórkach jelitowych; przełącznik ten zwiększa produkcję BHB; a BHB z kolei ożywia komórki macierzyste, które odbudowują wyściółkę jelita. Dla osób z IBD lub innymi stanami uszkadzającymi barierę jelitową terapie przywracające IPA lub bezpiecznie naśladujące jego działanie — poprzez dietę, ukierunkowane probiotyki lub zaprojektowane leki — mogłyby sprzyjać prawdziwemu gojeniu błony śluzowej bez szerokiego hamowania odporności. Chociaż potrzeba więcej badań u pacjentów, oś mikroba–metabolit–komórka macierzysta oferuje obiecujący nowy kierunek naprawy jelita od środka.
Cytowanie: Zhang, Y., Tu, S., Shao, X. et al. Microbiota-derived IPA protects against colitis by regulating intestinal HMGCS2-mediated ketogenesis to facilitate mucosal healing. Nat Commun 17, 2437 (2026). https://doi.org/10.1038/s41467-026-69341-z
Słowa kluczowe: mikrobiom jelitowy, komórki macierzyste jelit, zapalenie jelit, metabolity mikrobiologiczne, gojenie błony śluzowej