Clear Sky Science · pl
Ocena wnioskowania o szlaku sygnalizacyjnym EGF z użyciem fosfoproteomiki i interakcji kinaza-substrat
Dlaczego to ma znaczenie poza laboratorium
Nasze komórki nieustannie nasłuchują i reagują na sygnały ze środowiska. Jednym z najważniejszych takich sygnałów jest czynnik wzrostu naskórka (EGF), który pomaga kontrolować, jak komórki rosną, dzielą się i przetrwają. Gdy ten system komunikacji zawodzi, może napędzać nowotwory i inne choroby. W tym badaniu zadano pozornie proste pytanie o dalekosiężnych implikacjach: jeśli użyjemy współczesnych, wydajnych technologii pomiarowych i modeli komputerowych, o ile lepiej możemy naprawdę zrozumieć szlak sygnalizacyjny EGF niż to, co pokazują podręcznikowe schematy?
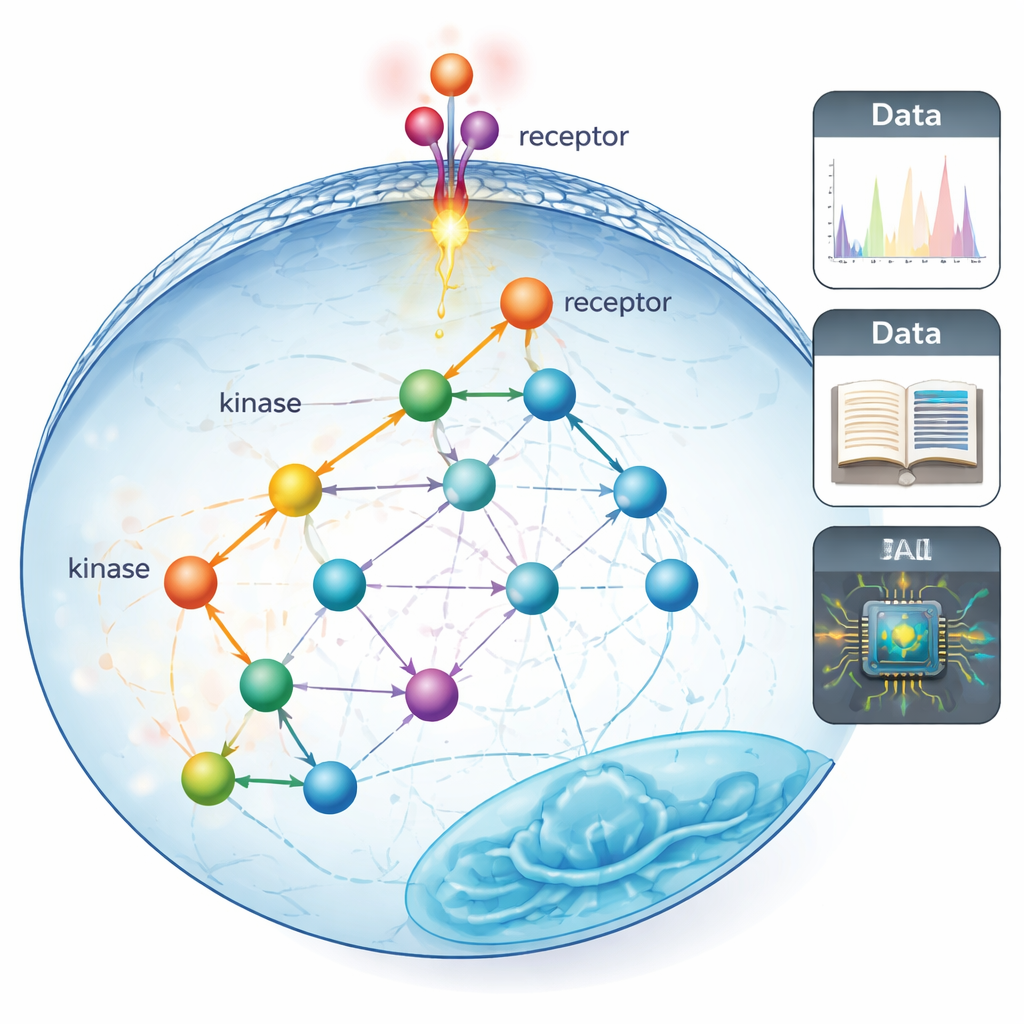
Od prostych linii do rzeczywistych schematów okablowania
Tradycyjne „szlaki sygnalizacyjne” często rysowane są jako uporządkowane, niemal liniowe łańcuchy białek przekazujących sygnał od powierzchni komórki do jądra. Mapy te powstawały przez dekady w oparciu o powolne, ukierunkowane eksperymenty, które mogły badać tylko kilka białek naraz. Autorzy twierdzą, że pozostawiło to wąskie, „pod latarnią” spojrzenie: dużo wiemy o niewielu białkach, które było łatwo badać, a znacznie mniej o szerszej sieci powiązań, która prawdopodobnie istnieje w rzeczywistych komórkach.
Nasłuchiwanie tysięcy molekularnych przełączników naraz
Aby wyjść poza to ograniczone spojrzenie, zespół użył fosfoproteomiki — techniki spektrometrii mas, która w jednym eksperymencie śledzi dziesiątki tysięcy małych chemicznych znaczników, zwanych grupami fosforanowymi, na białkach. Znaczniki te umieszczane są przez enzymy zwane kinazami i działają jak szybkie przełączniki on–off dla sygnalizacji. Badacze najpierw złożyli najbardziej wszechstronną mapę „kto może fosforylować kogo”, łącząc trzy typy informacji: ręcznie zanonimizowane wyniki z literatury, przewidywania z modelu sztucznej inteligencji analizującego sekwencje białkowe oraz duże eksperymentalne przesiewy preferencji kinaz. To znacznie rozszerzyło pokrycie znanych lub podejrzewanych relacji kinaza–substrat z około 5% możliwych miejsc do nawet 70–80%.
Test wytrzymałościowy sygnalizacji EGF w wielu eksperymentach
Następnie skupili się na odpowiedzi na EGF — klasycznym szlaku i głównym graczu w nowotworach płuc, piersi, skóry i mózgu. Grupa połączyła trzy opublikowane, nowoczesne zestawy danych ze trzema nowymi, bardzo głębokimi pomiarami zależnymi od czasu w komórkach pochodzenia nerkowego oraz dwoma badaniami kontrolnymi z różnymi bodźcami. Razem te eksperymenty zmierzyły ponad 40 000 miejsc fosforylacji na zestaw danych i śledziły, jak zmieniały się w minutach po stymulacji EGF. Choć ogólne wzorce różniły się nieco między typami komórek i technologiami, kluczowe miejsca fosforylacji w szlaku EGF były wielokrotnie aktywowane, potwierdzając, że rdzeń sygnału jest odporny nawet w zróżnicowanych eksperymentach.
Odtwarzanie ukrytej rozmowy między kinazami
Po ustaleniu, które kinazy stały się bardziej lub mniej aktywne, autorzy próbowali zrekonstruować leżącą u podstaw „rozmowę” między nimi: które kinazy prawdopodobnie aktywują lub wpływają na inne. Przekształcili swoje mapy kinaza–substrat w sieci kinaza–kinaza i zastosowali trzy strategie obliczeniowe, od prostych schematów rankingu po bardziej złożone podejście zmuszające wynik do wyglądu jak skierowane drzewo z korzeniem w receptorze EGF. Porównali wnioski z tej rekonstrukcji z kilkoma rodzajami „prawdy bazowej”: starannie opracowaną mapą EGF z bazy danych, eksperymentami na dużą skalę, w których pojedyncze kinazy były nadeksprymowane, oraz parami miejsc kinaz, których zachowanie było silnie skorelowane w czasie.
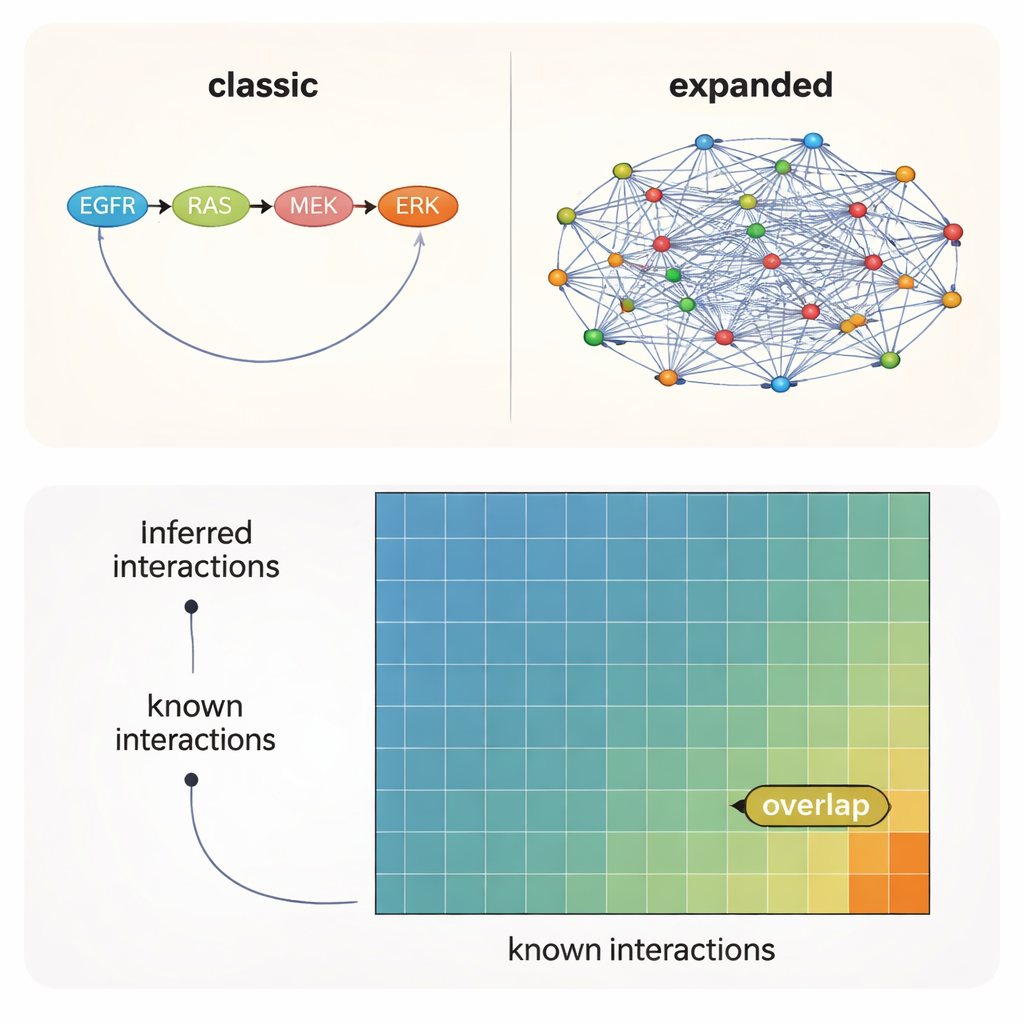
Najbardziej prawdopodobne połączenia wciąż poza oficjalną mapą
We wszystkich testach jedna wiadomość była jasna: wybór wiedzy uprzedniej — czyli sieci początkowej podanej do algorytmu — miał większe znaczenie niż konkretna metoda czy nawet kontekst eksperymentalny. Sieci zbudowane na literaturze odtwarzały największą liczbę znanych interakcji, podczas gdy szersze zasoby predykcyjne wskazywały wiele dodatkowych, prawdopodobnych połączeń, które nie zostały jeszcze formalnie udokumentowane. Nawet w najlepszych warunkach tylko około 10–12% interakcji sugerowanych przez dane i modele było obecnych w którymkolwiek z zestawów referencyjnych. Innymi słowy, mniej więcej 90% popartych linków kinaza–kinaza leży na niezbadanym terytorium.
Co to oznacza dla przyszłych terapii
Dla osób niebędących specjalistami kluczowy wniosek jest taki, że znany schemat szlaku EGF z podręczników prawdopodobnie stanowi tylko wierzchołek góry lodowej. Nowoczesna fosfoproteomika w połączeniu z zaawansowanymi metodami obliczeniowymi ujawnia znacznie bogatszą i bardziej splątaną sieć sygnalizacyjną. Wiele z tych nowo sugerowanych połączeń może odzwierciedlać pominięte mechanizmy, dzięki którym komórki nowotworowe przekierowują sygnały, by uchodzić przed lekami, albo stanowić nowe możliwości projektowania mądrzejszych kombinacji leków. Badanie nie dowodzi, że każde nowe połączenie jest prawdziwe, ale dostarcza mapy drogowej i otwartych narzędzi dla badaczy do weryfikacji tych pomysłów, z ostatecznym celem opracowania bardziej precyzyjnych i skutecznych terapii w chorobach, gdzie sygnalizacja EGF odgrywa kluczową rolę.
Cytowanie: Garrido-Rodriguez, M., Potel, C., Burtscher, M.L. et al. Benchmarking EGF signaling pathway inference using phosphoproteomics and kinase-substrate interactions. Nat Commun 17, 2071 (2026). https://doi.org/10.1038/s41467-026-69332-0
Słowa kluczowe: sygnalizacja EGF, fosfoproteomika, kinazy białkowe, sieci sygnalizacyjne komórek, biologia nowotworów