Clear Sky Science · pl
Mycobacterium tuberculosis modyfikuje fosforylację podjednostki ATP6V1E1 gospodarza, aby promować przeżycie wewnątrzkomórkowe
Dlaczego to ma znaczenie w walce z gruźlicą
Gruźlica pozostaje jedną z najbardziej śmiertelnych chorób zakaźnych na świecie, zabijając ponad milion osób rocznie. Nasze komórki odpornościowe dysponują potężnymi „kwasowymi koszami recyklingowymi”, które zwykle trawią napadające mikroby. W artykule odkryto, jak bakteria gruźlicy, Mycobacterium tuberculosis (Mtb), sabotuje ten system zakwaszania wewnątrz naszych komórek, oraz wykazano, że lek celujący w ten mechanizm może pomóc zakażonym zwierzętom skuteczniej pozbyć się infekcji.
Kwasowa kąpiel komórki dla drobnoustrojów
Gdy bakterie gruźlicy trafiają do płuc drogą inhalacji, są szybko pochłaniane przez komórki odpornościowe zwane makrofagami. Bakterie lądują w pęcherzykach błonowych, które powinny łączyć się z lizosomami — małymi zbiornikami wypełnionymi enzymami trawiącymi, działającymi najlepiej w silnie kwaśnym środowisku. To zakwaszenie tworzy pompa molekularna, vacuolarna ATPaza (V-ATPaza), która zużywa paliwo komórkowe, by wtłaczać protony do lizosomów i obniżać ich pH. Prawidłowe zakwaszenie jest kluczowe dla rozkładu Mtb, jednak badania prowadzone przez dekady wykazały, że patogen w jakiś sposób utrzymuje swoje kompartmenty w mniej kwaśnym stanie i przeżywa.
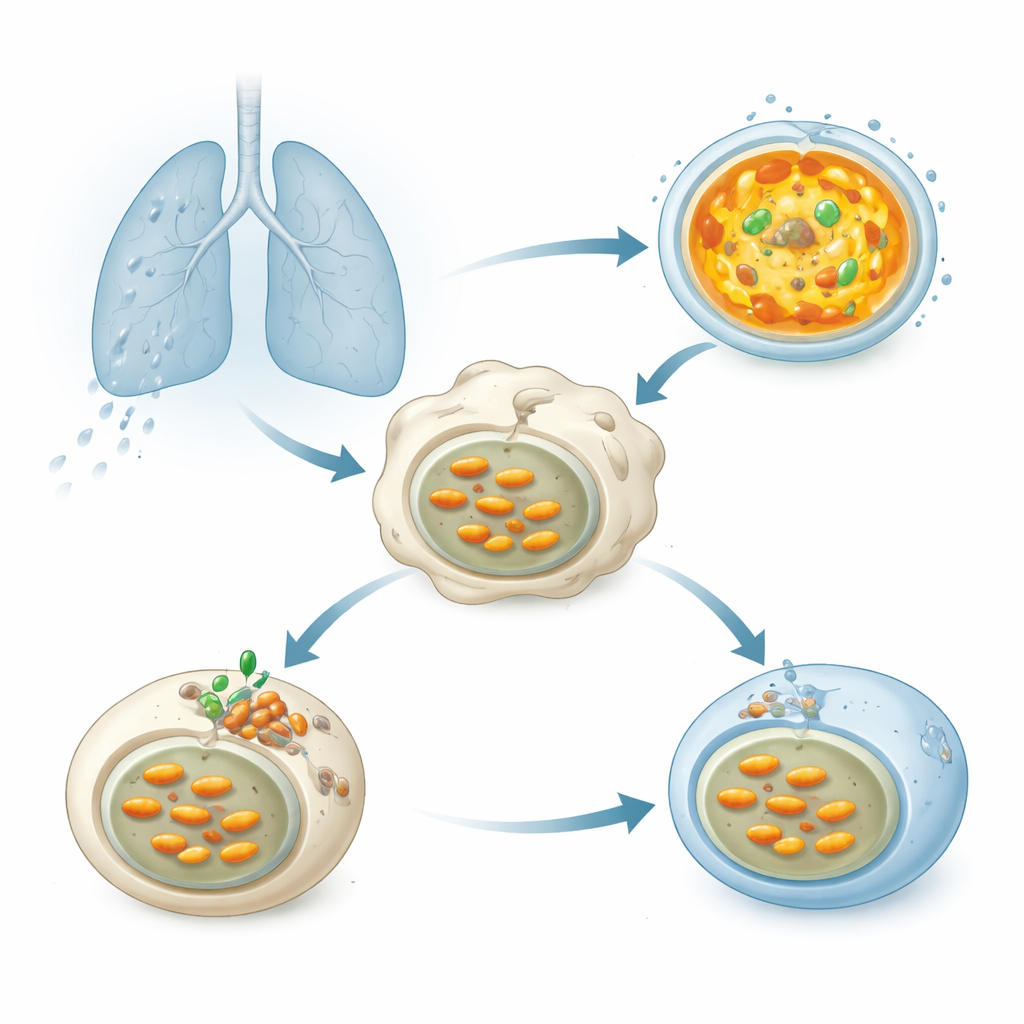
Ukryty bakteryjny pomocnik blokujący zakwaszanie
Naukowcy przeskanowali ponad 200 białek uwalnianych przez Mtb, aby sprawdzić, które osłabiają zakwaszanie lizosomów w ludzkich komórkach. Jeden wyróżnił się: enzym nazwany Chp2 (znany też jako Rv1184). Gdy komórki produkowały Chp2, ich lizosomy słabiej fluorescowały barwnikami wrażliwymi na kwas, co wskazywało na wyższe, mniej nieprzyjazne pH. Szczepy Mtb zaprojektowane bez Chp2 przestały tłumić zakwaszanie; w zakażonych makrofagach i u myszy te mutanty były skuteczniej eliminowane i wywoływały łagodniejsze uszkodzenia płuc. Przywrócenie Chp2 w szczepie mutantowym odwróciło zarówno blokadę zakwaszania, jak i zwiększone obciążenie bakteryjne, identyfikując Chp2 jako czynnik wirulencji pomagający Mtb utrzymywać się wewnątrz komórek gospodarza.
Podjednostka pompy gospodarza działająca jak przełącznik
Aby zrozumieć, jak Chp2 interferuje z zakwaszaniem, zespół poszukiwał elementów gospodarza, z którymi może się wiązać. Odkryli, że Chp2 bezpośrednio przyłącza się do konkretnej części V-ATPazy, podjednostki zwanej ATP6V1E1 (w skrócie E1), która pomaga stabilizować strukturę pompy. Zwiększenie ilości E1 w komórkach wzmocniło zakwaszanie lizosomów i utrudniło przetrwanie Mtb, podczas gdy zmniejszenie E1 miało odwrotny skutek. Myszy posiadające tylko jedną działającą kopię genu E1 miały mniej kwaśne lizosomy, wyższe obciążenie bakteryjne w płucach i poważniejsze uszkodzenia tkanek po zakażeniu, co pokazuje, że E1 jest ważnym czynnikiem obronnym gospodarza przeciw gruźlicy.
Znacznik kinazy na pompie, który osłabia kwas
Autorzy zapytali następnie, czy chemiczne „znaczniki” na E1 mogą regulować aktywność pompy. Odkryli, że dodanie grup fosforanowych do dwóch specyficznych tyrozyn (Tyr56 i Tyr57) na E1 działa jak hamulec: udawanie fosforylacji zmniejszało zakwaszanie i zapobiegało pełnemu złożeniu V-ATPazy, podczas gdy uniemożliwienie fosforylacji dawało efekt przeciwny. Przesiewając panel enzymów, zidentyfikowali kinazę o nazwie BMX jako białko gospodarza, które umieszcza tę modyfikację. Gdy BMX był blokowany genetycznie lub małą cząsteczką inhibitorową, fosforylacja E1 malała, pompa składała się sprawniej na błonach lizosomalnych, lizosomy stawały się bardziej kwaśne, a przetrwanie Mtb w makrofagach zmniejszało się.
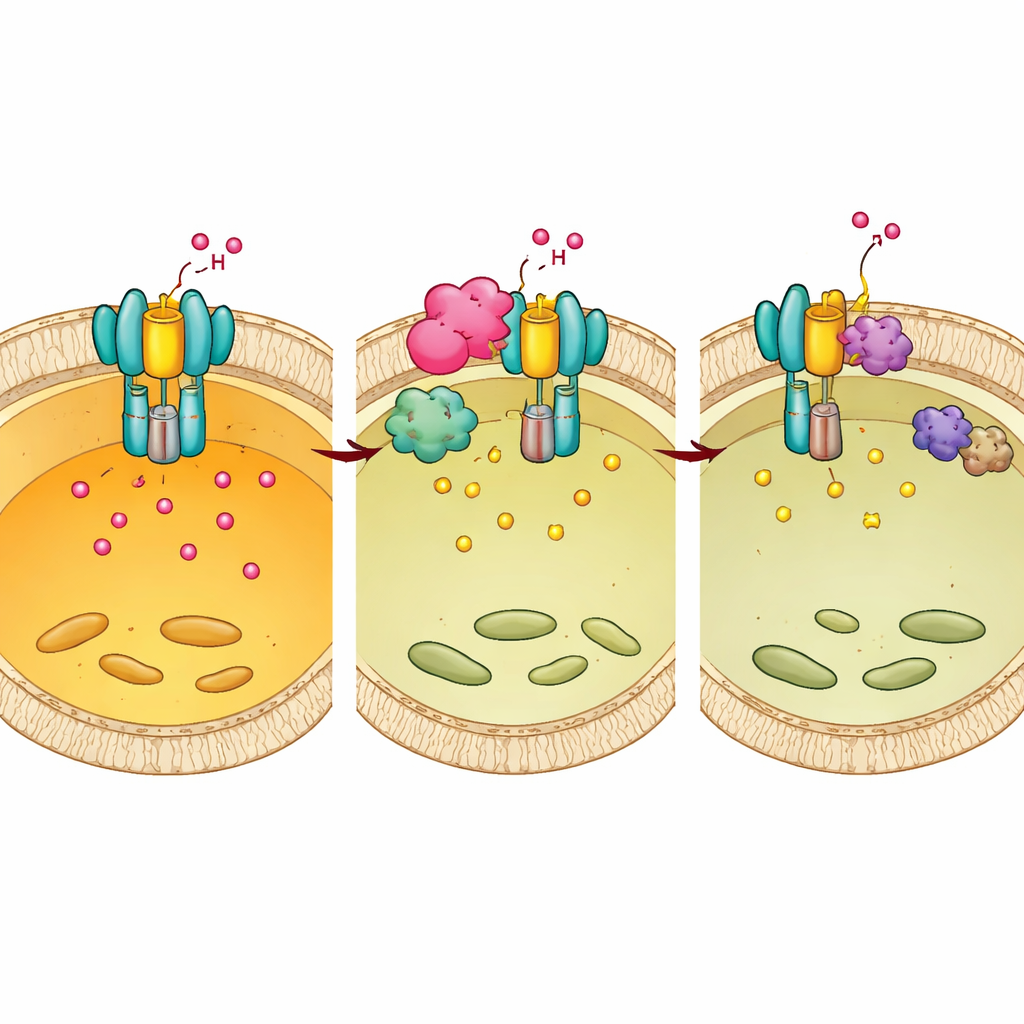
Jak Mtb przełącza przełącznik gospodarza na swoją korzyść
Okazało się, że Chp2 i BMX współdziałają. Eksperymenty strukturalne i biochemiczne wykazały, że Chp2 działa jako rusztowanie, które zbliża E1 i BMX na powierzchni lizosomu, wzmacniając fosforylację E1 na Tyr56/57. To dodatkowe znakowanie zakłóca pełne złożenie pompy, podnosi pH lizosomów i tworzy łagodniejsze środowisko, w którym Mtb może przetrwać. Gdy BMX był zahamowany, przewaga przetrwania nadawana przez Chp2 znikała zarówno w hodowlach komórkowych, jak i u zakażonych myszy. Co istotne, leczenie myszy inhibitorem BMX po zakażeniu zmniejszyło obciążenie bakteryjne i patologię płuc u normalnych zwierząt, ale nie u myszy z osłabionym E1, co wskazuje, że lek działa przez przywrócenie skutecznego zakwaszania napędzanego przez E1.
Przekształcenie bakteryjnego fortelu w pomysł na terapię
Mówiąc prostymi słowami, badanie pokazuje, że bakterie gruźlicy wrzucają do naszych komórek pomocnicze białko, które majstruje przy „pompie kwasu” na systemie usuwania odpadów, przygładzając ją na tyle, by mikroby uniknęły zniszczenia. Identyfikując podjednostkę pompy służącą jako główny pokrętło kontrolne (E1) oraz enzym gospodarza, który je przełącza (BMX), autorzy ujawniają precyzyjny punkt, w którym lek może interweniować. Hamowanie BMX u myszy skutecznie reaktywuje wewnętrzną „kwasową kąpiel” komórek i poprawia eliminację bakterii. Te odkrycia otwierają drogę do terapii ukierunkowanych na gospodarza, które sprawiają, że nasze własne komórki stają się bardziej nieprzyjazne dla Mtb, potencjalnie działając razem z antybiotykami i pomagając w walce z odporną na leki gruźlicą.
Cytowanie: Chen, J., Tang, F., Qin, L. et al. Mycobacterium tuberculosis modulates phosphorylation of host ATP6V1E1 to promote intracellular survival. Nat Commun 17, 2434 (2026). https://doi.org/10.1038/s41467-026-69331-1
Słowa kluczowe: gruźlica, lizosomy, terapia ukierunkowana na gospodarza, Mycobacterium tuberculosis, V-ATPaza