Clear Sky Science · pl
Przedwzrokowa sieć neuronalna kisspeptyna-nNOS-GnRH (KiNG) reguluje rytmiczność LH poprzez aktywację i hamowanie u myszy
Dlaczego ta historia z mózgu ma znaczenie dla płodności
Owulacja i płodność zależą od niewielkiej grupy komórek mózgowych, które uwalniają główny hormon w pulsach i okresowych szczytach. Gdy ten rytm się zaburza, reprodukcja może zawieść. Badanie to ujawnia, jak dwa rodzaje cząsteczek sygnałowych w mózgu myszy — jedna uruchamia aktywność, druga cicho ją wyłącza — współdziałają, by kształtować te hormonalne rytmy. Zrozumienie tego ukrytego obwodu czasowego może ostatecznie pomóc wyjaśnić niektóre formy niepłodności i zasugerować nowe sposoby leczenia zaburzeń rozrodczych.
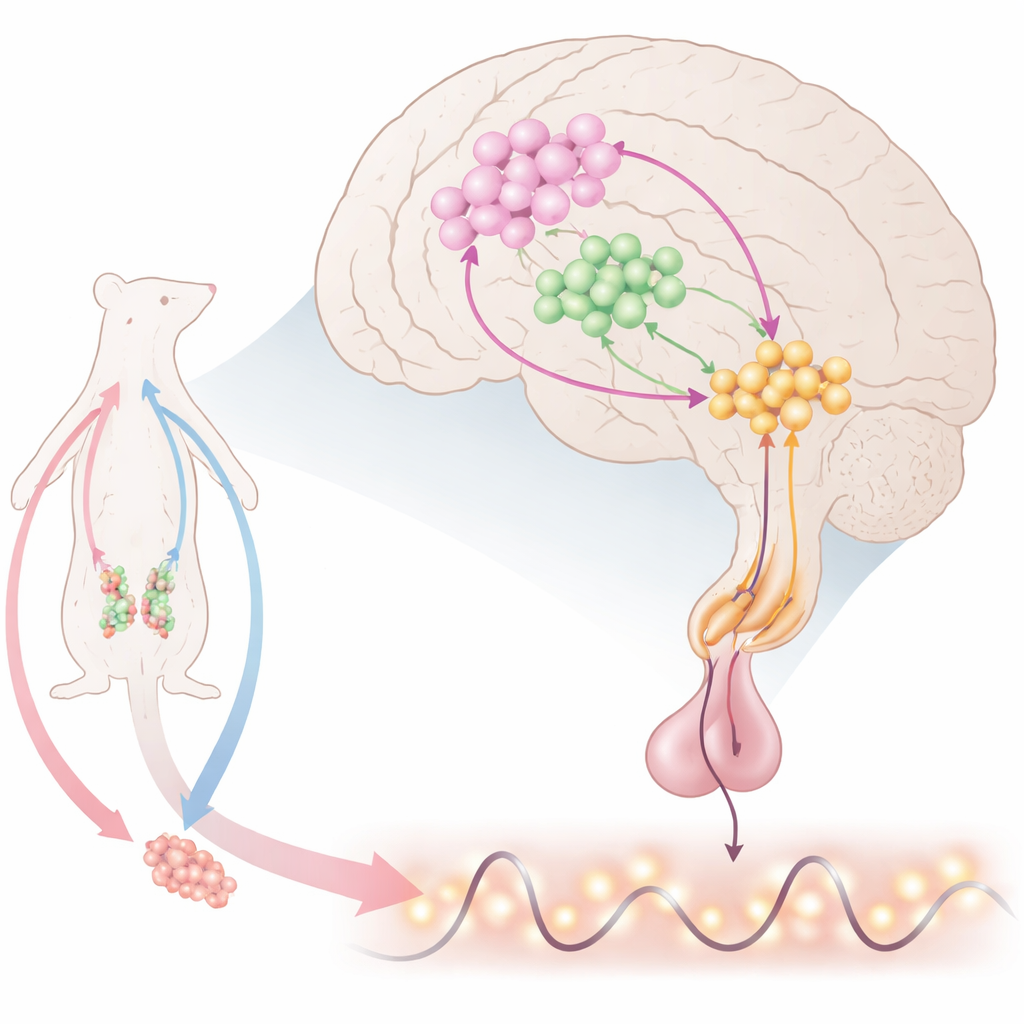
Zegarmistrz mózgu dla rozrodu
Głęboko w mózgu specjalne komórki nerwowe uwalniają hormon uwalniający gonadotropiny (GnRH), który informuje przysadkę mózgową, by wypuszczała hormon luteinizujący (LH) i hormon folikulotropowy. Te hormony kontrolują jajniki i jądra. GnRH nie jest wydzielany równomiernie; pojawia się w regularnych pulsach, a u samic także w dużym przedowulacyjnym wyrzucie. Naukowcy wiedzą, że wiele sygnałów dociera do komórek GnRH, ale dokładne połączenie, które generuje zarówno pulsacje, jak i wyrzuty, pozostawało niejasne. Praca ta koncentruje się na małym obszarze z przodu podwzgórza, gdzie komórki GnRH mieszają się z dwoma innymi istotnymi uczestnikami: neuronami produkującymi kisspeptynę, które pobudzają GnRH, oraz neuronami wytwarzającymi tlenek azotu (NO), gazowy sygnał, który może dyfundować na krótkie odległości.
Partnerstwo włącz–wyłącz między dwoma sygnałami
Naukowcy proponują trójskładnikową sieć „KiNG”, złożoną z kisspeptyny, neuronów produkujących NO (nNOS) oraz komórek GnRH. Kisspeptyna jest silnym aktywatorem, który może pobudzać uwalnianie GnRH i LH, ale stała stymulacja prowadzi do wyłączenia systemu, co sugeruje potrzebę wewnętrznego hamulca. Przy użyciu wysoce czułych sond molekularnych, narzędzi genetycznych i rejestracji aktywności w preparatach mózgowych myszy zespół pokazuje, że kisspeptyna robi więcej niż tylko bezpośrednio pobudzać neurony GnRH. Aktywuje też pobliskie neurony nNOS w obszarze przedwzrokowym, szczególnie w regionie zwanym OV/MePO. Gdy poziomy kisspeptyny rosną, komórki nNOS produkują serie impulsów NO, które wywołują produkcję drugiego przekaźnika, cGMP, w otaczających komórkach, w tym w samych neuronach GnRH. Ten sygnał NO–cGMP tłumi wyładowania GnRH, stanowiąc wbudowany wyłącznik dla napędu kisspeptynowego.
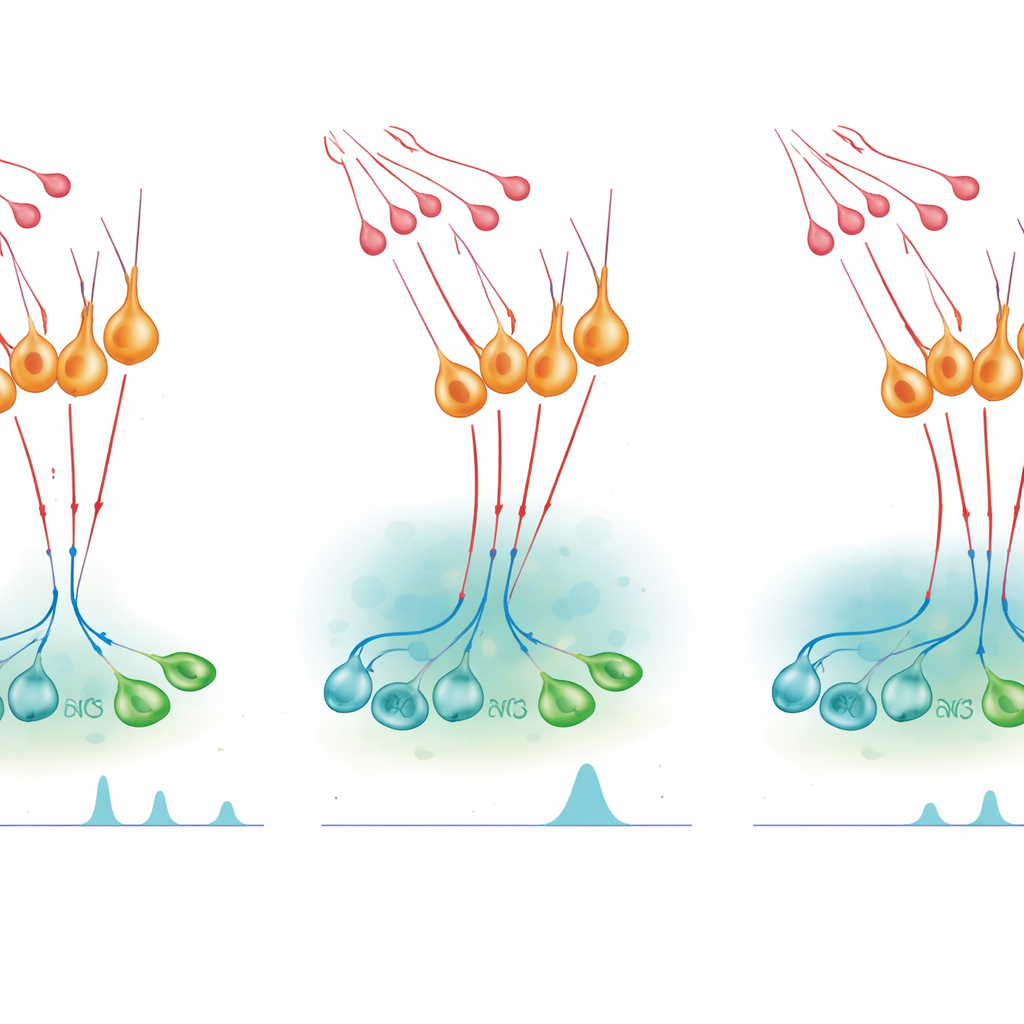
Włączanie wyrzutów hormonów i ich przycinanie
Aby sprawdzić, jak ten mikroukład wpływa na uwalnianie hormonów, zespół użył przełączników chemogenetycznych — receptorów zaprojektowanych tak, by aktywować je obojętne inaczej leki — aby włączać lub wyłączać neurony nNOS u żywych myszy. Sztuczne pobudzenie komórek nNOS w normalnie cichym etapie cyklu samicy wystarczyło, by wywołać przypominający wyrzut wzrost poziomu LH we krwi; podobne efekty obserwowano u samców. Zablokowanie produkcji NO niwelowało ten efekt, co pokazuje, że NO z tych neuronów jest niezbędne do wyrzutu. Jednak gdy naukowcy zahamowali neurony nNOS lub obniżyli ich wrażliwość na kisspeptynę, podanie kisspeptyny wywołało przesadzone i wydłużone podwyższenie LH. Leki farmakologiczne blokujące syntezę NO miały podobny wzmacniający efekt, podczas gdy lek wydłużający sygnalizację cGMP skracał odpowiedź na kisspeptynę i zmniejszał późniejsze wydzielanie LH. Razem te eksperymenty wskazują, że NO zarówno pomaga synchronizować neurony GnRH, aby tworzyć wyrzuty, jak i ogranicza czas trwania pobudzenia przez kisspeptynę.
Elastyczny rytm w trakcie cyklu jajnikowego
Badanie ujawnia także, że równowaga włącz–wyłącz zmienia się w trakcie cyklu samicy. Przy użyciu czułej metody detekcji RNA autorzy stwierdzili, że więcej neuronów nNOS wyraża receptor dla kisspeptyny na dzień przed owulacją, gdy poziomy estrogenu są wysokie i występuje wyrzut LH. W spokojniejszych fazach mniej neuronów nNOS reaguje na kisspeptynę, produkując jedynie małe, miejscowe ilości NO, które łagodnie powstrzymują pulsacje GnRH bez ich zatrzymania. W dniu wyrzutu silniejszy napływ kisspeptyny i zwiększona ekspresja receptora znacznie zwiększają produkcję NO, pozwalając mu rozprzestrzenić się dalej i chwilowo wyciszyć wiele neuronów GnRH jednocześnie. Gdy sygnał NO słabnie, te komórki wspólnie odbijają się z powrotem, generując duży, skoordynowany wyrzut LH potrzebny do owulacji.
Co to oznacza dla zdrowia ludzi
Mówiąc prosto, praca ta pokazuje, że ten sam sygnał, który uruchamia neurony GnRH — kisspeptyna — równocześnie rekrutuje opóźniony system hamujący za pośrednictwem NO, zapewniając, że hormonalne wybuchy są silne, ale nie wymykają się spod kontroli. Sieć KiNG działa więc zarówno jako przyspieszacz, jak i hamulec dla rozrodczego zegara, regulując pulsacje GnRH w większości cyklu i kształtując wyrzut, który wyzwala owulację. Ponieważ u ludzi wykryto zmiany genetyczne w szlakach kisspeptyny i NO w przypadkach problemów rozrodczych, zrozumienie tego precyzyjnie zrównoważonego układu może pomóc w opracowaniu nowych podejść do diagnozy i leczenia niepłodności oraz pokrewnych schorzeń.
Cytowanie: Delli, V., Moulinier, M., Lazaridou, AM. et al. Preoptic kisspeptin-nNOS-GnRH (KiNG) neuronal network regulates LH rhythmicity through activation-inhibition in mice. Nat Commun 17, 2558 (2026). https://doi.org/10.1038/s41467-026-69316-0
Słowa kluczowe: hormony rozrodcze, podwzgórze, kisspeptyna, tlenek azotu, czas owulacji