Clear Sky Science · pl
Laktylacja histonów zwiększa ekspresję CXCL1, sprzyjając naciekowi neutrofili i unikaniu odpowiedzi immunologicznej w raku trzustki
Dlaczego to badanie nad nowotworem ma znaczenie
Rak trzustki jest jednym z najbardziej śmiertelnych nowotworów, między innymi dlatego, że często opiera się nowoczesnym immunoterapiom, które działają w innych typach guzów. To badanie ujawnia, jak guzy trzustki przestawiają własny metabolizm cukrów, by po cichu unieszkodliwić układ odpornościowy, oraz jak zablokowanie tego procesu może otworzyć drogę dla obrony organizmu — i już dostępnych leków — do skuteczniejszej walki.
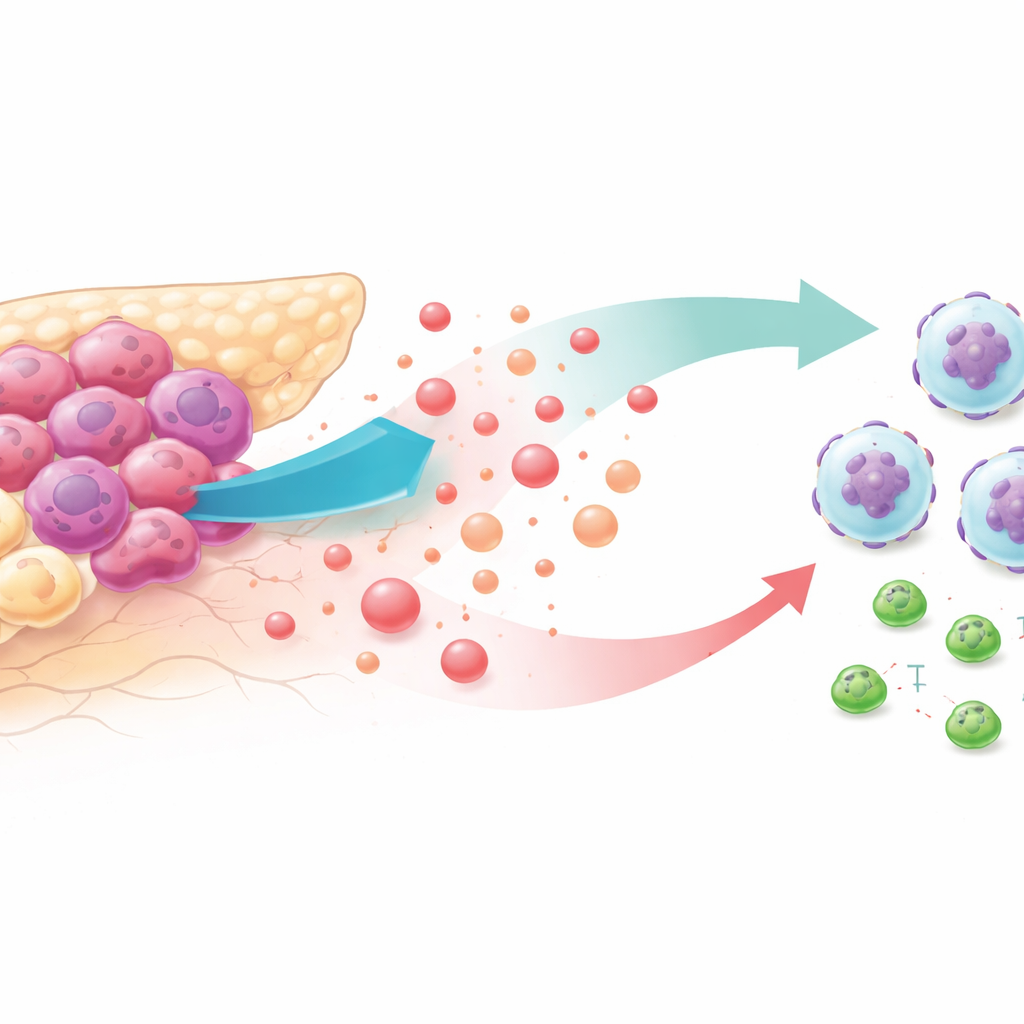
Głodne cukru guzy i wrogie otoczenie
Komórki nowotworowe są znane z intensywnego spalania glukozy, nawet gdy tlenu jest pod dostatkiem. Ten „wysoki poziom glikolizy” zalewa okolice guza laktem, produktem ubocznym niegdyś uważanym za metaboliczne odpady. Analiza baz danych z próbkami pacjentów i modeli mysich wykazała, że nowotwory trzustki z najsilniejszą glikolizą były pełne neutrofili — białych krwinek, które w tym kontekście wspierają wzrost guza — i miały mniej cytotoksycznych limfocytów CD8. Pacjenci, których guzy wykazywały taki profil, zazwyczaj żyli krócej, co sugeruje ścisły związek między zmienionym metabolizmem a unikaniem odpowiedzi immunologicznej.
Jak guzy wykorzystują laktat do przywoływania niewłaściwej pomocy
Aby zrozumieć, jak glikoliza przyciąga neutrofile, zespół ograniczył glikolizę w liniach komórkowych raka trzustki i u myszy za pomocą leków lub sztucznych manipulacji genetycznych. Gdy rozkład cukru był zahamowany, komórki guza uwalniały znacznie mniej sygnału chemicznego zwanego CXCL1, a krążące poziomy tego sygnału spadły u myszy i w próbkach pacjentów. W testach migracji w laboratorium neutrofile chętnie przesuwały się w kierunku pożywki z komórek o silnej glikolizie, ale nie w kierunku pożywki z komórek z zahamowaną glikolizą — chyba że badacze dodali oczyszczony CXCL1. U żywych myszy przywrócenie CXCL1 w guzach z obniżoną glikolizą przywracało liczbę neutrofili i osłabiało przeciwguzowy efekt hamowania glikolizy.
Nowy przełącznik epigenetyczny napędzany laktem
Badanie zagłębiło się następnie na poziom pakowania DNA. Nasze geny są owinięte wokół białek typu histonów, których chemiczne oznaczenia działają jak przełączniki włączające lub wyłączające aktywność genów. Autorzy pokazują, że w raku trzustki laktat produkowany przez glikolizę dodaje specyficzną grupę „laktylową” do jednego miejsca w histonie, znanego jako H3K18. Ta modyfikacja, nazwana laktylacją histonu H3K18, była wyraźnie wyższa w tkankach nowotworowych niż w zdrowej trzustce. Gdy glikolizę zniesiono, laktylacja przy H3K18 malała, zwłaszcza w rejonie kontrolnym genu CXCL1, a produkcja CXCL1 spadała. Dodanie z powrotem laktatu przywracało zarówno znak na histonie, jak i ekspresję CXCL1. W próbkach pacjentów guzy z wyższą laktylacją H3K18 wykazywały również większe poziomy CXCL1, łącząc tę molekularną zmianę z proguzowym środowiskiem immunologicznym.
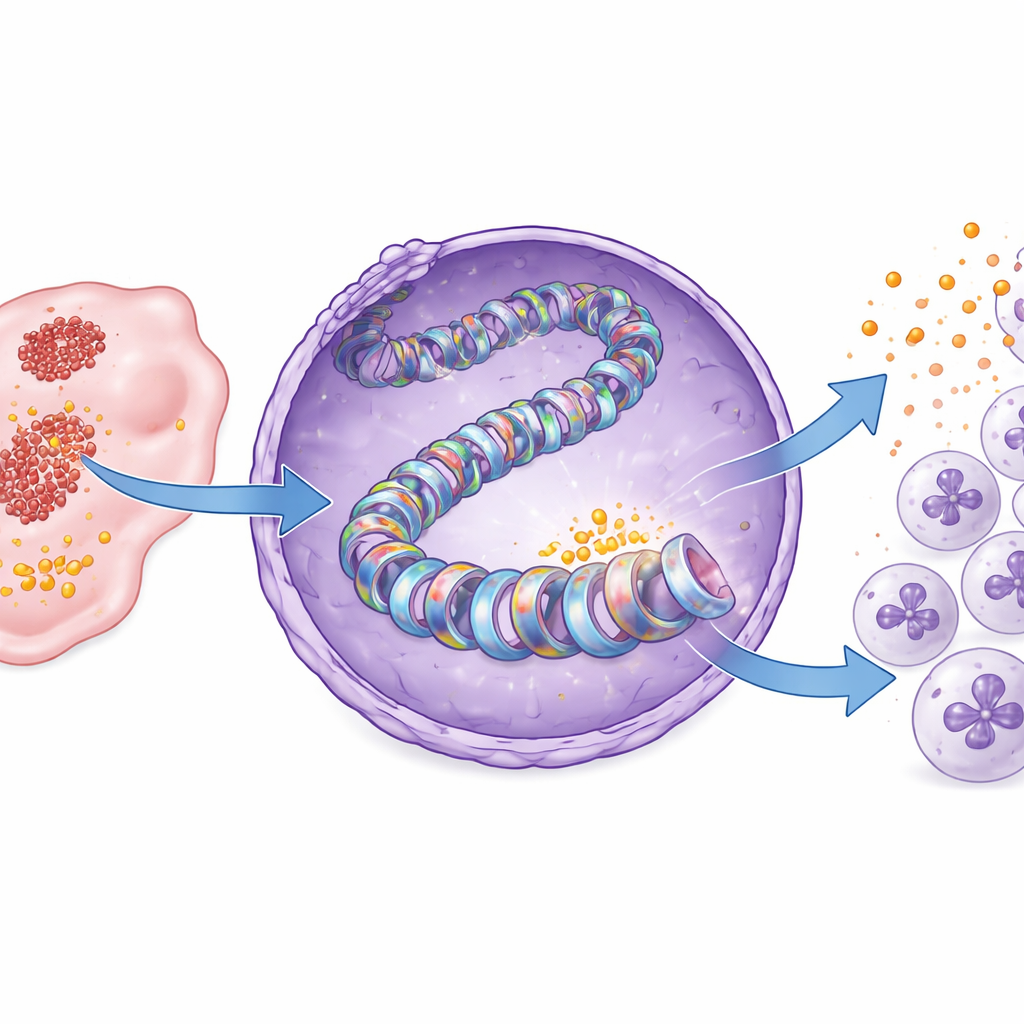
Identyfikacja enzymu i podatnego na leki punktu
Oznaczenia histonów są zapisywane przez wyspecjalizowane enzymy. Poprzez testowanie inhibitorów znanych białek modyfikujących histony badacze wskazali enzym zwany PCAF jako kluczowego „pisarza” znaku laktylacji H3K18 w raku trzustki. Modelowanie strukturalne sugerowało, że PCAF może wiązać laktyl-CoA, aktywowaną formę laktatu używaną do znakowania, a testy biochemiczne potwierdziły, że oczyszczony PCAF może bezpośrednio dodawać grupy laktylowe do histonu H3. Zablokowanie PCAF małą cząsteczką, bromosporiną, obniżało laktylację H3K18 i produkcję CXCL1 w komórkach nowotworowych i w guzach mysich. W rezultacie mniej neutrofili wnikało do guzów, więcej limfocytów CD8 się kumulowało, a wzrost guza spowalniał — bez wyraźnej utraty masy ciała czy toksyczności u myszy.
Zmiana „zimnego” guza w gorętszy przez terapię skojarzoną
Ponieważ standardowe leki blokujące punkty kontrolne immunologiczne, takie jak przeciwciała przeciw PD-1, dają ograniczone efekty w raku trzustki, zespół sprawdził, czy rozmontowanie szlaku laktat–PCAF–CXCL1 może zwiększyć wrażliwość tych guzów. Zarówno w podskórnych, jak i ortotopowych modelach mysich bromosporina w połączeniu z terapią przeciw PD-1 zmniejszała guzy bardziej niż każdy z tych zabiegów osobno, ograniczała naciek neutrofili, zwiększała aktywne komórki CD8 i istotnie wydłużała przeżycie. To sugeruje, że stłumienie metabolicznego „sygnału alarmowego” guza przywołującego neutrofile pomaga przekształcić immunologicznie „zimny” guz w „gorętszy”, z którym terapia blokująca punkty kontrolne może lepiej współdziałać.
Co to oznacza dla przyszłego leczenia
Mówiąc prosto, badanie ujawnia łańcuch zdarzeń: guzy trzustki spalają cukier, wydzielają laktat, wykorzystują ten laktat do przełączenia epigenetycznego na białkach pakujących DNA, zwiększają CXCL1 i w ten sposób przyciągają neutrofile, które pomagają im ukryć się przed komórkami zabójczymi T. Przerwanie tego łańcucha na etapie PCAF za pomocą leku nie tylko spowalnia guzy, lecz także zwiększa skuteczność istniejącej immunoterapii u myszy. Choć potrzebne są dalsze prace nad bezpieczeństwem i optymalnym sposobem celowania w ten szlak u ludzi, wyniki te wskazują obiecującą strategię: przeprogramować metabolizm guza i przełączniki genowe, aby dać układowi odpornościowemu uczciwsze szanse w walce.
Cytowanie: Zhang, P., Ma, J., Wan, Y. et al. Histone lactylation increases CXCL1 expression for neutrophil infiltration and immune escape in pancreatic cancer. Nat Commun 17, 2526 (2026). https://doi.org/10.1038/s41467-026-69311-5
Słowa kluczowe: rak trzustki, metabolizm guza, laktylacja histonów, mikrośrodowisko guza, immunoterapia przeciwnowotworowa