Clear Sky Science · pl
Wykorzystanie przewidywalnej kinetyki wiązania w DNA-PAINT do odszumiania obrazów o nadrozmiarowej rozdzielczości
Bardziej ostre spojrzenia w mikroskopijny świat
Nowoczesne mikroskopy potrafią „zobaczyć” pojedyncze cząsteczki wewnątrz komórek, ale te obrazy często są usiane myląco wyglądającymi punktami tła. W tym badaniu przedstawiono sposób oczyszczania takich obrazów, wykorzystujący naturalne zachowanie fragmentów DNA — ich przyłączanie się i odłączanie w czasie. Efektem są wyraźniejsze obrazy maszynerii molekularnej wewnątrz komórek, co ma znaczenie zarówno dla biologii podstawowej, jak i odkrywania leków.
Jak sztuczka z migotaniem ujawnia ukryte detale
Jedna z potężnych metod obrazowania, zwana DNA-PAINT, zamienia losowe przyłączanie krótkich nici DNA w mikroskop o nadrozdzielczości. Jedna nić DNA jest przyłączona do białka, które chcemy zobaczyć; dopasowana nić z barwnikiem fluorescencyjnym krąży w roztworze. Gdy unosząca się nić chwilowo wiąże się ze swoim partnerem, pojawia się krótki błysk światła. Rejestrując wiele takich mignięć i lokalizując je z dużą precyzją, badacze mogą odtworzyć położenie białek z dokładnością rzędu nanometrów — znacznie lepszą niż w konwencjonalnej mikroskopii świetlnej.
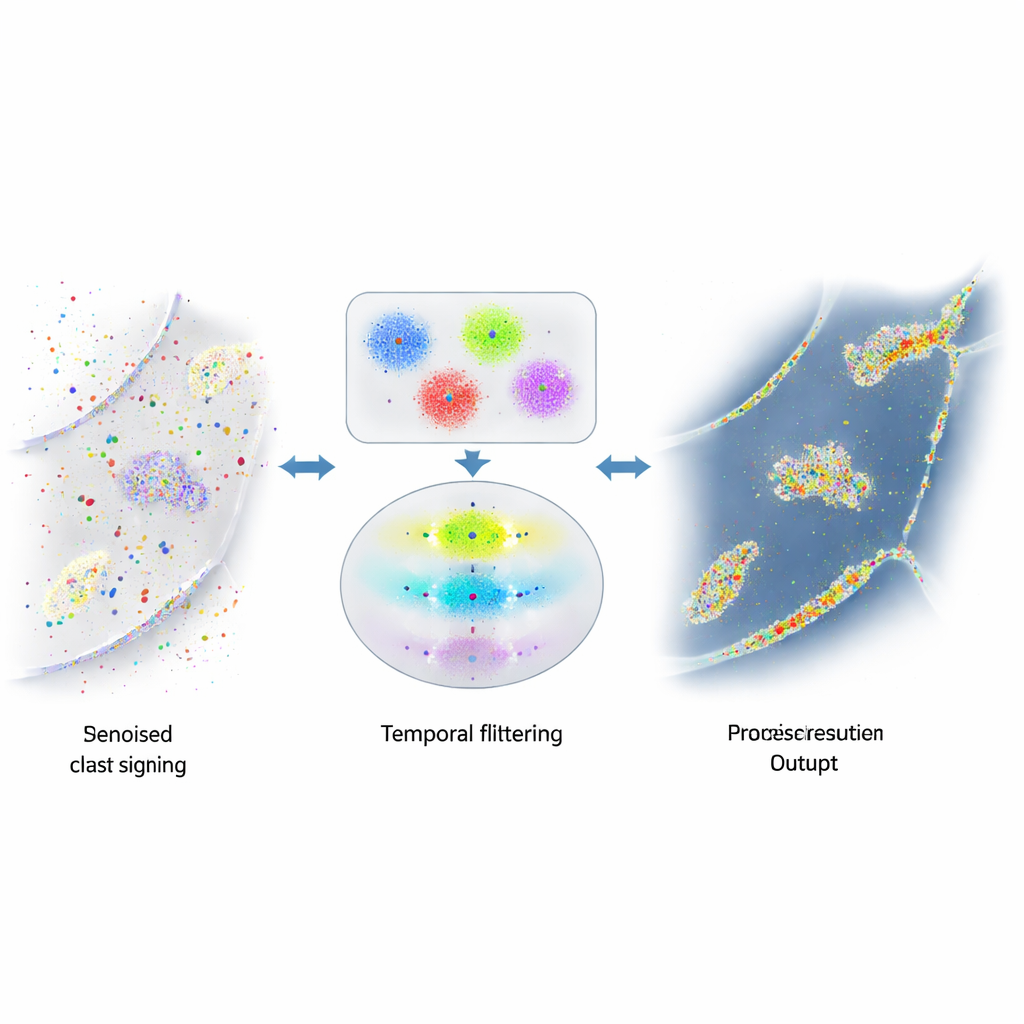
Kiedy użyteczne sygnały toną w hałasie
Siłą DNA-PAINT — duża liczba swobodnie poruszających się fluorescencyjnych nici — jest jednocześnie problemem. Te nici od czasu do czasu przyczepiają się tam, gdzie nie powinny, na przykład do losowych powierzchni komórkowych albo do obfitego DNA w jądrze. Te przypadkowe błyski są nierozróżnialne wizualnie od prawdziwych i zagracają końcowy obraz fałszywymi punktami i skupiskami. Wcześniejsze próby zmniejszenia tego szumu koncentrowały się na modyfikacji chemii, by rzadziej występowały niepożądane przyczepienia, lub na prostych zasadach wykrywających ewidentne odstępstwa. Jednak znaczna część mylącego sygnału pozostawała, ograniczając wiarygodność pomiarów liczby białek czy relacji przestrzennych.
Wykorzystanie czasu do rozróżnienia prawdy od fałszu
Autorzy zauważyli, że prawdziwe pary DNA w DNA-PAINT podlegają prostej regule czasowej: przerwy między autentycznymi zdarzeniami wiązania podążają za przewidywalnym, wykładniczym rozkładem. Natomiast przypadkowe zdarzenia przyczepiania się nie. Opracowali wieloetapowy algorytm, który najpierw grupuje bliskie sobie mignięcia w małe skupiska na podstawie ich położenia, używając kombinacji klastrowania opartego na gęstości i k‑means, aby rozbić złożone kształty na jednostki o wielkości lokalizacji. Dla każdego skupiska konstruują następnie „ślad czasowy” zdarzeń wiązania, starannie łącząc szybkie włączania i wyłączania z tego samego wiązania w pojedyncze zdarzenia. Na koniec stosują test statystyczny, aby sprawdzić, czy przerwy między zdarzeniami w danym skupisku odpowiadają oczekiwanemu wykładniczemu zachowaniu. Skupiska, które zdadzą test, traktowane są jako prawdziwe; te, które nie przejdą, są odrzucane jako szum.
Sprawdzenie metody w prawdziwych komórkach
Aby przetestować swoje podejście, zespół obrazował białko adhezji komórkowej E‑kadherynę w komorach jajowych muszki owocowej, gdzie niektóre komórki produkowały znakowane białko, a komórki sąsiednie nie. To stworzyło przyległe obszary bogate w autentyczny sygnał i obszary, które powinny zawierać tylko tło. Poprzez dostrojenie minimalnej liczby zdarzeń wiązania, które skupisko musi wykazać przed testem, znaleźli ustawienia usuwające ponad 90% fałszywych skupisk przy zachowaniu ponad 98% prawdziwych na brzegach komórek. W obrazach po odszumianiu drobne struktury, takie jak cienkie rury i pęcherzyki, stały się znacznie wyraźniejsze. Ta sama strategia zadziałała w innych systemach, w tym w mitochondriach i mikrotubulach, a nawet dla białek o bardziej rozmytym, amorficznym rozkładzie, gdzie sama informacja przestrzenna nie wskazuje, co jest prawdziwe.
Wyraźniejsze mapy molekularne dla przyszłych badań
Słuchając „rytmu” wiązania DNA zamiast tylko patrzeć, gdzie pojawiają się mignięcia, ta metoda niezawodnie usuwa mylące tło z danych DNA-PAINT. Dla niespecjalistów kluczowy wynik jest prosty: ostrzejsze, bardziej wiarygodne mapy molekularne wewnątrz komórek. Ułatwia to bezpieczniejsze zliczanie liczby cząsteczek białek, ocenę bliskości między różnymi białkami oraz budowanie dokładniejszych obrazów wewnętrznego życia komórek. W miarę jak obrazowanie oparte na DNA będzie się rozwijać, takie inteligentne odszumianie będzie niezbędne do przekształcania surowych, nakropkowanych obrazów w solidne biologiczne wnioski.
Cytowanie: Sirinakis, G., Allgeyer, E.S., Richens, J.H. et al. Utilizing the predictable binding kinetics of DNA-PAINT to denoise super-resolution images. Nat Commun 17, 2397 (2026). https://doi.org/10.1038/s41467-026-69304-4
Słowa kluczowe: DNA-PAINT, mikroskopia o nadrozdzielczości, odszumianie obrazów, obrazowanie pojedynczych cząsteczek, mapowanie białek