Clear Sky Science · pl
Aktywacja STING wywołuje odpowiedzi cytotoksyczne i immunologiczne w oponiakach przez patologiczne drogi śmierci komórkowej
Włączając alarmy organizmu przeciwko nowotworom mózgu
Oponiaki należą do najczęstszych guzów mózgu; mimo że operacja i radioterapia często pomagają, niektóre guzy nawracają. Te oporne nowotwory mogą powodować napady, bóle głowy i upośledzenie funkcji, a brak powszechnie zaakceptowanych leków pozostaje problemem. W niniejszym badaniu autorzy badają sposób, by sprawić, iż same komórki guza i pobliskie komórki odpornościowe uruchomią silny wewnętrzny alarm, wykorzystując molekułę aktywującą wrodzony system wykrywania zagrożeń o nazwie STING. Celem jest nie tylko bezpośrednie zabicie komórek nowotworowych, lecz także pobudzenie układu odpornościowego i rozluźnienie twardej, podporowej matrycy guza.
Guz ukryty w cichym, immunologicznym sąsiedztwie
Autorzy najpierw odwzorowali komórkowe „sąsiedztwo” w ludzkich oponiakach, stosując sekwencjonowanie pojedynczych komórek i obrazowanie przestrzenne. Stwierdzili, że guzy te są wypełnione komórkami odporności wrodzonej, zwłaszcza makrofagami, podczas gdy klasyczne komórki przeciwnowotworowe — limfocyty T i komórki NK — są nieliczne i często wyczerpane. Otaczające komórki nowotworowe jest gęsta powłoka kolagenu i innych białek macierzy, tworząca opancerzoną, warstwową strukturę. Wiele makrofagów w tych rejonach nosi receptory hamujące, aktywowane przez kolagen, co tworzy silnie stłumione środowisko, w którym komórki odpornościowe są obecne, lecz powstrzymywane zamiast uwolnione przeciwko nowotworowi.
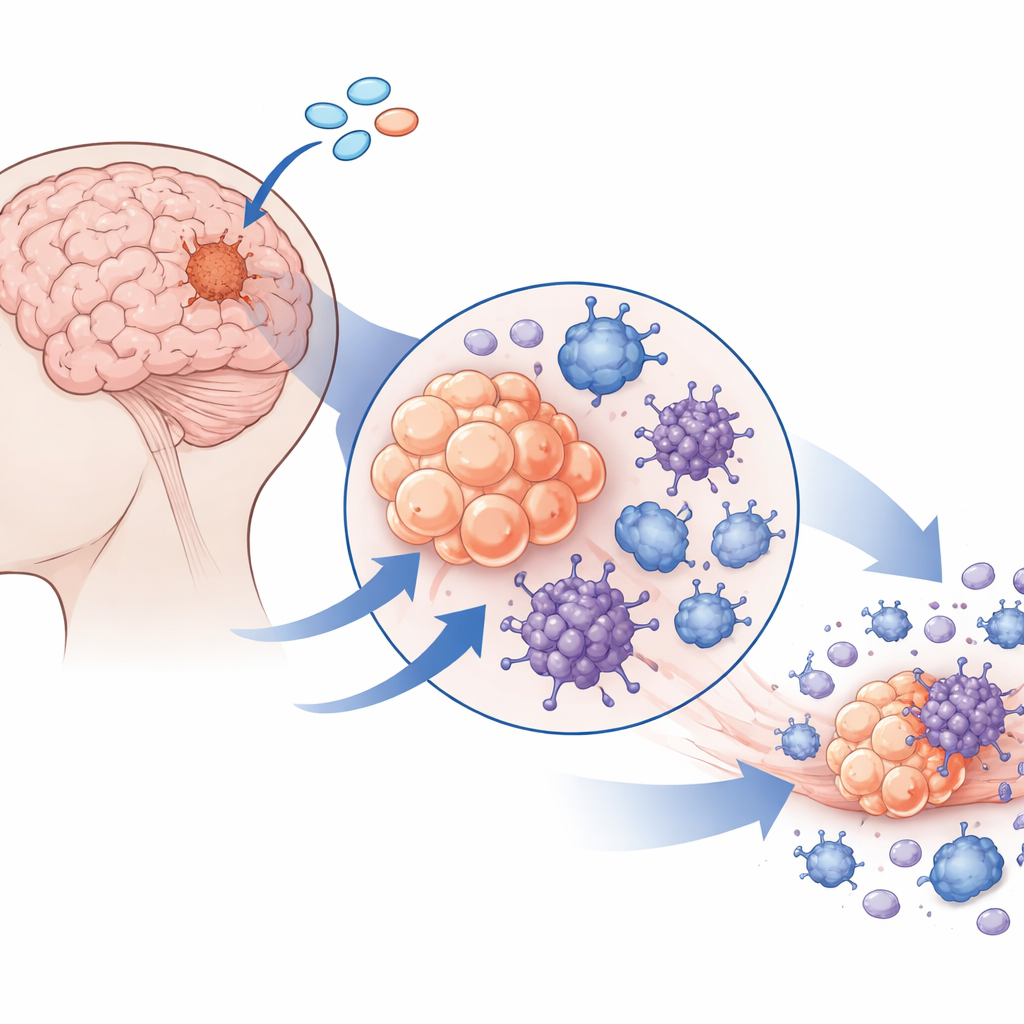
Odnalezienie przełącznika, który komórki guza wciąż zachowują
Następnie zespół poszukiwał szlaków, które mogłyby przełączyć to stłumione środowisko w stan zapalny nieprzyjazny dla guza. Skoncentrowano się na STING — sensorze reagującym na nieoczekiwane DNA w komórkach i wywołującym odpowiedzi przeciwwirusowe oraz zapalne. W przeciwieństwie do wielu innych guzów mózgu, komórki oponiaka wykazywały nadzwyczaj wysokie poziomy STING. Wyjaśniono to otwartą chromatyną i niskim poziomem metylacji DNA przy genie STING, co oznacza, że gen jest epigenetycznie przygotowany do aktywności. STING był obfity nie tylko w komórkach guza, lecz także w komórkach naczyń krwionośnych i makrofagach pobliskich tkanek, co sugeruje, że pojedynczy lek mógłby jednocześnie oddziaływać na wiele kluczowych składników mikrośrodowiska guza.
Wymuszanie płomiennej autodestrukcji komórek guza
Naukowcy potraktowali świeżo wycięte próbki oponiaków od pacjentów silnym agonistą STING o nazwie 8803. Nawet po usunięciu komórek odpornościowych komórki guza obumierały, co dowodzi bezpośredniego działania. Poprzez dodanie leków selektywnie blokujących różne drogi śmierci komórkowej oraz analizę aktywności genów wykazano, że 8803 nie powodował jedynie cichej apoptozy. Zamiast tego popychał komórki oponiaka do kilku zapalnych form śmierci — piroptozy, nekroptozy i ferroptozy — które powodują pękanie komórek, zamiast ich uporządkowanego rozkładu. Kluczowym krokiem była aktywacja i cięcie białka zwanego gasderminą D, które tworzy pory w błonie komórkowej. Mikroskopia elektronowa ujawniła komórki guza przepełnione dziurami w błonie i uszkodzonymi mitochondriami, a blokada reaktywnych form tlenu zmniejszała śmiertelność, łącząc stres mitochondrialny z tą „płomienną” śmiercią.
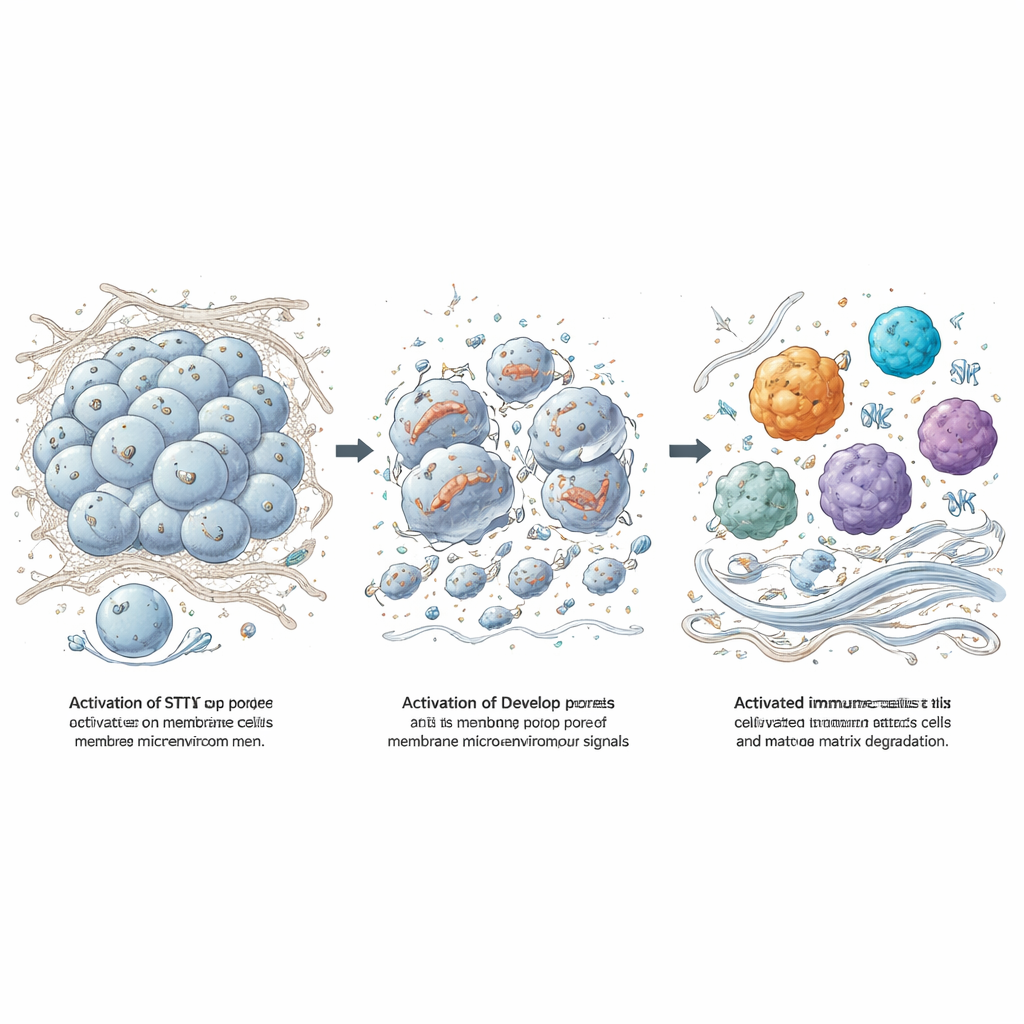
Od szczątków guza do pobudzenia odporności i erozji macierzy
Kiedy komórki guza umierają w tak dramatyczny sposób, uwalniają cząsteczki „zagrożenia”, które mogą pobudzić komórki odpornościowe. Zespół wystawił mysie makrofagi na lizaty komórek oponiaka i zaobserwował wzrost czynników zapalnych oraz enzymów rozkładających kolagen, zwłaszcza metaloproteinazy macierzy-3 (MMP-3). Pracując na myszach pozbawionych konkretnych adaptorów sygnałowych, wykazano, że receptory toll-podobne, inny system wykrywania zagrożeń, są kluczowe dla tej odpowiedzi, podczas gdy aktywacja STING przez 8803 dodaje własną warstwę stymulacji immunologicznej. W modelach mysich oponiaków bezpośrednie wstrzyknięcie 8803 do guzów zmniejszało lub stabilizowało wzrost, wydłużało przeżycie i przekształcało miejsce guza z cichej, bogatej w kolagen masy w obszar wypełniony aktywnymi makrofagami, komórkami NK, limfocytami T oraz z wyraźnie zmniejszonym barwieniem kolagenu.
Dlaczego to podejście może zmienić leczenie pacjentów
Podsumowując, badanie pokazuje, że oponiaki mają wbudowaną słabość: komórki guza zachowują dostępny „przełącznik” STING, który po aktywacji przez 8803 popycha je do eksplodującej, zapalnej śmierci. Proces ten zarówno zabija komórki nowotworowe, jak i zalewa obszar sygnałami alarmowymi, które rekrutują i pobudzają komórki odpornościowe, a także przyczynia się do rozkładu kolagenowej rusztowania nasilającego efekt masy. Ponieważ oponiaki zazwyczaj są zlokalizowane, a nie szeroko przerzutujące, oraz że standardowe opcje są ograniczone przy nawrotowym przebiegu, miejscowo podawany agonista STING, taki jak 8803, może dostarczyć nowego, ukierunkowanego podejścia do zmniejszenia objętości guza i przekształcenia jego mikrośrodowiska immunologicznego w kierunku trwalszej kontroli.
Cytowanie: Youngblood, M.W., Tripathi, S., Najem, H. et al. STING activation induces cytotoxic and immune responses in meningiomas via inflammatory cell death pathways. Nat Commun 17, 2685 (2026). https://doi.org/10.1038/s41467-026-69296-1
Słowa kluczowe: oponiak, szlak STING, immunoterapia guzów mózgu, zapalna śmierć komórek, mikrośrodowisko guza