Clear Sky Science · pl
Genetyczny czynnik ostrej nekrotycznej encefalopatii, RANBP2, reguluje odpowiedź zapalną na zakażenie wirusem grypy A
Kiedy grypa uszkadza mózg
Większość osób myśli o grypie jako o tygodniu gorączki, kaszlu i leżenia w łóżku. Jednak w rzadkich przypadkach, szczególnie u dzieci, zwykłe zakażenie grypą może nagle przekształcić się w zagrażające życiu zaburzenie mózgu zwane ostrą nekrotyczną encefalopatią (ANE). Rodziny i lekarze od dawna podejrzewali, że geny mogą wpływać na to, kto rozwija to katastrofalne powikłanie. W tym badaniu wyjaśniono, jak pojedynczy komórkowy strażnik — białko RANBP2 — zwykle powstrzymuje wirusa grypy i zapobiega wymykaniu się spod kontroli własnej odpowiedzi zapalnej organizmu.
Rzadkie, ale wyniszczające powikłanie grypy
ANE pojawia się nagle po gorączkowej chorobie, często grypie, i może szybko doprowadzić do drgawek, śpiączki i trwałych uszkodzeń neurologicznych. Około połowa znanych epizodów ANE na świecie jest powiązana z wirusem grypy A, szczególnie szczepem H1N1. Dzieci, które odziedziczą pewne zmiany w genie RANBP2, mają znacznie wyższe ryzyko — stan ten znany jest jako ANE1. Do tej pory naukowcy nie rozumieli jednak, co to białko robi podczas zakażenia grypą ani dlaczego jego zmiana powodowałaby tak nasilone zapalenie w mózgu.
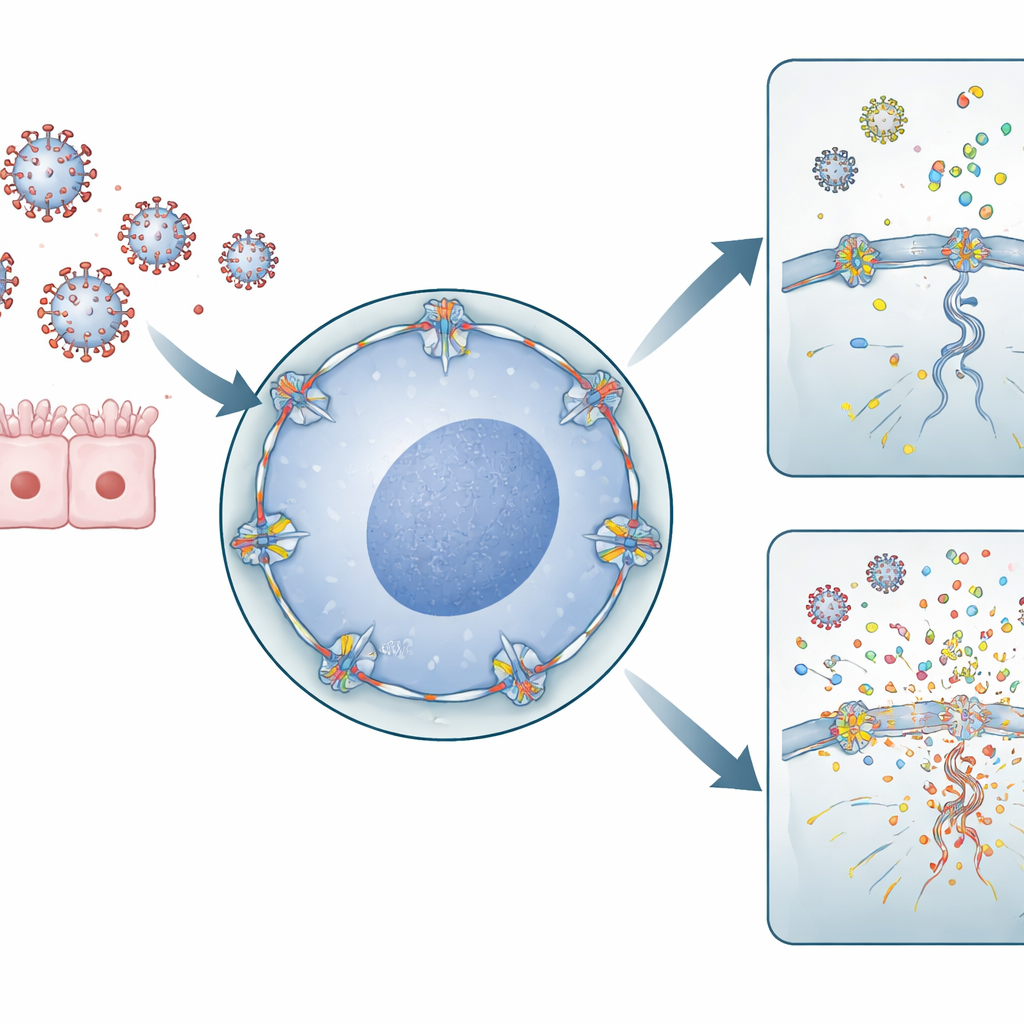
Komórkowe wrota i wirusowe genomy
Wirus grypy A ma nietypowy tryb życia jak na wirusa RNA: musi wejść do jądra komórkowego, aby skopiować swój materiał genetyczny. Robi to, przechodząc przez pory jądrowe — duże bramy w otoczce jądrowej, które regulują ruch między jądrem a otaczającą cytoplazmą. RANBP2 jest głównym składnikiem po zewnętrznej stronie tych porów. Autorzy wykorzystali komórki pochodzenia płucnego i komórki układu odpornościowego, aby obniżyć poziomy RANBP2 lub wprowadzić mutację związaną z ANE. Stwierdzili, że gdy RANBP2 był nieobecny lub źle zlokalizowany, genomy grypy były intensywniej kopiowane w jądrze, a segmenty wirusowego materiału genetycznego eksportowano do cytoplazmy w niezrównoważony sposób. Co zaskakujące, taki nadmiar wirusowego RNA nie skutkował większą liczbą zakaźnych cząstek wirusa, ale zmieniał miejsce i sposób gromadzenia się materiału wirusowego w komórce.
Kiedy wirusowe szczątki wzmagają system alarmowy
Układ odpornościowy polega na czujnikach molekularnych, które wykrywają porozrzucane fragmenty wirusowego RNA w cytoplazmie jako sygnały niebezpieczeństwa. Zespół wykazał, że w komórkach pozbawionych prawidłowego RANBP2 dodatkowe segmenty wirusowego RNA gromadziły się w cytoplazmie, tworząc dokładnie takie wzorce, na które te czujniki są wyczulone. W komórkach pochodzenia płucnego wywołało to wyższe poziomy cząsteczek zapalnych, takich jak IL‑6 i IL‑1β. W pierwotnych ludzkich makrofagach — komórkach odpornościowych pierwszej linii pobranych od dawców krwi — utrata RANBP2 prowadziła do uderzeniowego wzrostu prozapalnych chemokin, w tym CXCL8, CXCL10, CCL2, CCL3 i CCL4. Te chemiczne przekaźniki rekrutują i aktywują kolejne komórki odpornościowe, wzmacniając ogólną reakcję na zakażenie.
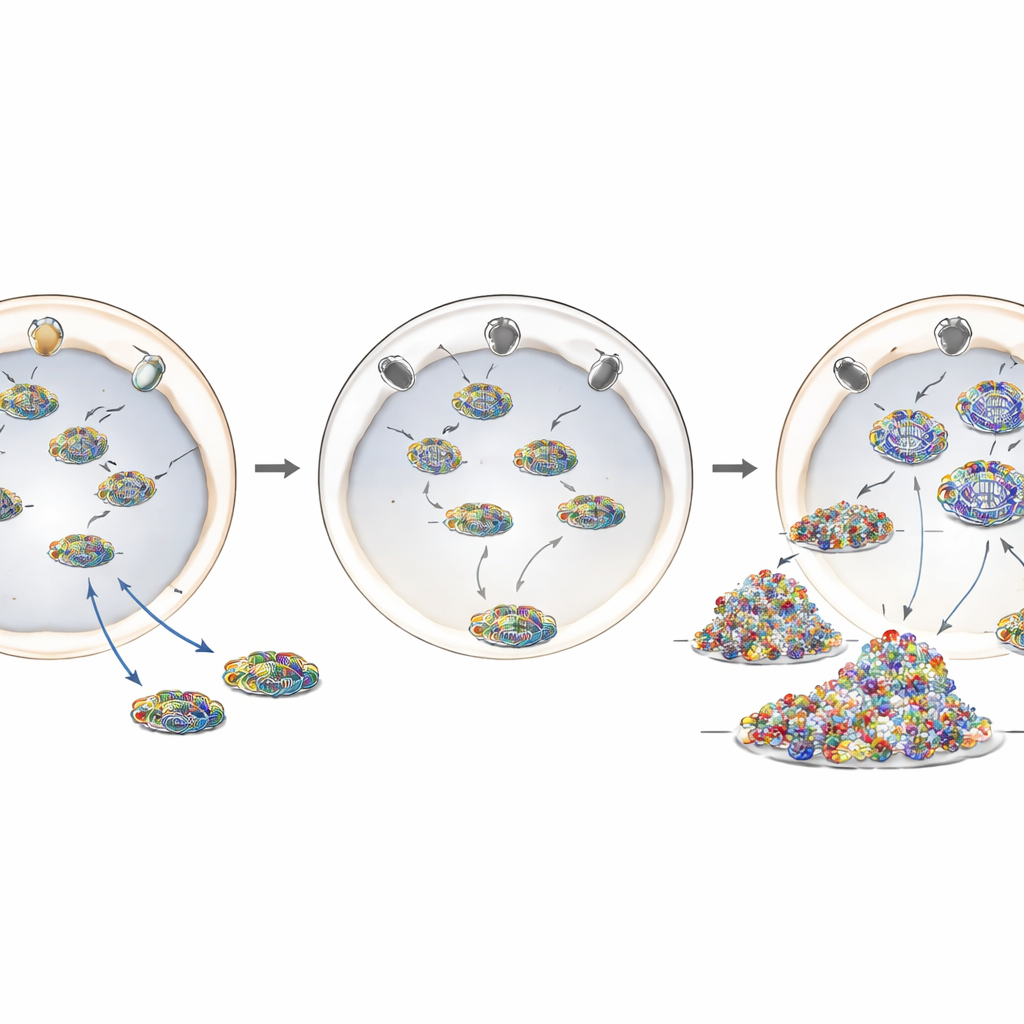
Mutacja chorobowa, która przemieszcza strażnika
Aby wierniej odwzorować ANE1, badacze użyli edycji genomu CRISPR‑Cas9, aby wprowadzić najczęściej występującą zmianę związaną z chorobą, T585M, do ludzkiego genu RANBP2. W tych zmodyfikowanych komórkach poziomy białka RANBP2 były w dużej mierze normalne, ale jego lokalizacja nie: zamiast tworzyć jasny obwód wokół otoczki jądrowej, znaczna część białka była przesunięta do wnętrza komórki. Komórki noszące tę mutację, niezależnie od tego, czy w jednej czy obu kopiach genu, zachowywały się podobnie do komórek z niedoborem RANBP2. Wspierały zwiększoną replikację genomu grypy, wykazywały więcej materiału wirusowego w cytoplazmie i po zakażeniu uruchamiały silniejszą odpowiedź zapalną. Wskazuje to, że prawidłowe umiejscowienie RANBP2 przy porach jądrowych — a nie jego całkowita obfitość — jest kluczowe dla jego ochronnej roli.
Dlaczego to ma znaczenie dla dzieci zagrożonych chorobą
Podsumowując, wyniki przedstawiają RANBP2 jako komórkowego strażnika, który precyzyjnie reguluje, jak materiał genetyczny grypy wchodzi do jądra i z niego wychodzi. Gdy RANBP2 jest nieobecny lub źle zlokalizowany, wirusowe RNA jest nadmiernie replikowane i eksportowane w chaotyczny sposób, zanieczyszczając cytoplazmę szczątkami molekularnymi, które znacznie nasilają sygnalizację immunologiczną. Dla większości tkanek może to oznaczać surowszy, ale do przetrwania epizod grypy. U podatnych dzieci z ANE1 taka niekontrolowana reakcja zapalna — zwłaszcza jeśli dotrze do mózgu — może pomóc wyjaśnić nagłe, ciężkie uszkodzenia neurologiczne obserwowane po pozornie zwykłych zakażeniach. Zrozumienie tej ścieżki może ukierunkować przyszłe strategie wczesnego identyfikowania pacjentów z ryzykiem oraz dostosowywania leczenia przeciwzapalnego, zanim odpowiedź immunologiczna zmieni się z ochronnej w destrukcyjną.
Cytowanie: Desgraupes, S., Decorsière, A., Perrin, S. et al. The genetic driver of Acute Necrotizing Encephalopathy, RANBP2, regulates the inflammatory response to Influenza A virus infection. Nat Commun 17, 2427 (2026). https://doi.org/10.1038/s41467-026-69288-1
Słowa kluczowe: grypa, ostra nekrotyczna encefalopatia, RANBP2, hiperodczyn zapalny, por jądrowy