Clear Sky Science · pl
Klasa MHC II działa jako receptor wejścia specyficzny dla gospodarza dla reprezentatywnych ludzkich i świńskich wirusów grypy A H3N2
Dlaczego to badanie nad grypą ma znaczenie
Sezonowa grypa wydaje się znajoma, ale wirus ją wywołujący nieustannie poszukuje nowych sposobów na zakażanie naszych komórek i przeskakiwanie między gatunkami. To badanie pokazuje, że powszechny szczep grypy H3N2 może wykorzystywać nie tylko klasyczne „drzwi” do komórek, lecz także drugi, zaskakujący szlak wejścia, który różni się między ludźmi a świniami. Zrozumienie tej zapasowej drogi wnikania pomaga wyjaśnić, jak grypa przystosowuje się do nowych gospodarzy i może poprawić monitorowanie oraz przygotowanie na szczepy o potencjale pandemicznym. 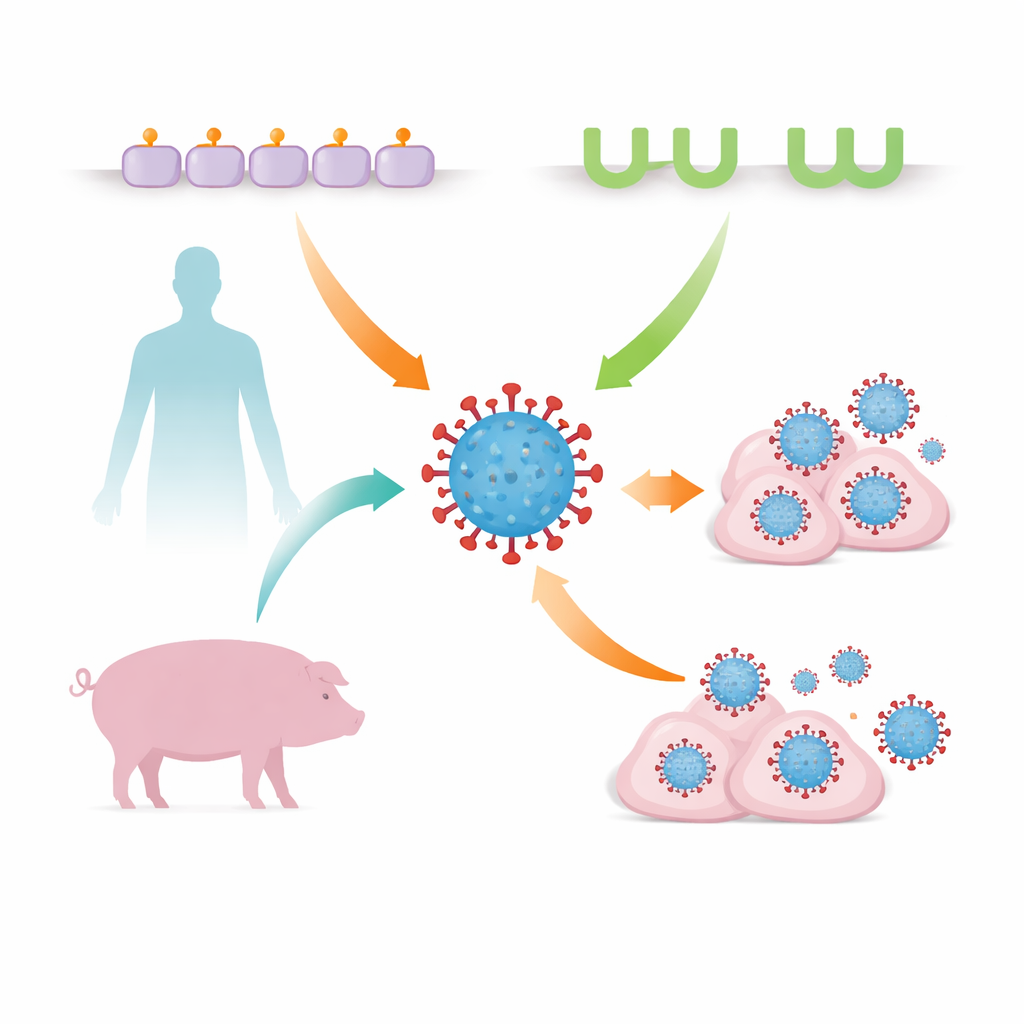
Standardowy sposób, w jaki grypa wnika
Przez dziesięciolecia naukowcy wiedzieli, że wirusy grypy A zwykle wchodzą do komórek, przyczepiając się do cząsteczek cukru zwanych kwasami sialowymi, które pokrywają powierzchnię komórki. „Hak” wirusa, białko hemaglutynina, rozpoznaje określone kształty i połączenia tych cukrów, które różnią się między ptakami, ludźmi i innymi zwierzętami. Małe zmiany w hemaglutyninie mogą przesunąć preferencje cukrowe, pomagając wirusowi ptasiemu przystosować się do ssaków. Ostatnio jednak odkryto nietypowe wirusy grypy z nietoperzy i kaczek, które całkowicie ignorują kwasy sialowe i zamiast nich używają białka zwanego klasą MHC II jako wejścia, co sugeruje, że nasze rozumienie wnikania grypy było niepełne.
Pojawiają się drugie „drzwi”
Nowa praca pokazuje, że bardziej znane wirusy H3N2 również mogą wykorzystywać klasę MHC II jako alternatywną drogę wejścia, obok kwasów sialowych. MHC II normalnie pomaga komórkom układu odpornościowego prezentować fragmenty patogenów, by zaalarmować system odpornościowy. Zespół skupił się na dwóch blisko spokrewnionych wirusach zbudowanych na tym samym szkielecie genetycznym: jednym przypominającym ludzki sezonowy szczep H3N2 (hVIC/11) i drugim zaadaptowanym do świń (sOH/04). W płucach świń wirus zaadaptowany do świń był stwierdzany w ścisłym powiązaniu z komórkami bogatymi w świńską MHC II, zwłaszcza z makrofagami pęcherzykowymi — komórkami odpornościowymi frontu w pęcherzykach płucnych — sugerując, że ta cząsteczka może działać jako „uchwyt”, który wirus może chwycić.
Wyłączenie jednych drzwi, by sprawdzić drugie
Aby sprawdzić, czy MHC II rzeczywiście działa jako niezależny receptor wejścia, badacze chemicznie usunęli kwasy sialowe z makrofagów świń i z genetycznie zmodyfikowanych ludzkich linii komórkowych. Gdy usunięto tylko klasyczne cukry, oba wirusy nadal wywoływały pewne zakażenie. Jednak gdy kwasy sialowe usunięto i jednocześnie zablokowano MHC II przeciwciałami, zakażenie znacząco spadło, szczególnie dla wirusa zaadaptowanego do świń. W ludzkich komórkach nerkowych i płucnych, które genetycznie nie produkowały żadnych kwasów sialowych, dodanie ludzkiej wersji MHC II umożliwiło efektywne zakażenie przez wirus przypominający ludzki, natomiast dodanie świńskiej wersji sprzyjało wirusowi świńskiemu. Leczenie komórek lekami blokującymi zakwaszanie wewnętrznych pęcherzyków również hamowało to zakażenie zależne od MHC, co wskazuje, że po wejściu wirus podąża po tej samej wewnętrznej trasie co przy standardowym sposobie wnikania grypy. 
Jak drobne zmiany pomagają wirusowi zmieniać gospodarza
Następnie autorzy zapytali, które części hemaglutyniny wirusa kontrolują ten nowy typ wiązania. Wcześniejsze badania wykazały, że gdy ludzki wirus H3N2 przechodzi przez świnie, często nabywa pojedyncze zmiany literowe w pobliżu, lecz nie bezpośrednio w kieszeni wiążącej kwasy sialowe. Przetestowano wirusy niosące dowolną z trzech takich zmian (w pozycjach oznaczonych jako 138, 186 lub 193 w białku). Te zmutowane wirusy potrafiły wykorzystać zarówno ludzką, jak i świńską MHC II, aby wejść do komórek pozbawionych kwasów sialowych, a w niektórych testach nawet preferowały wersję świńską. Jednocześnie te same mutacje zmieniały siłę, z jaką wirusy wiązały się z kwasami sialowymi o charakterze ludzkim lub ptasim. Innymi słowy, modyfikacje w pobliżu zwykłego miejsca wiązania cukru mogą jednocześnie dostrajać zarówno klasyczny, jak i nowy receptor, dając wirusowi elastyczność w trakcie adaptacji do nowego gatunku.
Co to oznacza dla grypy i przyszłych zagrożeń
Łącznie wyniki pokazują, że powszechne wirusy grypy H3N2 nie są ograniczone do jednego typu „uchwytu” na powierzchni komórki: mogą wykorzystywać zarówno kwasy sialowe, jak i klasę MHC II, i robią to w sposób odzwierciedlający, czy wirus jest lepiej przystosowany do ludzi czy do świń. W trakcie wczesnej adaptacji do nowego gospodarza wirus może tymczasowo angażować MHC II z obu gatunków, poszerzając zakres celów i ułatwiając zadomowienie się. Ponieważ MHC II występuje obficie na kluczowych komórkach odpornościowych w płucach, ta alternatywna droga może pozwalać grypie selektywnie atakować komórki, które powinny nas bronić, co potencjalnie wspiera rozprzestrzenianie się wirusa i przebieg choroby. Uznanie MHC II jako receptora wejścia specyficznego dla gospodarza dodaje istotny element do obrazu, jak grypa przełamuje bariery gatunkowe, i podkreśla potrzebę monitorowania nie tylko wiązania cukrów, lecz także receptorów białkowych przy ocenie ryzyka pandemicznego nowych szczepów.
Cytowanie: Cardenas, M., Compton, S., Caceres, C.J. et al. MHC class II functions as a host-specific entry receptor for representative human and swine H3N2 influenza A viruses. Nat Commun 17, 2560 (2026). https://doi.org/10.1038/s41467-026-69267-6
Słowa kluczowe: grypa A H3N2, receptory wejścia wirusa, klasa MHC II, adaptacja do gospodarza, transmisja zoonotyczna