Clear Sky Science · pl
Trifunkcyjny flawoenzym katalizujący asymetryczną syntezę 4‑alkyl‑butenolidu w biosyntezie avenolidu
Dlaczego małe pierścienie w bakteriach mają dla nas znaczenie
Wiele ratujących życie leków, od środków przeciwpasożytniczych po środki ochrony roślin, opiera się na niewielkim motywie chemicznym zwanym butenolidem. Obecnie te pierścienie są w przeważającej mierze produkowane z surowców pochodzenia petrochemicznego w wieloetapowych procesach przemysłowych, które zużywają energię i generują odpady. W tym badaniu ujawniono, jak bakterie glebowe budują jeden z takich pierścieni — hormon zwany avenolidem, który uruchamia produkcję szeroko stosowanych środków przeciwpasożytniczych, awermektyn. Zrozumienie tej naturalnej ścieżki wskazuje drogę do czystszych, tańszych metod wytwarzania użytecznych związków i może pomóc w odkryciu nowych antybiotyków.
Szczególny pierścień w sercu wielu leków
Butenolidy to zwarte, pięcioczłonowe pierścienie, które chemikom się podobają, ponieważ reagują na wiele sposobów i występują w licznych produktach naturalnych oraz współczesnych lekach. Pomagają tworzyć cząsteczki o aktywności przeciwnowotworowej, przeciwgrzybiczej, przeciwzapalnej i owadobójczej, wykorzystywane w medycynie i rolnictwie. Tradycyjne drogi syntezy tych pierścieni zwykle wymagają kilku starannie kontrolowanych etapów, drogich katalizatorów i surowców petrochemicznych. Taka kombinacja podnosi koszty i wpływ na środowisko, skłaniając badaczy do poszukiwania biologicznych skrótów, które natura już udoskonaliła.
Bakteryjny hormon, który uruchamia produkcję przełomowego leku
W bakterii glebowej Streptomyces avermitilis związek zawierający butenolid, avenolid, działa jak drobny hormon. W bardzo niskich stężeniach wiąże się z białkiem regulatorowym i znosi molekularny hamulec na genach odpowiedzialnych za syntezę awermektyn — silnych środków paraliżujących robaki pasożytnicze i niektóre owady. Wcześniejsze badania genetyczne sugerowały, że dwa enzymy, nazwane SavA i SavB, budują avenolid, ale konkretne etapy były nieznane. Zespół przeniósł najpierw odpowiednie geny do bardziej uległego pokrewnego szczepu, Streptomyces albidoflavus, i zoptymalizował warunki hodowli, aż zmodyfikowany szczep wytworzył miligramowe ilości czystego avenolidu — wystarczające, by szczegółowo rozłożyć ścieżkę biochemiczną. 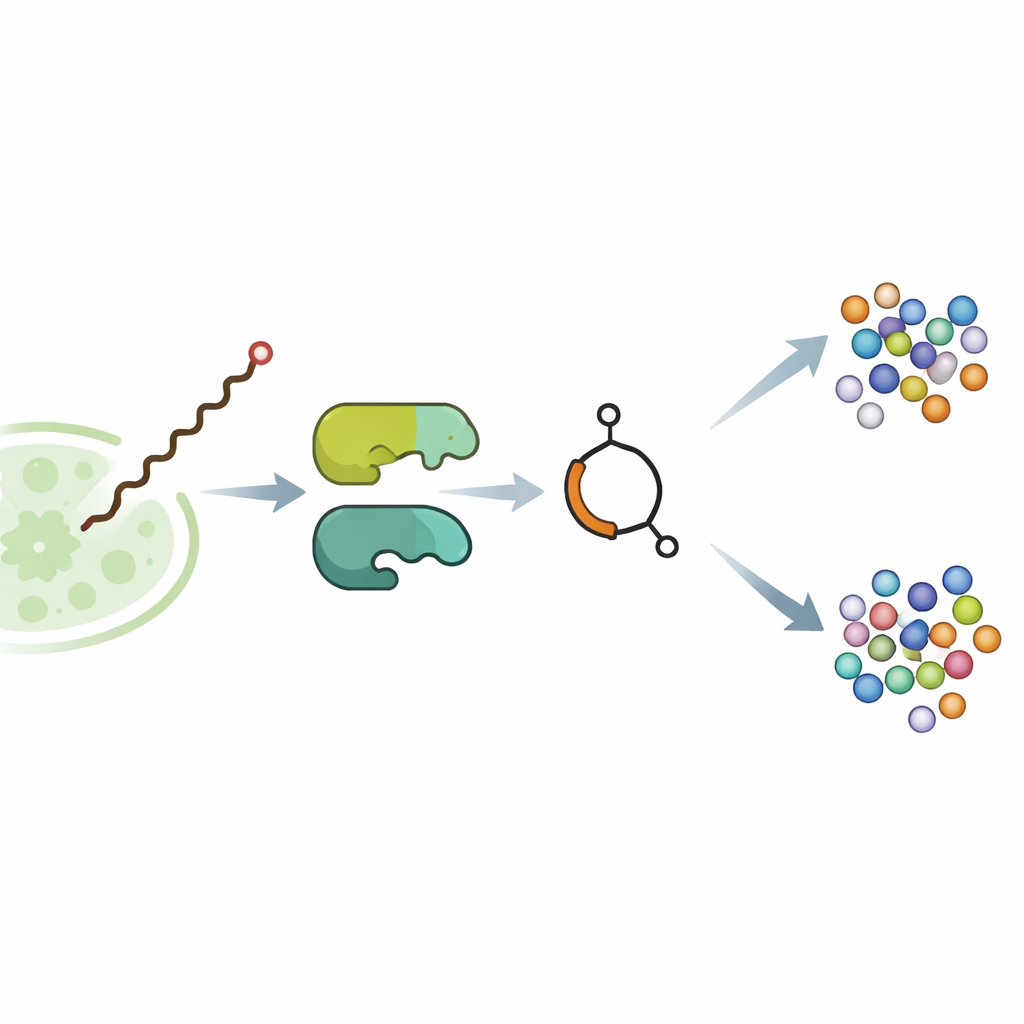
Pojedynczy enzym wykonujący trzy kolejne zadania
Główną niespodzianką badania jest SavA, enzym zawierający flawinę, który przeprowadza trzy odrębne przekształcenia chemiczne na fragmencie przypominającym kwas tłuszczowy pochodzącym z normalnego metabolizmu komórki. Pracując w reakcjach probówkowych z precyzyjnie syntezowanymi substratami‑imitacjami, badacze wykazali, że SavA najpierw usuwa atomy wodoru, wprowadzając podwójne wiązanie, potem dodaje grupę zawierającą tlen w określonej pozycji, a na końcu sprzyja zamknięciu łańcucha w pierścień butenolidowy. Doświadczenia z izotopami wykorzystujące tlen atomowy wzbogacony w cięższą odmianę potwierdziły, że tlen pierścienia pochodzi bezpośrednio z powietrza. Modele strukturalne i ukierunkowane mutacje wskazały pojedynczy aminokwas jako zasadę inicjującą reakcję oraz ujawniły, jak związany kofaktor flawinowy cykluje między postaciami zredukowanymi i utlenionymi, nie będąc przy tym zużywanym.
Enzym wykończeniowy dopracowujący łańcuch boczny
Gdy SavA zbuduje chiralną podstawę butenolidu, SavB — enzym cytochromu P450 — przejmuje dalsze prace nad ozdobieniem przyległego łańcucha węglowego. W obecności swoich partnerów redoks i powszechnego kofaktora komórkowego SavB przeprowadza precyzyjną serię utlenień na dwóch sąsiadujących atomach węgla. Analiza czasowa ujawniła dwa pośrednie związki: najpierw produkt z pojedynczą grupą hydroksylową, potem formę ketonową, zanim pojawi się w pełni funkcjonalny avenolid. Pomiary metodą rezonansu magnetycznego jądrowego potwierdziły pozycje i trójwymiarowe ułożenie wprowadzonych grup. Praca pokazuje, że SavB wprowadza te atomy tlenu w określonej kolejności i z rygorystyczną kontrolą orientacji — istotną cechą dla aktywności biologicznej hormonu. 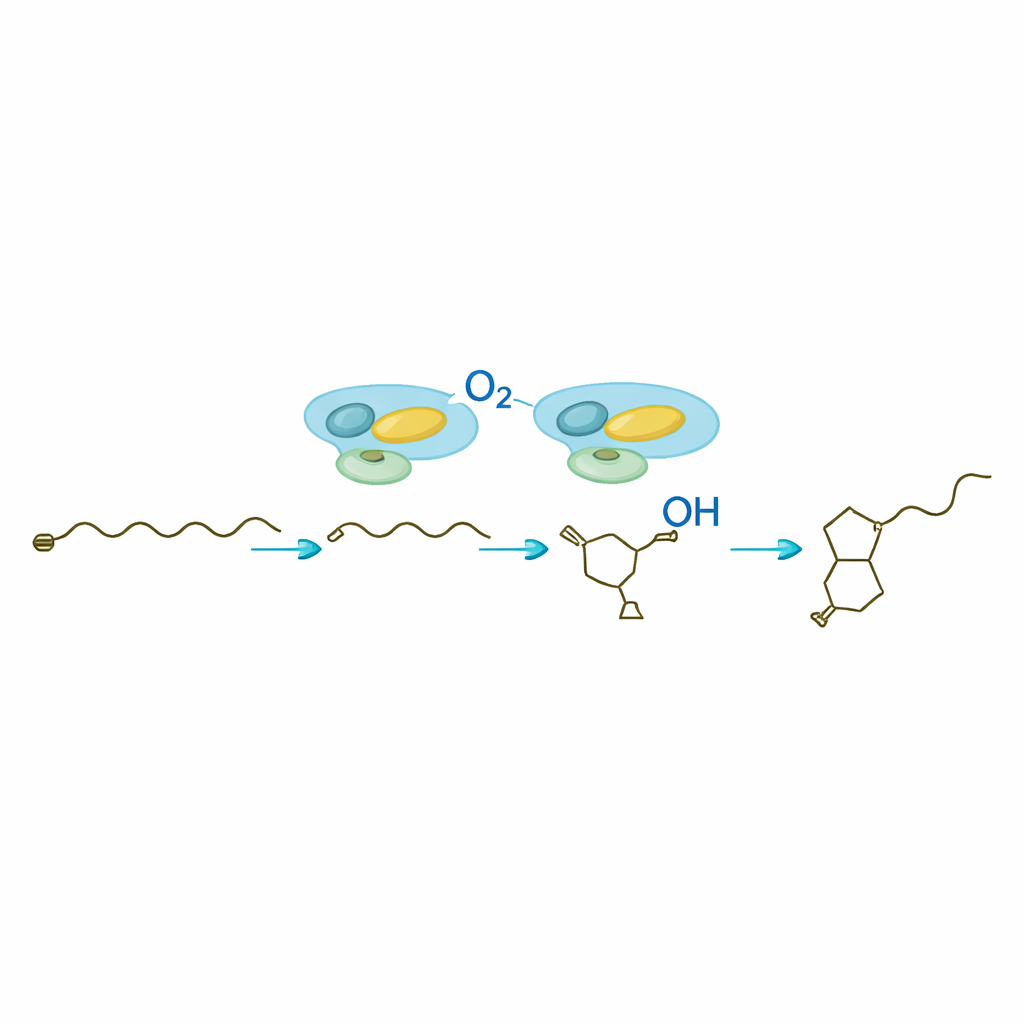
Wnioski z zielonej chemii płynące z enzymów bakteryjnych
Wspólnie SavA i SavB przekształcają zwykły blok konstrukcyjny pochodzący od kwasu tłuszczowego w precyzyjnie dostrojony związek sygnalizacyjny, używając jedynie tlenu z powietrza i standardowych pomocników komórkowych. W przeciwieństwie do wielu procesów przemysłowych, SavA nie potrzebuje dodatkowych środków redukujących ani reagentów ofiarnych; jego kofaktor flawinowy jedynie przenosi elektrony, podczas gdy substrat dostarcza napęd termodynamiczny reakcji. Autorzy wyróżniają SavA jako nowy typ wielozadaniowego flawoenzymu o dużym potencjale jako biokatalizator do zrównoważonej produkcji butenolidów i powiązanych motywów. W praktycznym wymiarze wykorzystanie lub inżynieria takich enzymów mogłaby w przyszłości pozwolić fabrykom — lub zaprojektowanym mikrobom — wytwarzać ważne fragmenty leków i środki rolnicze ze źródeł odnawialnych w łagodnych warunkach, zmniejszając zarówno koszty, jak i ślad środowiskowy.
Cytowanie: Li, W., Zhao, J., Zeng, W. et al. Trifunctional flavoenzyme-catalyzed asymmetric 4-alkyl-butenolide assembly in avenolide biosynthesis. Nat Commun 17, 2459 (2026). https://doi.org/10.1038/s41467-026-69265-8
Słowa kluczowe: biosynteza butenolidów, flawoenzym SavA, hormon avenolid, biokataliza, sygnalizacja Streptomyces