Clear Sky Science · pl
Degradery białka kapsydu wirusa denga wykazują odmienną farmakologię w porównaniu z inhibitorami kapsydu
Obrócić osłonkę wirusa przeciwko niemu samemu
Gorączka denga infekuje setki milionów ludzi rocznie, a mimo to lekarze wciąż nie dysponują pewnymi lekami przeciwwirusowymi. To badanie bada nową metodę unieszkodliwiania wirusa denga poprzez niszczenie jednego z jego kluczowych składników wewnątrz zakażonych komórek, zamiast jedynie prób blokowania jego aktywności. Praca pokazuje, że starannie zaprojektowane cząsteczki mogą znakować ważne białko wirusa do usunięcia przez komórkowy system utylizacji, ograniczając produkcję wirusa i osłabiając jego zdolność do ukrywania się przed naszą odpornością.
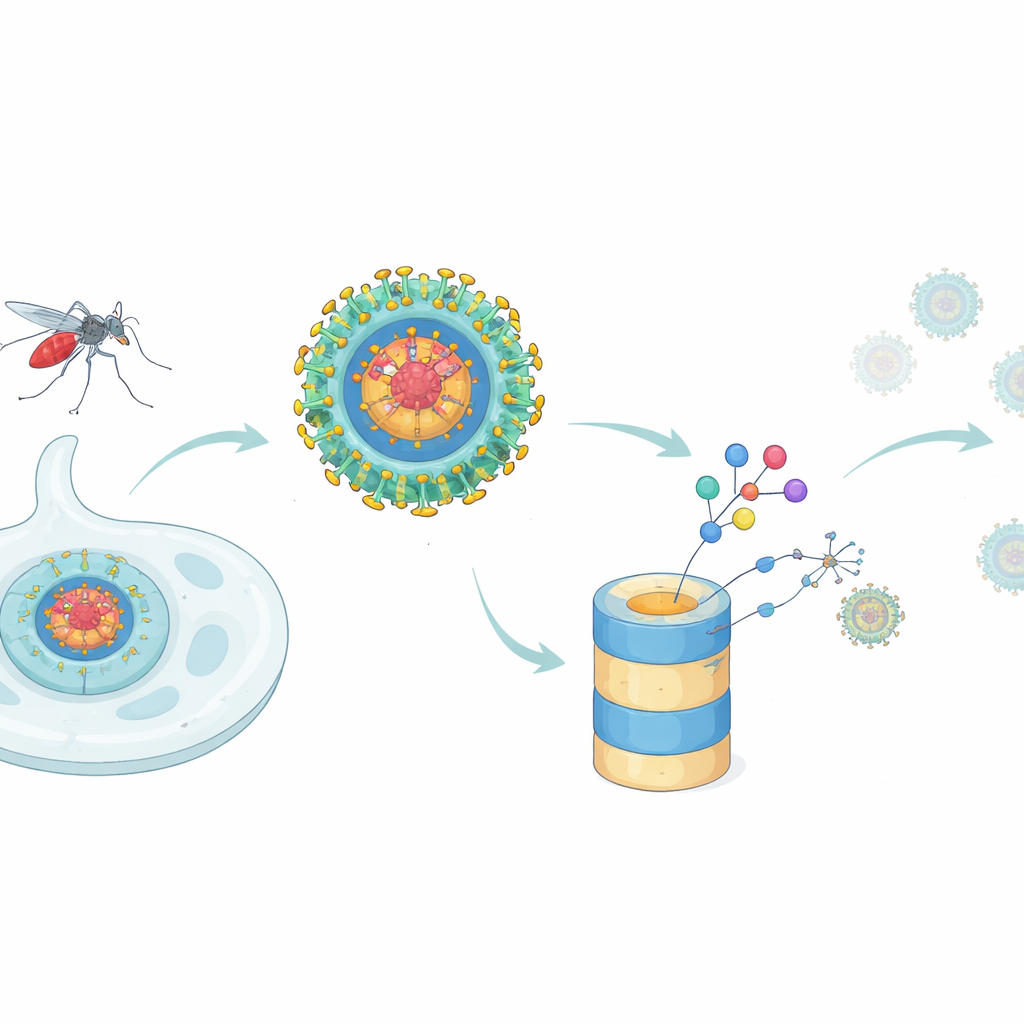
Nowa taktyka zatrzymywania dengu
Większość leków przeciwwirusowych działa jak zatyczki w maszynie: przyczepiają się do jednego miejsca funkcjonalnego białka wirusowego i próbują je zablokować. To podejście ma trudności, gdy jedno białko wirusa wykonuje wiele różnych funkcji, lub gdy drobne mutacje osłabiają przyczepność leku. Białko kapsydu dengu jest tego przykładem. Tworzy ono rdzeńową osłonkę pakującą materiał genetyczny do nowych cząstek, ale także wpływa na komórkę gospodarza poprzez interakcje z wieloma ludzkimi białkami i tłumienie odpowiedzi interferonowej — pierwszej linii alarmowej przeciw wirusom. Autorzy zapytali, czy nowsza koncepcja leków — celowane degradowanie białek — może wyjść poza klasyczne inhibitory, faktycznie usuwając białko kapsydu z zakażonych komórek.
Projektowanie molekularnego „łowcy nagród”
Aby zbudować taki degrader, badacze zaczęli od ST148, znanej małocząsteczkowej substancji wiążącej kapsyd dengu i zakłócającej składanie nowych cząstek wirusa. Chemicznie połączyli ST148 z drugim modułem rekrutującym ludzki kompleks enzymatyczny odpowiedzialny za znakowanie białek do degradacji. Powstałe chimeryczne cząsteczki, zwane PROTACami, mają kształt umożliwiający złapanie kapsydu jednym końcem i kompleksu ligazy E3 drugim, zbliżając je do siebie, aby kapsyd mógł zostać oznakowany ubikwityną i skierowany do proteasomu komórkowego — głównego niszczarki białek. Testując wiele długości łączników i grup rekrutujących ligazę, zidentyfikowali jeden wyróżniający się związek, nazwany RPG‑01‑132, który niezawodnie obniżał poziomy kapsydu w zakażonych komórkach w sposób zależny od formy ligazy CRBN i od prawidłowej funkcji proteasomu.
Zatrzymanie produkcji wirusa i unikania odpowiedzi immunologicznej
Mając działający degrader, zespół zbadał, jaki faktycznie ma on wpływ na zakażenie dengą. W komórkach pochodzenia wątrobowego zakażonych wirusem denga, RPG‑01‑132 powodował silny spadek liczby uwalnianych zakaźnych wirusów, w stężeniach, przy których tylko częściowo obniżał całkowite poziomy kapsydu. Co ważne, inne białka wirusowe i wirusowe RNA pozostały niezmienione, co pokazuje, że związek nie zatruwał po prostu ogólnej replikacji, lecz działał specyficznie przez utratę kapsydu. Mikroskopia elektronowa dała wizualny odczyt: komórki traktowane oryginalnym inhibitorem ST148 gromadziły stosy częściowo złożonych cząstek wirusa w retikulum endoplazmatycznym, zgodnie z blokadą składania, podczas gdy komórki traktowane degraderem wykazywały niemal brak widocznych wirionów. Degrader także przywracał zdolność sygnalizacji interferonu‑β w systemie reporterowym, co sugeruje, że pozafunkcyjna rola kapsydu w osłabianiu odporności wrodzonej może zostać odwrócona przez jego degradowanie.
Pokonanie różnorodności wirusowej i oporności na leki
Wirus denga występuje w czterech głównych serotypach, które różnią się wrażliwością na inhibitory ukierunkowane na kapsyd, a oporność może wynikać z pojedynczych mutacji. Autorzy porównali degrader z ST148 na reprezentatywnych szczepach wszystkich czterech serotypów oraz przeciwko wirusowi niosącemu mutację (S34L w kapsydzie), która wcześniej wykazywała, że ST148 jest nieskuteczny. Jak przewidywano, ST148 działał najlepiej na jednym serotypie i tracił aktywność wobec opornego wariantu. RPG‑01‑132, w przeciwieństwie do tego, wykazywał podobną potęgę przeciwwirusową we wszystkich serotypach i zachował aktywność wobec mutanta S34L, nadal działając przez tę samą ścieżkę degradacji zależną od CRBN. Ilustruje to kluczową zaletę farmakologii „wywołanej zdarzeniem”: degrader nie musi trwale przyczepiać się do każdej cząsteczki kapsydu cały czas, o ile potrafi wywołać wystarczającą liczbę zdarzeń degradacji, by przechylić równowagę.
Co to oznacza dla przyszłych terapii dengy
To badanie pokazuje, że białko kapsydu dengu można atakować nie tylko jako składnik strukturalny wirusa, lecz także jako usuwalny węzeł wspierający wiele etapów zakażenia i unikania odpowiedzi immunologicznej. Przekształcając tradycyjny inhibitor w degrader, badacze stworzyli związek, który blokuje produkcję wirusa, łagodzi część supresji odporności wrodzonej przez wirusa i pozostaje skuteczny w różnych szczepach wirusa oraz wobec znanej mutacji opornej. Sam RPG‑01‑132 będzie wymagał optymalizacji — lepszego wnikania do komórek, silniejszej aktywności w modelach zwierzęcych i starannych badań bezpieczeństwa — ale stanowi przekonujący dowód koncepcji. Szerzej, praca sugeruje, że przejęcie komórkowego systemu utylizacji może otworzyć nowe drogi do leków przeciwwirusowych, których wirusy trudniej ominąć i które mogą neutralizować białka pełniące różne role w zakażonych komórkach.
Cytowanie: Chakravarty, A., Wang, LN., Golden, R.P. et al. Degraders of the dengue virus capsid protein exhibit differentiated pharmacology relative to capsid inhibitors. Nat Commun 17, 2594 (2026). https://doi.org/10.1038/s41467-026-69263-w
Słowa kluczowe: wirus denga, białko kapsydu, celowane degradowanie białek, projektowanie leków przeciwwirusowych, PROTACy