Clear Sky Science · pl
Współdzielona aktywacja anionu przy centrum kobaltowym przez parowanie jonowe i projektowanie ligandów
Dlaczego mali partnerzy wokół metali mają znaczenie
Chemicy często koncentrują się na głównym „aktorze” reakcji — atomie metalu, który pomaga łamać i tworzyć wiązania. Jednak ta praca pokazuje, że cisi partnerzy krążący w pobliżu, niewidoczni gołym okiem, mogą całkowicie zmienić rolę metalu. Poprzez staranne ukształtowanie przestrzeni wokół atomu kobaltu autorzy ujawniają, jak dwa niemal wymienne aniony, często traktowane w chemii i bateriach jako bierni obserwatorzy, prowadzą do wyraźnie odmiennych rezultatów. 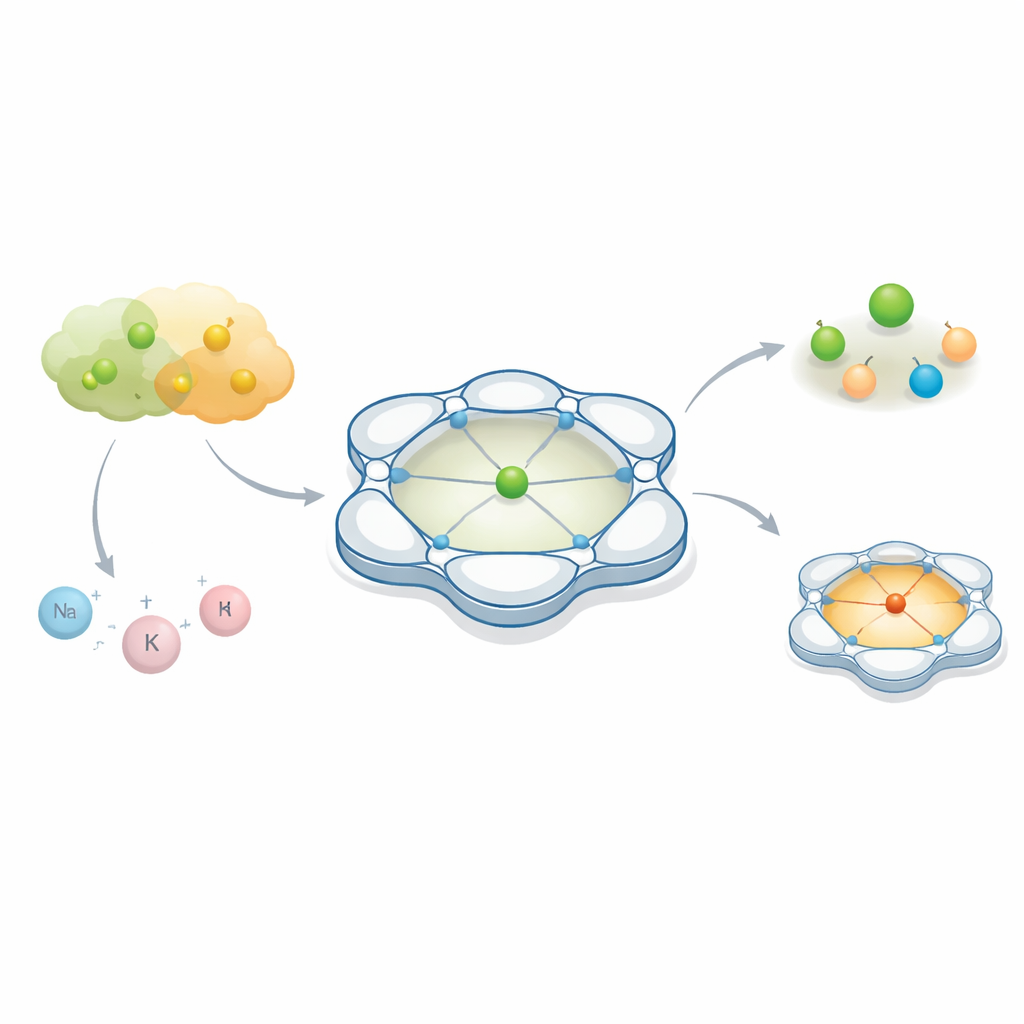
Budowanie dopasowanej kieszeni wokół kobaltu
Naukowcy zaprojektowali organiczny szkielet przypominający klatkę, nazwany Py4Im, który ciasno otacza jon kobaltu. Ten układ składa się z kilku powiązanych pierścieni pirydynowych i jednostki imidazolidynowej, które razem tworzą sztywną, miseczkowatą wnękę zawierającą pojedynczą grupę N–H. Ta mała wnęka jest „protyczna”, co oznacza, że może tworzyć wiązania wodorowe, i jest skierowana w określoną stronę, jak niewielki dok dla nadchodzących anionów. Gdy kobalt jest zespalany z tym ligandem, powstaje rodzina kompleksów o ładunku dodatnim, których ogólny kształt i wewnętrzna kieszeń pozostają niezmienne, podczas gdy anion przeciwstawny — ujemny partner — można wymieniać. Dzięki temu system jest idealnym polem doświadczalnym do obserwacji, jak różne aniony zachowują się w tym samym kontrolowanym środowisku.
Dwa podobne aniony, dwa zupełnie różne zachowania
Zespół porównał dwa powszechnie stosowane aniony: tetrafluoroboran (BF4−) i heksafluorofosforan (PF6−), które są szeroko używane jako tzw. słabo koordynujące aniony. Są popularne, ponieważ zwykle trzymają dystans od centrów metalicznych, stabilizując wysoce naładowane gatunki bez bezpośredniego zaangażowania. Ku zaskoczeniu, we wnęce Py4Im nie zachowują się jednakowo. W łagodnych warunkach PF6− oddaje jon fluorkowy kobaltowi, łamiąc silne wiązanie P–F i tworząc dobrze zdefiniowany kompleks kobalt–fluorek. Natomiast BF4−, zwykle uważany za bardziej „kruchy”, odmawia oddania fluoru w tych samych warunkach. Zamiast tego układa się w stabilne wiązanie z centrum kobaltu, nie przechodząc w krok rozszczepienia wiązania.
Obserwowanie parowania i ruchu jonów
Aby zrozumieć te kontrastujące zachowania, autorzy zastosowali kombinację wysokorozdzielczych technik NMR oraz obliczeń chemii kwantowej. Eksperymenty dyfuzyjne NMR mierzyły, jak szybko dodatnie i ujemne gatunki poruszają się w roztworze, co ujawnia, jak ciasno są sparowane. Pomiary wykazały, że BF4− tworzy z kompleksem kobaltu bliższą, bardziej trwałą parę jonową niż PF6−. Kieszeń Py4Im lokuje anion bezpośrednio pod pierścieniem imidazolidynowym, gdzie wiązania wodorowe z grupy N–H i pobliskich grup C–H utrzymują go na miejscu. Obliczenia komputerowe potwierdziły, że to silniejsze, kierunkowe parowanie z BF4− stabilizuje stan początkowy tak bardzo, że rozbicie wiązania B–F staje się nieznacznie niekorzystne, mimo iż to wiązanie jest z natury słabsze niż P–F w PF6−. PF6−, parując luźniej, może zbliżyć się, przenieść fluorek na kobalt i odejść jako PF5, prowadząc do kompleksu kobaltu z fluorem, który jest termodynamicznie osiągalny. 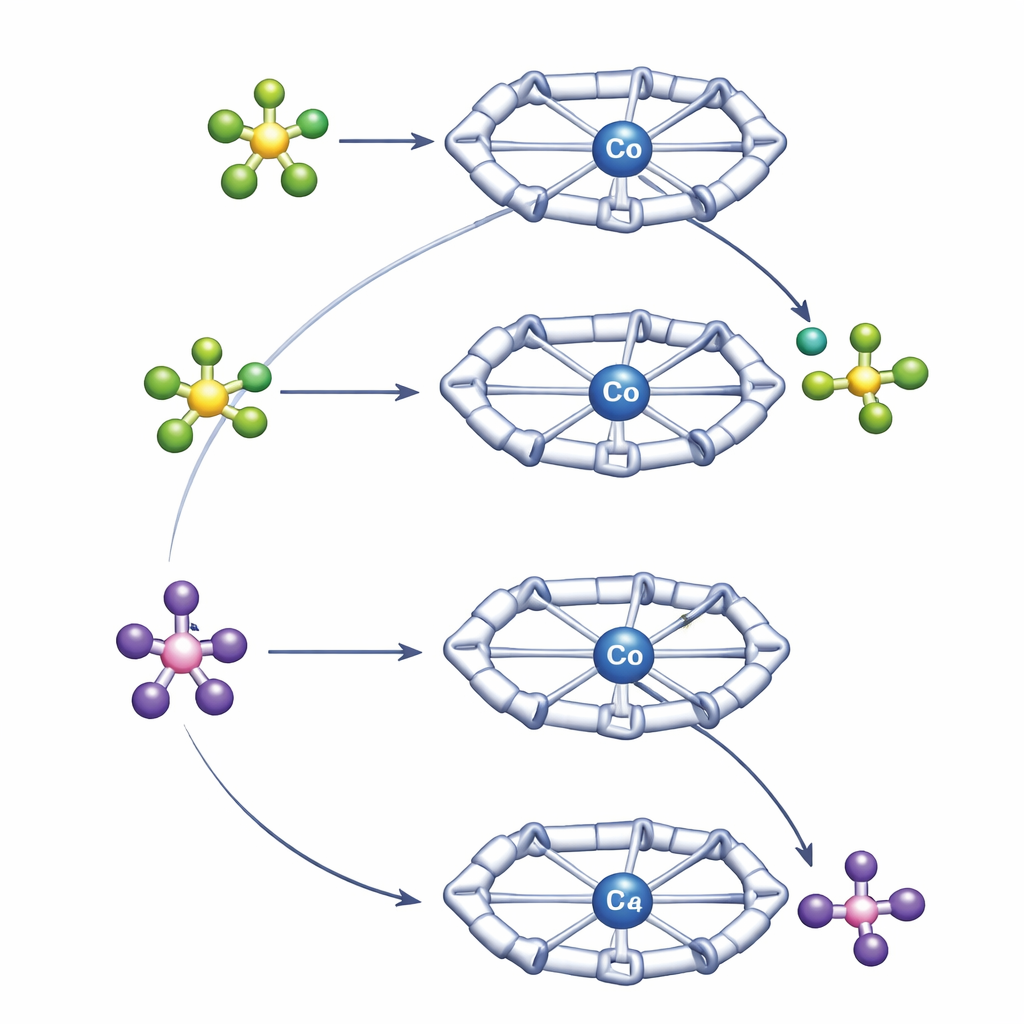
Przekształcenie związego fluorku w użyteczne narzędzie
Po utworzeniu kompleks kobalt–fluorek nie jest martwym końcem. Autorzy pokazują, że zachowuje się on jako nukleofilowe źródło fluorku — mówiąc prościej, potrafi dostarczyć fluorek do dodatnio naładowanych lub elektronowo ubogich partnerów. W roztworze ten gatunek kobalt–fluorkowy czysto przekazuje fluorek do reaktywnych centrów węgla, do atomów krzemu w chlorosilanach oraz do chlorków acylowych, generując organiczne fluorki, podczas gdy kompleks kobaltu przełącza się z powrotem w formę chlorkową lub wiąże nowego partnera. W sprytnym posunięciu zespół wykazał też, że BF4− można skłonić do oddania fluoru, jeśli obecna jest odrębna zasada, która „schwyta” pozostający fragment BF3. To przekształca drogę BF4−, zwykle niechętną, w taką, która również prowadzi do tego samego produktu kobalt–fluorkowego.
Co to oznacza dla projektowania inteligentniejszych katalizatorów
Dla niespecjalisty kluczowy przekaz jest taki, że jony dawniej traktowane jako obojętne sole tła mogą w rzeczywistości silnie sterować przebiegiem reakcji. Poprzez wyrzeźbienie precyzyjnej kieszeni wokół centrum metalicznego i kontrolę, jak ciasno aniony z nim parują, autorzy odwrócili oczekiwaną reaktywność dwóch niemal identycznych gatunków. PF6−, zwykle uznawany za wyjątkowo odporny, staje się łatwiejszym źródłem fluoru, podczas gdy BF4− zostaje zablokowany przez silniejsze parowanie, chyba że system otrzyma dodatkową pomoc. Ta praca dostarcza schematu wykorzystania projektowania ligandów i doboru anionów razem, aby regulować reaktywność kompleksu metalu — pomysł, który może wpłynąć na dziedziny od katalizy jednorodnej po projektowanie elektrolitów do zaawansowanych baterii, gdzie „cisi partnerzy” w roztworze mogą wcale nie być bierni.
Cytowanie: Tarifa, L., Cano-Asensio, J., López, J.A. et al. Cooperative anion activation at a cobalt center through ion pairing and ligand design. Nat Commun 17, 2469 (2026). https://doi.org/10.1038/s41467-026-69257-8
Słowa kluczowe: kompleksy kobaltu, słabo koordynujące aniony, transfer fluoru, parowanie jonów, projektowanie ligandów