Clear Sky Science · pl
Metaliczny siarczek molibdenu katalizuje protometaboliczne sieci reakcji dwutlenku węgla w warunkach ekstremalnych
Jak skały mogły zapoczątkować chemię życia
Długo zanim komórki żywe wyewoluowały enzymy, Ziemia i tak potrzebowała sposobów na przekształcanie prostych gazów, takich jak dwutlenek węgla, w organiczne związki, od których zależy życie. To badanie analizuje, czy niektóre naturalnie występujące minerały, podobne do tych spotykanych przy podwodnych źródłach hydrotermalnych, mogły działać jako prymitywne „silniki chemiczne”. Pokazując, że metaliczna forma siarczku molibdenu potrafi przekształcać dwutlenek węgla w zaskakująco rozbudowaną sieć związków organicznych, praca ta proponuje konkretny scenariusz, w jaki sposób podstawowa chemia życia mogła się rozpocząć na bezżyciowej planecie.

Gorące kominy i ukryte silniki chemiczne
Współczesne życie opiera się na złożonych sieciach reakcji, które przemieszczać węgiel w komórkach i ekosystemach. Sieci te zależą od białek zwanych enzymami, które same są efektem ewolucji. Kwestia zasadnicza brzmi: co istniało wcześniej. Autorzy zwrócili uwagę na kominy hydrotermalne — naturalne, gorące źródła na dnie oceanu bogate w siarczki metali i wodór — jako prawdopodobne środowisko najwcześniejszej chemii węgla. W takich miejscach gorąca, sprężona woda spotyka skały zawierające metale, takie jak żelazo, nikiel i molibden. Wcześniejsze eksperymenty wykazały, że niektóre z tych metali mogą przekształcać dwutlenek węgla w małe związki organiczne, lecz zwykle tylko fragmenty szlaków metabolicznych, nie pełne sieci.
Mineralna imitacja dawnych enzymów
Zespół skupił się na szczególnej formie siarczku molibdenu, zwanej fazą 1T′, której uporządkowanie atomowe naśladuje centra metal–siarka występujące we współczesnych enzymach przetwarzających dwutlenek węgla. W warunkach wysokiej temperatury i ciśnienia w wodzie, przy wodoru jako paliwie, ten minerał katalizował przekształcanie rozpuszczonego dwutlenku węgla (modelowanego jako wodorowęglan) w zaskakująco szeroki zakres kwasów organicznych. Poprzez staranne zmiany temperatury, czasu reakcji i ciśnienia gazu oraz śledzenie produktów metodami chromatografii, spektrometrii mas i NMR, zidentyfikowali 32 różne pośrednie i końcowe produkty powstające z tego samego prostego źródła węgla.
Odtworzenie podstawowych szlaków węgla bez enzymów
Te 32 związki nie są przypadkowe. Wiele z nich to te same molekuły, które leżą u podstaw współczesnego metabolizmu — takie jak octan, pirogronian, szczawiooctan, bursztynian i alfa-ketoglutaran. Razem pokrywają pięć głównych dróg fiksacji węgla używanych przez współczesne mikroby: szlak acetyl–CoA oraz warianty cyklu Krebsa i powiązanych pętli. W eksperymentach te ścieżki pojawiały się jako powiązana sieć: octan łączył kilka cykli; większe związki rozkładały się i na nowo tworzyły; a kluczowe pośredniki znikały i ponownie się pojawiały w miarę zmiany warunków. Produkcja kwasów wielowęglowych osiągała dużą wydajność — do około 70% przetworzonego węgla kończyło w cząsteczkach zawierających dwa lub więcej atomów węgla. Sieć reakcji wykazywała także oscylacje, w których ilości niektórych produktów rosły i malały w czasie, echo dynamicznego zachowania żywych systemów chemicznych.
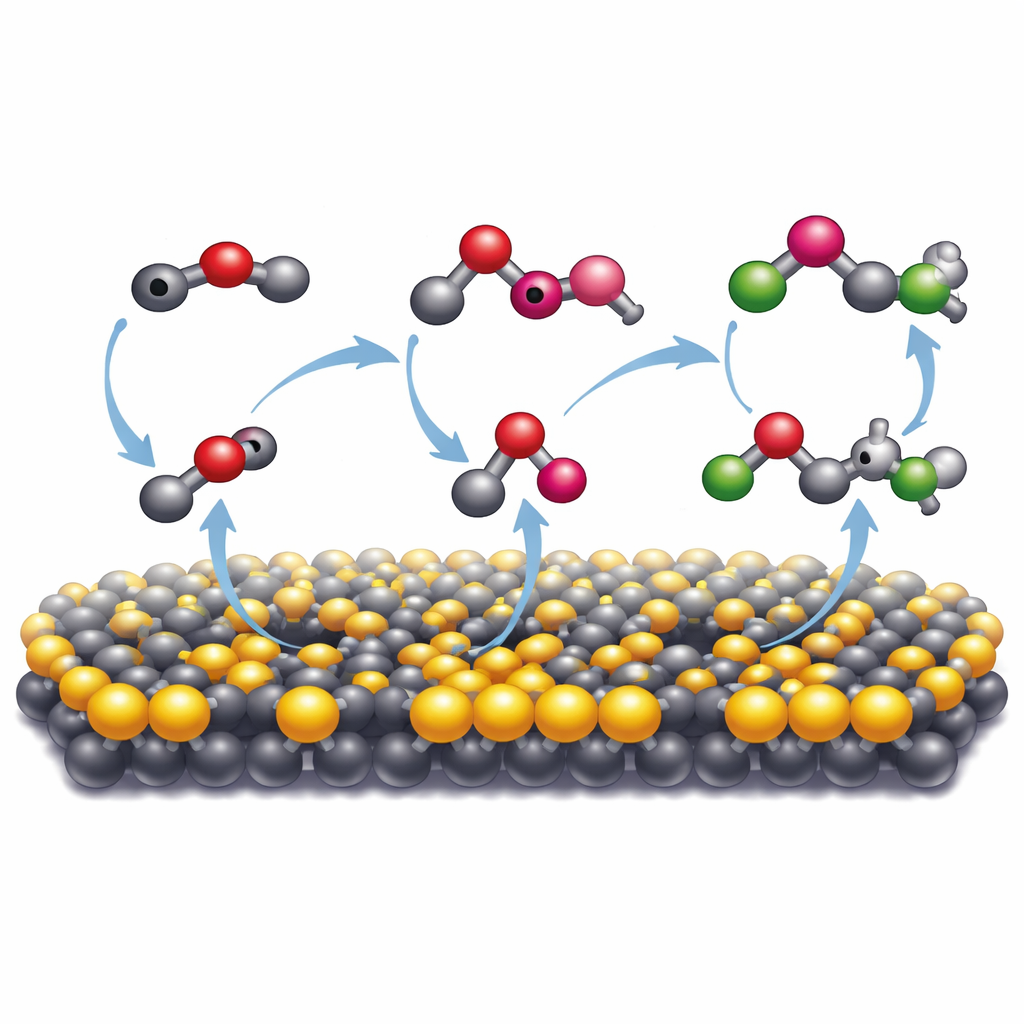
Jak minerał sprawia, że atomy węgla łączą siły
Aby zrozumieć, dlaczego ten konkretny minerał był tak skuteczny, badacze porównali go z bardziej powszechną formą siarczku molibdenu o innej strukturze atomowej. Tylko metaliczna, zniekształcona postać — z wieloma brakującymi atomami siarki — napędzała intensywne tworzenie większych związków organicznych. Techniki spektroskopowe wykazały, że na tej powierzchni tlenek węgla pochodzący z dwutlenku węgla wiąże się silnie i jest dalej redukowany do wysoce reaktywnych fragmentów, czyli rodników. Te rodniki są stabilizowane w wystarczającym stopniu na powierzchni minerału, by zderzać się ze sobą i tworzyć nowe wiązania węgiel–węgiel. Pomiary spinów elektronowych potwierdziły obecność takich rodników, a dodanie chemicznej „pułapki” na rodniki ostro zahamowało powstawanie produktów wielowęglowych. Symulacje komputerowe poparły ten obraz, pokazując, że wakancje siarkowe i zmieniona struktura elektronowa fazy 1T′ ułatwiają powierzchni oddawanie elektronów i przyciąganie fragmentów węglowych blisko siebie, tak by mogły się połączyć.
Z chemii skalnej do pierwszego metabolizmu
Zebrane razem, te wyniki sugerują, że niektóre siarczki metali na wczesnej Ziemi mogły napędzać złożoną, samoorganizującą się chemię węgla na długo przed pojawieniem się enzymów. W warunkach kominów hydrotermalnych, gdzie gorące, bogate w wodór płyny spotykają dwutlenek węgla i skały zawierające metale, minerał taki jak 1T′ siarczek molibdenu mógł ciągle przekształcać nieorganiczny węgiel w sieć powiązanych dróg organicznych przypominających współczesne cykle metaboliczne. Dla osoby niebędącej specjalistą kluczowy przekaz jest taki, że centralna chemia życia mogła nie potrzebować życia, by się zacząć: w odpowiednich warunkach proste skały, woda i gaz mogą samoistnie zbudować wiele z tych samych cząsteczek i pętli reakcyjnych, z których komórki korzystają do dziś.
Cytowanie: Chen, P., Liu, X., He, D. et al. Metallic molybdenum sulfide catalyses protometabolic carbon dioxide reaction networks under extreme conditions. Nat Commun 17, 2395 (2026). https://doi.org/10.1038/s41467-026-69255-w
Słowa kluczowe: pochodzenie życia, chemia prebiotyczna, kominy hydrotermalne, fiksacja węgla, siarczek molibdenu