Clear Sky Science · pl
Atomowo zorientowane pojedyncze atomy w kieszeni wiążącej imitującej enzym kierujące ścieżkami dechlorowania–polimeryzacji w stronę upcyklingu zanieczyszczeń wodnych
Przekształcanie toksycznej wody w użyteczne materiały
Wiele chemikaliów przemysłowych, które trafiają do rzek i jezior, jest jednocześnie trwałych i toksycznych, zwłaszcza te zawierające atomy chloru. Zamiast jedynie spalać te zanieczyszczenia agresywnymi zabiegami, badanie to pokazuje, jak przekształcić jeden taki związek w elementy budulcowe tworzyw sztucznych, jednocześnie oczyszczając wodę i wytwarzając użyteczny produkt.
Dlaczego zanieczyszczenia bogate w chlor są trudne do usunięcia
Współczesne oczyszczanie wody często opiera się na silnych utleniaczach — związkach chemicznych, które odbierają elektrony z zanieczyszczeń, aż te rozpadną się do dwutlenku węgla i innych prostych cząsteczek. Choć skuteczne, podejście „spal wszystko” zużywa duże ilości reagentów, może wytwarzać szkodliwe produkty uboczne i marnuje zawartość węgla z zanieczyszczeń. Związki zawierające chlor, takie jak szeroko stosowany 2,4,6-trichlorofenol, są szczególnie kłopotliwe. Atomy chloru odciągają elektrony z cząsteczki, utrudniając inicjację reakcji łańcuchowych przez reaktywne rodniki. W efekcie oczyszczanie przebiega wolno, w pozostałościach utrzymuje się chlor, a także istnieje ryzyko powstania nowych toksycznych substancji.
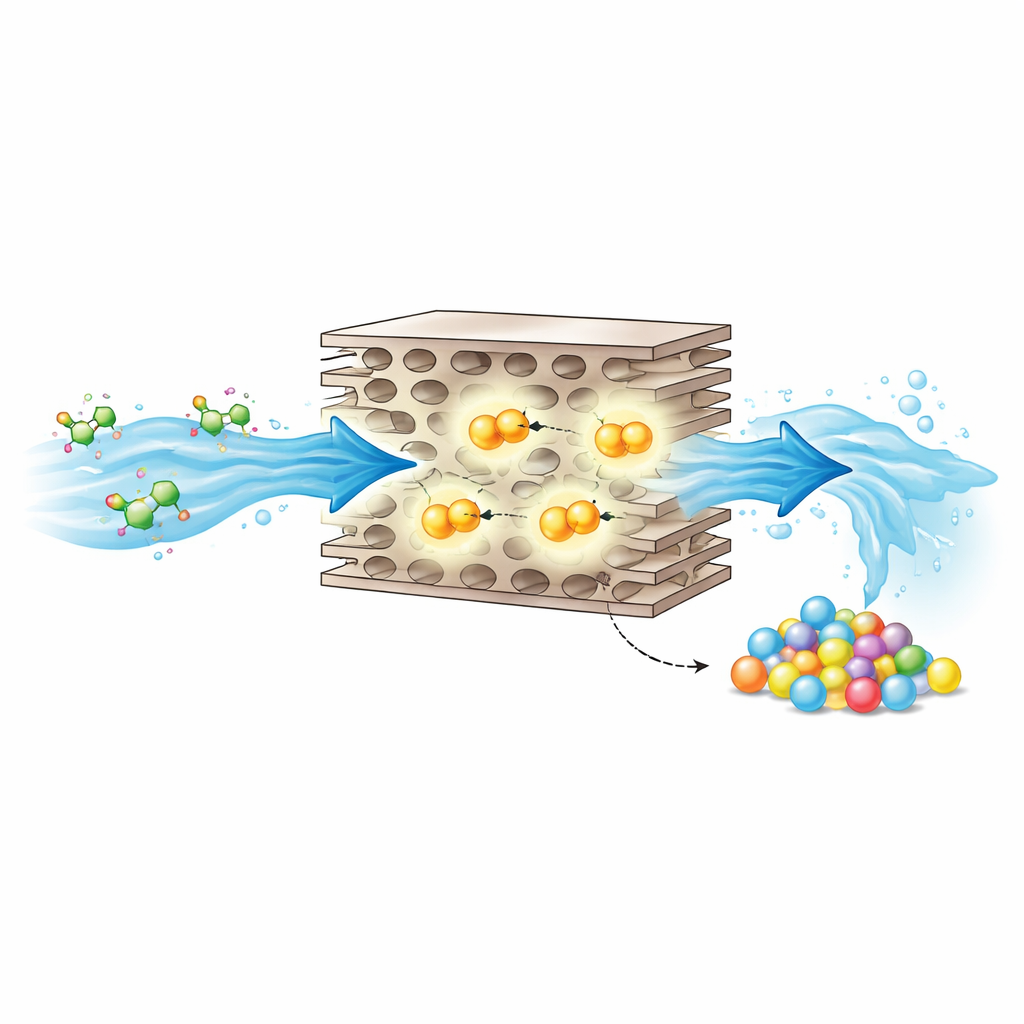
Wykorzystywanie sztuczek naturalnych enzymów
Przyroda rozwiązuje podobne problemy za pomocą enzymów, które precyzyjnie umieszczają atomy metalu we wnękach zbudowanych z aminokwasów. Enzymy te używają grup hydroksylowych pochodzących z wody do ataku na „aktywowane” miejscach w pobliżu atomów halogenu, sprawnie usuwając chlor przy jednoczesnym dodaniu bardziej reaktywnych miejsc do dalszej chemii. Inspirowani tym, autorzy zaprojektowali stały katalizator naśladujący aktywne miejsce enzymu na skali atomowej. Zakotwiczyli pojedyncze atomy żelaza na arkuszach węglika azotu i dołączyli dodatkowy atom azotu nad każdym żelazem, tworząc pięciokrotne „koordynacyjne” miejsce osiowe. Otaczające atomy węgla i azotu tworzą hydrofobowo-polarne mikrośrodowisko zachowujące się jak kieszeń wiążąca, utrzymując zarówno zanieczyszczenie, jak i utleniacz blisko centrum żelazowego.
Nowa, spokojna ścieżka utleniania
Gdy utleniacz — nadsiarczanowy (peroxymonosulfate) — styka się z tym katalizatorem, nie tworzy się znane rojowisko krótkożyjących rodników ani tlenu singletowego, na których opiera się wiele systemów zaawansowanego utleniania. Zamiast tego pomiary spektroskopowe i testy elektrochemiczne pokazują, że utleniacz tworzy trwały kompleks powierzchniowy z miejscem żelazowym. Kompleks ten odciąga elektrony bezpośrednio z pobliskiego chlorowanego zanieczyszczenia w kontrolowanym, dwuelektronowym kroku. W tym procesie utleniacz przekształca się w reaktywną, na powierzchni związana grupę hydroksylową, podczas gdy zanieczyszczenie przechodzi przez krótkotrwały, dodatnio naładowany stan pośredni. Ta „ścieżka transferu elektronów” jest krótkozasięgowa i wysoce selektywna: cząsteczki zanieczyszczenia muszą siedzieć tuż obok aktywowanego utleniacza na powierzchni katalizatora, zamiast być atakowane losowo w wodzie.
Od dechlorowania do monomerów polimerowych
Gdy zanieczyszczenie odda elektrony, jego atomy chloru stają się łatwiejsze do oderwania. Cząsteczki wody wchodzą jako nukleofile — dawcy elektronów — które zastępują pozycje zawierające chlor grupami hydroksylowymi, najpierw w najbardziej odsłoniętych miejscach, a potem na sąsiednich pozycjach. Modelowanie komputerowe i eksperymenty z izotopowym śledzeniem pokazują, że nowe grupy hydroksylowe pochodzą z wody, a nie bezpośrednio z utleniacza. W miarę usuwania chloru cząsteczka zyskuje wiele grup hydroksylowych, które stabilizują reaktywne pośredniki i otwierają liczne punkty łączenia. Zamiast rozkładu do gazów, zmodyfikowane cząsteczki łączą się głównie przez mostki tlenowe, tworząc oligomery przypominające poli(terfenylo) eter: średniej wielkości, w dużym stopniu zdechlorowane polimery przylegające do powierzchni katalizatora.
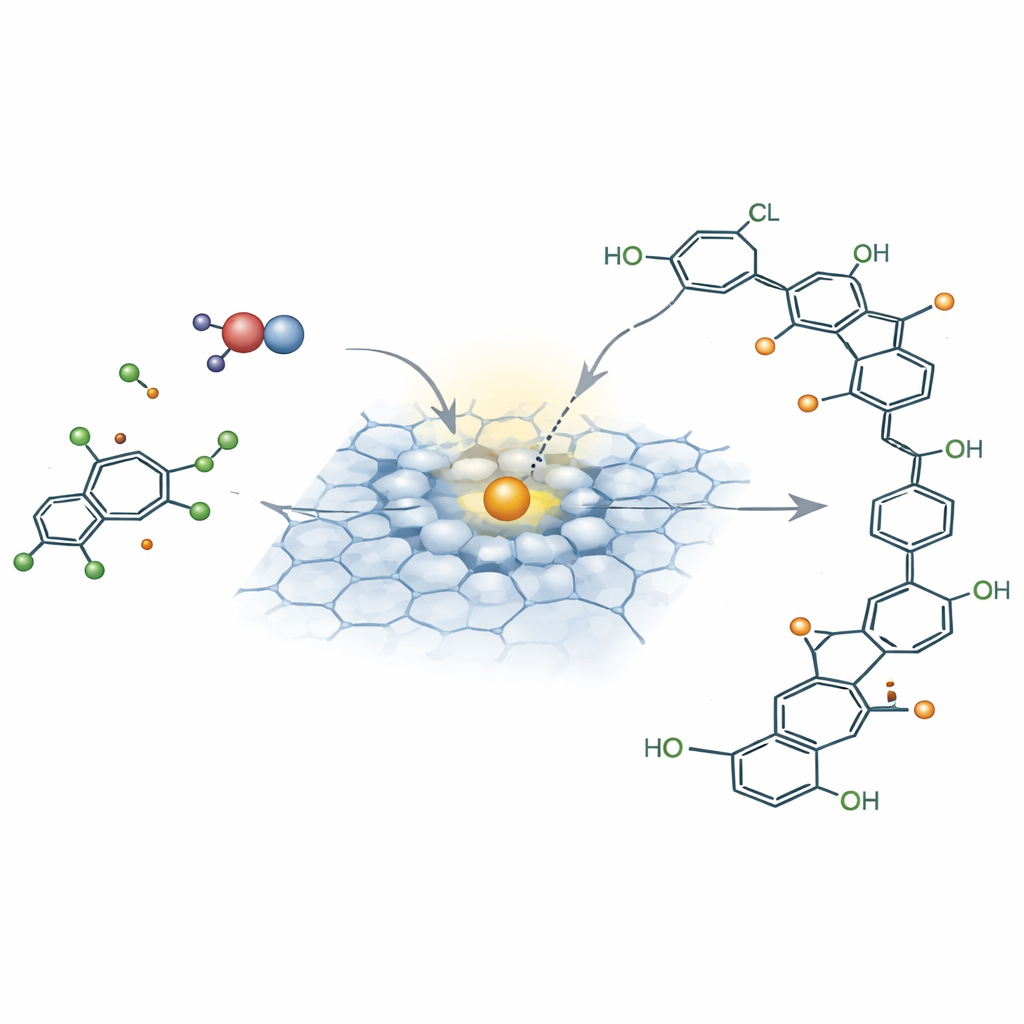
Skalowanie: oczyszczanie wody przy jednoczesnej produkcji tworzyw
Co istotne, produkty polimerowe można zebrać i przetworzyć. Poprzez przepłukanie katalizatora rozpuszczalnikami organicznymi badacze odzyskali znaczną część węgla jako stałe oligomery, które następnie przetworzono na jednorodne granulaty tworzyw sztucznych przy użyciu standardowych etapów wytłaczania i granulacji. Testy wykazały, że katalizator utrzymuje wysoką aktywność przez wiele cykli i w realistycznych układach, w tym reaktorach membranowych i złożach fluidalnych przetwarzających chloroorganiczne ścieki. Analizy ekonomiczne i środowiskowe sugerują, że ten system inspirowany enzymami mógłby działać przy niższych kosztach i znacznie mniejszym śladzie węglowym niż tradycyjne metody utleniania, zwłaszcza gdy uwzględni się wartość odzyskanych tworzyw.
Co to oznacza dla przyszłego oczyszczania wody
Zamiast wyboru między kontrolą zanieczyszczeń a odzyskiem surowców, praca ta wskazuje na przyszłość, w której zanieczyszczona woda staje się surowcem. Dzięki zaprojektowaniu pojedynczych atomów metali tak, by zachowywały się jak centra naturalnych enzymów, autorzy kierują reakcję z dala od całkowitej destrukcji ku selektywnemu dechlorowaniu i tworzeniu polimerów. Mówiąc prościej, przekształcają problematyczny, chloroorganiczny zanieczyszczający związek w bezpieczniejsze, niechloroorganiczne prekursory tworzyw sztucznych, jednocześnie oczyszczając wodę — co dowodzi obiecującej drogi ku czystszym i bardziej obiegowym technologiom oczyszczania wód.
Cytowanie: Wu, B., Li, Z., Zhang, J. et al. Axially engineered single atoms in enzyme-mimic-binding pocket steering dehalogenation–polymerization pathways toward water pollutant upcycling. Nat Commun 17, 2405 (2026). https://doi.org/10.1038/s41467-026-69253-y
Słowa kluczowe: zanieczyszczenie wód, związki chloroorganiczne, zaawansowana utlenianie, katalizatory jednoatomowe, upcykling tworzyw sztucznych