Clear Sky Science · pl
Interpretowalne i generatywne modele głębokiego uczenia wyjaśniają fazowo-separujące motywy obszarów niestrukturalnych
Dlaczego małe fragmenty białek mają znaczenie
W każdej z naszych komórek istotne cząsteczki często gromadzą się w kroplopodobne grudki zwane kondensatami biomolekularnymi. Kropelki te pomagają organizować reakcje chemiczne bez użycia błon, kształtując aktywację genów, przekazywanie sygnałów i reakcje komórki na stres. Wiele takich kropelek powstaje z elastycznych odcinków białek znanych jako regiony wewnętrznie niestrukturalne. Jednak biologom wciąż trudno jest określić krótkie fragmenty sekwencji, które faktycznie inicjują powstawanie tych kropelek. W tym badaniu przedstawiono ramy uczenia głębokiego, PhaSeMotif, które potrafią zarówno odnajdywać te kluczowe segmenty, jak i projektować nowe, dając badaczom potężne narzędzie do badania i przeprogramowywania kondensatów komórkowych.
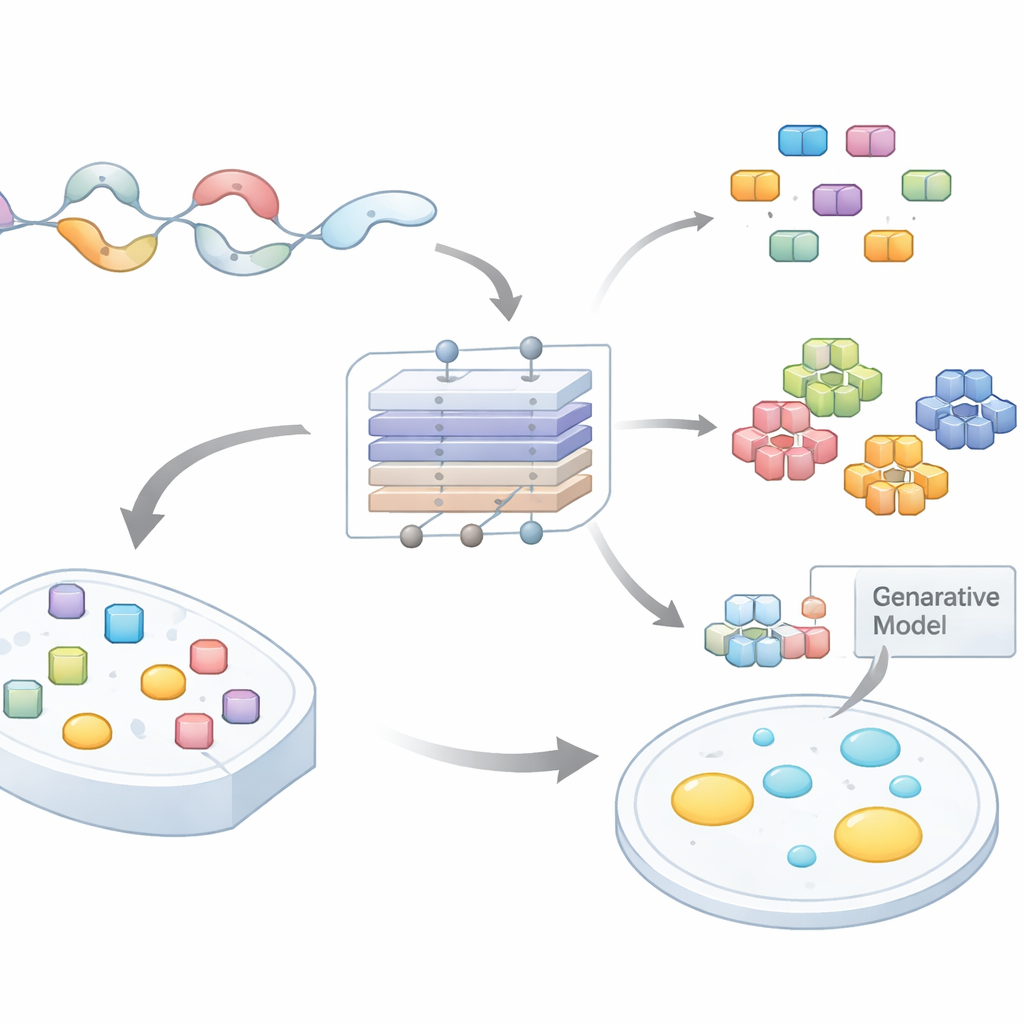
Z nieuporządkowanych ogonków białek do testowalnych hipotez
Wiele białek ma długie, elastyczne ogonki, które nie składają się w stałe struktury. Regiony te są wzbogacone w określone aminokwasy i często zawierają powtarzające się wzory lub krótkie motywy. Coraz więcej dowodów pokazuje, że takie motywy napędzają kondensację przez umożliwienie wielu słabych oddziaływań jednocześnie. Jednak przeszukiwanie całych proteomów w celu wskazania, które krótkie fragmenty są istotne i dlaczego, stanowiło poważne ograniczenie. Istniejące narzędzia obliczeniowe zwykle oceniają całe białka lub duże regiony, dając niewiele wskazówek, gdzie wprowadzać mutacje lub co testować w laboratorium. Autorzy postanowili zbudować model, który przewiduje nie tylko, czy region niestrukturalny może tworzyć kropelki, lecz także które dokładne podsekwencje wykonują największą pracę.
Mapa motywów napędzających tworzenie kropelek stworzona przez uczenie głębokie
Zespół skompilował obszerne zbiory danych regionów niestrukturalnych z kilku gatunków i oznaczył je zgodnie z prawdopodobieństwem, że ich białka macierzyste ulegają rozdziałowi fazowemu. Następnie wytrenowali sieć neuronową opartą na mechanizmie attention, PhaSeMotif, która przyjmuje sekwencję aminokwasów dowolnej długości i zwraca wynik wskazujący zdolność do tworzenia kropelek. Kluczowe było użycie połączenia warstw konwolucyjnych i mechanizmów attention, aby ocenić, jak bardzo każde krótkie okno sekwencji przyczynia się do tego wyniku. Przez śledzenie wstecz przez model (stosując techniki podobne do guided backpropagation) autorzy wydobyli fragmenty o wysokim znaczeniu — krótkie motywy często krótsze niż 20 reszt — które model uznał za niezbędne do tworzenia kropelek.
Weryfikacja przewidywań w żywych komórkach
Aby sprawdzić, czy te motywy rzeczywiście mają znaczenie, badacze sięgnęli po system aktywowany światłem w komórkach ludzkich. Połączyli przewidywane regiony niestrukturalne tworzące kropelki z modułem oligomeryzacji czułym na światło i znacznikiem fluorescencyjnym. Pod niebieskim światłem konstrukty te szybko kondensowały się w jasne punkty, raportując rozdział fazowy w czasie rzeczywistym. Zespół następnie chirurgicznie usuwał pojedyncze motywy, zastępując je neutralnymi, elastycznymi łącznikami o tej samej długości. W 82% z 17 zmodyfikowanych sekwencji testowanych tworzenie kropelek było znacząco osłabione lub całkowicie zanikło, podczas gdy kontrolne mutacje poza segmentami wskazanymi przez PhaSeMotif często miały niewielki efekt. Co ważne, wiele z tych kluczowych motywów nakładało się na miejsca, gdzie znane są mutacje związane z chorobami zakłócające kondensację, co podkreśla ich biologiczne znaczenie.
Odkrywanie słownika typów motywów
Mając w ręku ponad 17 000 motywów, autorzy zapytali następnie, czy istnieją wspólne „smaki” segmentów napędzających kropelkowanie. Przeanalizowali skład aminokwasowy i wzorce występowania, a następnie pogrupowali motywy w dziewięć klastrów. Niektóre klastry były bogate w reszty aromatyczne i glicynę, co zgadza się z lepkością wynikającą z oddziaływań π–π i kation–π. Inne zawierały oddzielone kawałki ładunków dodatnich i ujemnych, sprzyjając przyciąganiu elektrostatycznemu i selektywnemu partycjonowaniu do konkretnych kondensatów. Dodatkowe klastry dominowane były przez prolinę i glicynę, które wspierają elastyczność, lub przez długie sekwencje glutaminy, które mogą tworzyć gęste sieci wiązań wodorowych. Różne przedziały komórkowe i typy kondensatów wykazywały charakterystyczne mieszanki tych klas motywów, co sugeruje, że skład motywów pomaga określić, gdzie i z jakimi partnerami białko będzie kondensować.
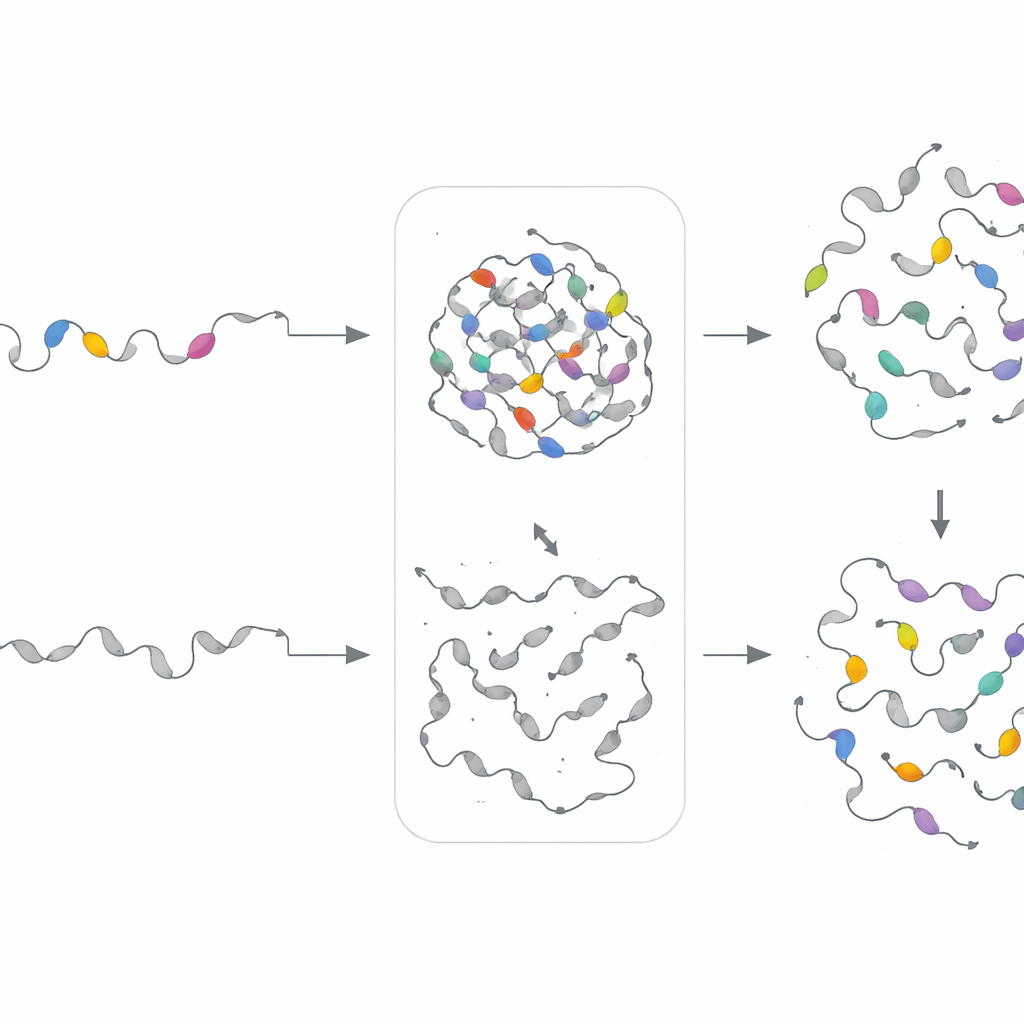
Projektowanie nowych motywów, by przetestować reguły
Aby sprawdzić, czy to „przepisy” motywów — a nie dokładne sekwencje — rządzą zachowaniem kropelek, zespół zbudował oddzielne modele generatywne dla każdego klastra motywów. Te wariacyjne autoenkodery nauczyły się statystycznych wzorców dla danego klastra, a następnie generowały nowe, sztuczne sekwencje dzielące te same odciski kompozycyjne, lecz różniące się dokładnym uporządkowaniem. Badacze eksperymentalnie wstawili te syntetyczne motywy do białek, z których usunięto oryginalne segmenty. Co godne uwagi, w 18 z 21 przypadków zaprojektowane motywy przywróciły rozdział fazowy w komórkach, czasem nawet dostrajając szybkość lub gęstość formowania kropelek. Pokazuje to, że PhaSeMotif uchwycił podstawowe zasady projektowania, które można ponownie wykorzystać do budowy lub naprawy regionów tworzących kropelki.
Znaczenie dla biologii i chorób
Łącząc interpretowalne uczenie głębokie z projektowaniem generatywnym i bezpośrednimi testami w komórkach, praca ta przekształca mglistą koncepcję „niestrukturalnych regionów tworzących kropelki” w konkretny zestaw krótkich, składanych motywów. Dla osób spoza tej dziedziny główny wniosek jest taki, że naukowcy potrafią teraz czytać i pisać drobne fragmenty białek kontrolujące, jak kondensaty komórkowe się składają, mieszają i ulegają dysfunkcji. Otwiera to drogę do szybszego wykrywania mutacji powodujących choroby w tych segmentach, jaśniejszych badań mechanistycznych nad tym, jak kondensaty organizują fizjologię komórkową, a w końcu do racjonalnego projektowania białek, które sterują kropelkami w zastosowaniach terapeutycznych lub syntetycznej biologii.
Cytowanie: Yang, H., You, K., Ma, L. et al. Interpretable and generative deep learning models explicate phase separating intrinsically disordered motifs. Nat Commun 17, 2571 (2026). https://doi.org/10.1038/s41467-026-69252-z
Słowa kluczowe: kondensaty biomolekularne, białka wewnętrznie niestrukturalne, rozdzielanie fazowe, głębokie uczenie, motywy białkowe