Clear Sky Science · pl
Hepatocyty funkcjonalnie przeprogramowane przez komórki raka jelita grubego o wysokim poziomie KIAA1199 sprzyjają gromadzeniu pro‑metastatycznych neutrofilów Egr1+
Gdy rak jelita atakuje wątrobę
Większość osób wyobraża sobie rozprzestrzenianie się raka jako proces, w którym zbuntowane komórki odrywają się i dryfują do nowych narządów. To badanie pokazuje bardziej niepokojącą historię: guzy jelita grubego mogą dyskretnie przebudować wątrobę na długo przed pojawieniem się jakichkolwiek komórek nowotworowych, tworząc „glebę” sprzyjającą osiedlaniu się przyszłych przerzutów. Zrozumienie tego ukrytego etapu przygotowawczego może otworzyć drogę do terapii, które zatrzymają przerzuty do wątroby — główną przyczynę zgonów w raku jelita grubego — zanim się rozpoczną.
Skryte przygotowania przed przybyciem guza
Rak jelita grubego często daje przerzuty do wątroby, ale tylko niektóre guzy robią to agresywnie. Autorzy skupili się na cząsteczce KIAA1199, która występuje w nadmiarze w rakach o wysokim ryzyku. W modelach mysich i próbkach od pacjentów guzy o wysokim poziomie KIAA1199 nie tylko rosły szybciej; również przygotowywały wątrobę do stania się „pre‑metastatyczną niszą” — mikrośrodowiskiem wyjątkowo przyjaznym dla napływających komórek nowotworowych. Nawet gdy guzy wątroby były wtórnie zaszczepiane eksperymentalnie z oddzielnego źródła, zwierzęta z guzami jelita grubego o wysokim KIAA1199 rozwijały znacznie więcej przerzutów wątroby i umierały szybciej. To dowodzi, że sygnały z guza pierwotnego, nie tylko wędrujące komórki nowotworowe, przekształcały wątrobę z wyprzedzeniem.
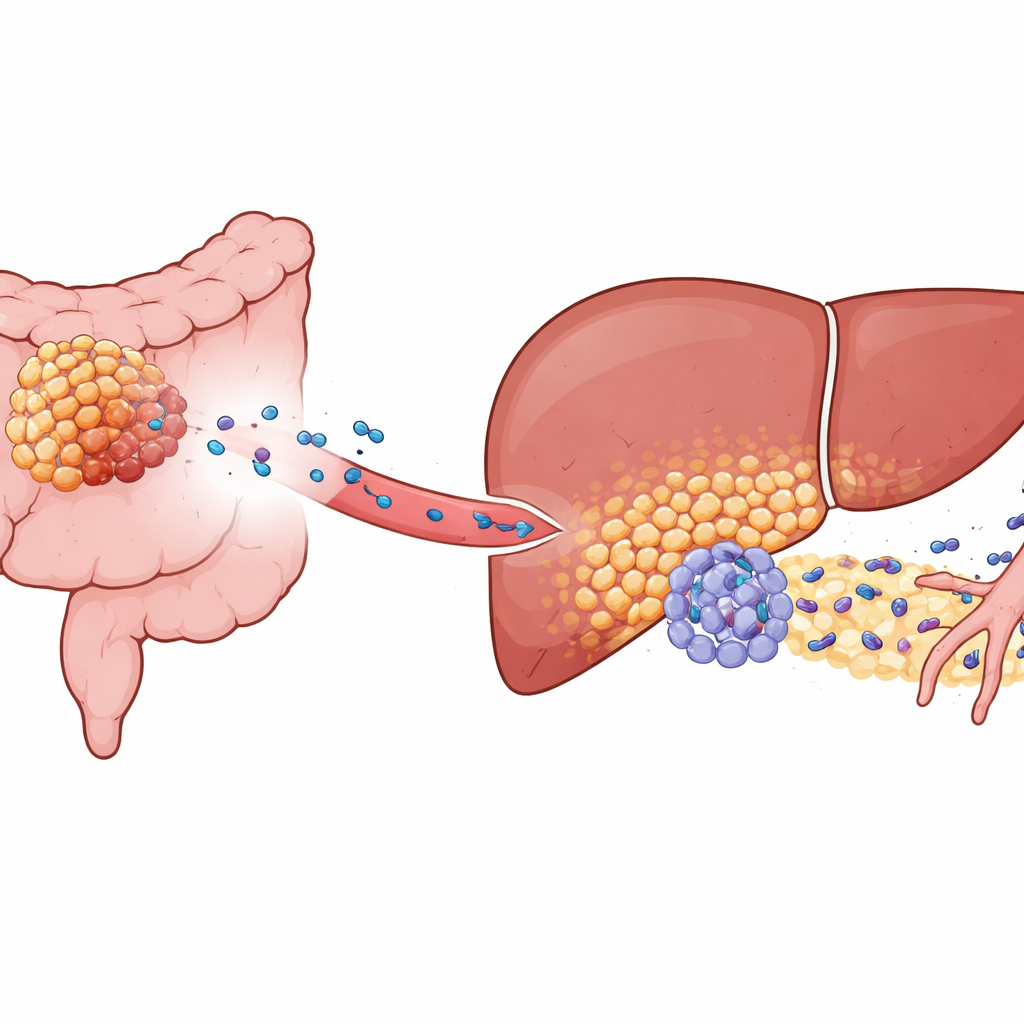
Komórki wątroby przekształcone w pomocników guza
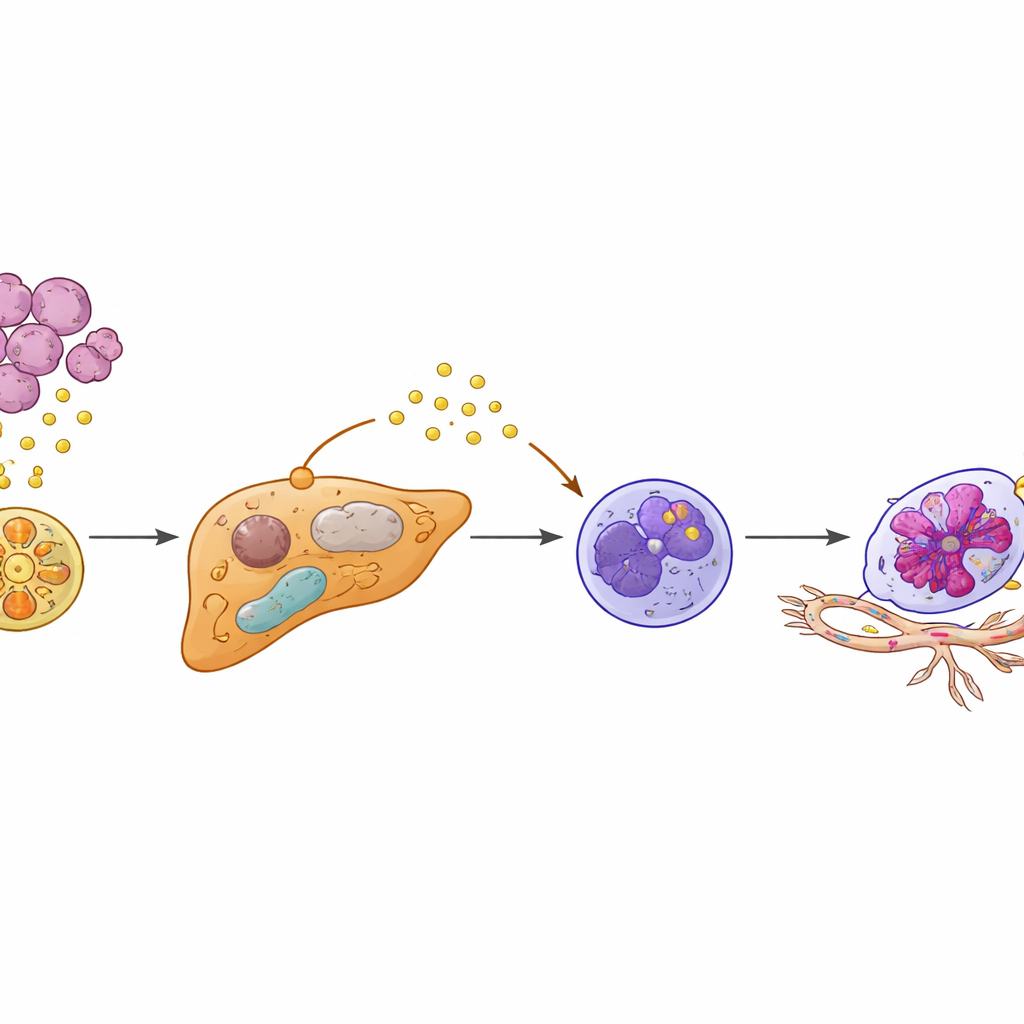
Wnikliwsze badania z użyciem pojedynczokomórkowego sekwencjonowania i mapowania przestrzennego pozwoliły przyjrzeć się tkance wątroby z dużą rozdzielczością. Odkryto szczególną podpopulację hepatocytów — normalnie podstawowych komórek wątroby — które zostały „funkcjonalnie przeprogramowane”. Te komórki pojawiały się tylko w obecności guzów o wysokim poziomie KIAA1199. Zamiast spokojnie zarządzać metabolizmem, zmienione hepatocyty przestawiły się na bardziej podobny do złośliwego program metaboliczny i obniżyły aktywność ochronnego regulatora PPARγ, który zwykle pomaga kontrolować stany zapalne i odpowiedzi na stres. Przy tłumionym PPARγ hepatocyty zaczęły produkować duże ilości białka SAA2, uwalniając je do otoczenia, szczególnie na granicy między tkanką wątroby a nacierającymi komórkami nowotworowymi.
Przekształcanie zwykłych obrońców w pro‑metastatyczne neutrofile
Neutrofile — białe krwinki znane głównie z walki z infekcjami — również zachowywały się nietypowo w tej przygotowanej wątrobie. Autorzy zidentyfikowali specjalną podpopulację o sygnaturze „Egr1+”, nazwaną od czynnika transkrypcyjnego, który przeprogramowuje funkcjonowanie tych komórek. Zamiast przybywać z krwi już zmienione, neutrofile wydawały się być lokalnie reedukowane przez przeprogramowane hepatocyty. SAA2 uwalniane przez hepatocyty wiązało się z receptorem FPR2 na pobliskich neutrofilach, uruchamiając wewnątrzkomórkowy szlak PI3K‑AKT, który stabilizował aktywność Egr1. W efekcie powstawały dłużej żyjące, wysoce aktywne neutrofile wydzielające duże ilości VEGFA, silnego czynnika pobudzającego tworzenie nowych naczyń. Te neutrofile Egr1+ gromadziły się na styku guza i wątroby, dokładnie tam, gdzie wyrastały nowe, kruche naczynia.
Budowanie naczyń krwionośnych przyjaznych komórkom nowotworowym
Badanie wykazuje, że te reedukowane neutrofile nie są obserwatorami — aktywnie przekształcają naczynia wątroby. W hodowlach komórkowych czynniki uwalniane przez neutrofile Egr1+ powodowały wzrost, migrację i formowanie struktur rurowych przez komórki śródbłonka, przypominających nowe naczynia. U myszy dodanie neutrofili Egr1+ zwiększało przerzuty do wątroby i przyspieszało zgon. Zablokowanie kluczowych etapów tego łańcucha — albo sygnału SAA2–FPR2 do neutrofili, albo dalszego szlaku PI3K‑AKT — przerywało przeżywalność neutrofili i produkcję VEGFA, zmniejszając wzrost naczyń i rozprzestrzenianie przerzutów. Podobnie przywrócenie aktywności PPARγ w hepatocytach za pomocą leku przeciwcukrzycowego rosiglitazonu obniżało poziomy SAA2, hamowało pojawianie się neutrofili Egr1+ i istotnie zmniejszało przerzuty do wątroby w modelach przedklinicznych.
Od mechanizmu do przewidywania i zapobiegania
Ponieważ KIAA1199 w guzie i SAA2 w wątrobie leżą wysoko w tej kaskadzie, autorzy sprawdzili, czy te białka mogą pomóc zidentyfikować pacjentów o wysokim ryzyku przerzutów do wątroby. W kilku kohortach pacjentów osoby z wysokim poziomem obu markerów we krwi były znacznie bardziej narażone na rozwój przerzutów wątroby i robiły to szybciej. Prosty łączony wskaźnik KIAA1199–SAA2 przewyższał każdy marker osobno w przewidywaniu ryzyka i został umieszczony w klinicznym „nomogramie”, który szacuje prawdopodobieństwo rozprzestrzenienia się do wątroby w ciągu następnych dwóch lat u konkretnego pacjenta. Razem wyniki rysują wyraźny obraz: guzy jelita grubego z wysokim KIAA1199 wysyłają sygnały w pęcherzykach, które przepisują hepatocyty, a te z kolei przekształcają pobliskie neutrofile w długo żyjących, budujących naczynia wspólników. Celowanie w oś KIAA1199–PPARγ/SAA2–Egr1 — poprzez leki metaboliczne, modulatory układu odpornościowego lub oba rodzaje terapii — może umożliwić nie tylko leczenie istniejących przerzutów wątroby, ale też ich zapobieganie, zanim się zakorzenią.
Cytowanie: Li, L., Zhao, L., Cao, K. et al. Hepatocytes functionally reprogrammed by KIAA1199-high colorectal cancer cells favour the accumulation of pro-metastatic Egr1+ neutrophils. Nat Commun 17, 2462 (2026). https://doi.org/10.1038/s41467-026-69250-1
Słowa kluczowe: przerzuty raka jelita grubego do wątroby, pre‑metastatyczna nisza, neutrofile, reprogramowanie hepatocytów, mikrośrodowisko nowotworu