Clear Sky Science · pl
Zmniejszenie metylacji lizyny 4 histonu 3.3 w przyśrodkowej wyniosłości zwojowej i w podwzgórzu odtwarza fenotypy zaburzeń neurorozwojowych
Jak maleńkie chemiczne znaczniki kształtują mózg i ciało
Dlaczego niektóre zmiany genetyczne powodują jednocześnie problemy z uczeniem się i nietypowy wzrost, na przykład bardzo mały wzrost w dzieciństwie, a otyłość w dorosłości? To badanie przygląda się drobnym chemicznym znacznikom na białkach pakujących DNA w mózgu i pokazuje, jak ich zaburzenie w zaledwie dwóch kluczowych regionach może rozlać się na drgawki, zachowania przypominające lęk, problemy z pamięcią i dramatyczne zmiany masy ciała u myszy.
Włączniki na ściemniaczach genomu
W każdej komórce mózgu DNA jest owinięte wokół białek przypominających szpule, zwanych histonami. Znaczniki chemiczne umieszczane na tych histonach działają jak pokrętła ściemniacza, przygaszając lub zwiększając aktywność grup genów. Jeden z takich znaczników, dodawany w miejscu zwanym H3K4, jest mocno związany z włączaniem genów. Badania genetyczne u ludzi wykazały, że osoby z wadami enzymów dodających lub usuwających ten znacznik często mają zaburzenia neurorozwojowe łączące upośledzenie intelektualne, padaczkę i nieprawidłowy wzrost. Nie było jednak jasne, które komórki mózgu są najbardziej wrażliwe na tę dysfunkcję i jak ich zaburzenie może łączyć pobudliwość mózgu z metabolizmem całego organizmu.
Celowanie w dwa krytyczne ośrodki mózgu
Naukowcy zaprojektowali myszy, w których mutantna wersja białka histonowego (H3.3K4M) była włączana tylko w komórkach pochodzących z dwóch zarodkowych regionów mózgu: przyśrodkowej wyniosłości zwojowej, która produkuje wiele hamujących komórek „hamulcowych”, oraz rozwijającego się podwzgórza, które reguluje apetyt, hormony i bilans energetyczny. Ta mutacja specyficznie blokuje metylację H3K4, nie eliminując samych histonów. Testy potwierdziły, że mutantne białko było szeroko obecne w celowanych obszarach, a normalne znaczniki H3K4 były tam mocno zredukowane, podczas gdy ogólny poziom histonów pozostał stabilny. Ten projekt naśladuje wiele ludzkich przypadków, w których wadliwa jest tylko jedna kopia genu związana z H3K4, a nie cały gen jest nieobecny.
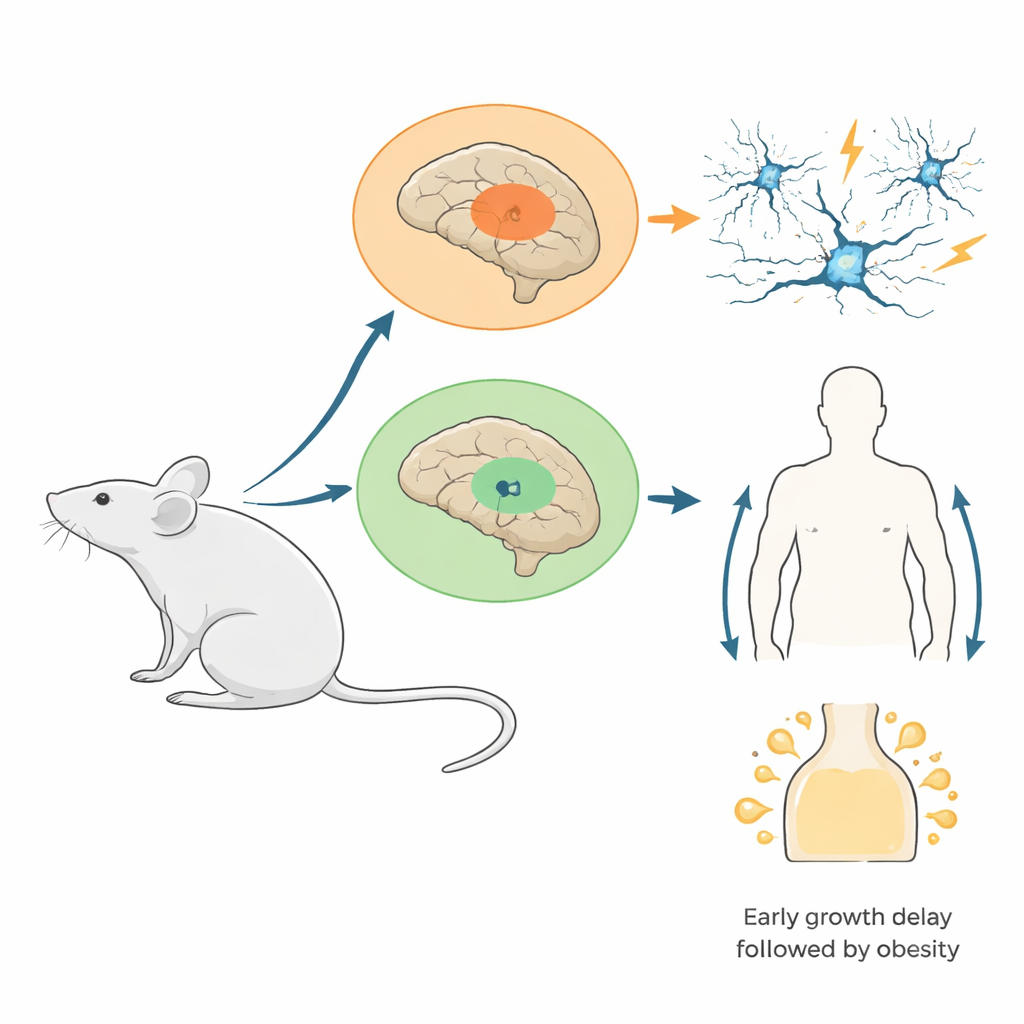
Od brakujących hamulców do obwodów podatnych na drgawki
W miarę jak myszy dojrzewały, konsekwencje dla obwodów mózgowych stały się oczywiste. Młode mutanty miały mniej hamujących interneuronów w korze i hipokampie, zwłaszcza szybkostrzelnego typu, który normalnie utrzymuje rytmy neuronalne w ścisłym tempie. Szczegółowe zapisy wykazały, że pozostałe interneurony były obecne, ale bardziej zmienne w swoich właściwościach elektrycznych, co sugeruje zaburzenie ich dojrzewania. Po stymulacji hipokampa w preparatach skrawkowych zwykłe wysokoczęstotliwościowe oscylacje „gamma” — rytmy elektryczne powiązane z przetwarzaniem informacji — były słabsze i wolniejsze, a pojawiały się nieprawidłowe epizody przypominające wybuchy. U żywych zwierząt wiele mutantów, szczególnie samice, rozwijało spontaniczne drgawki i było znacznie bardziej wrażliwych na drgawki wywołane lekami. Wcześnie w rozwoju zespół ustalił, że utrata tych komórek wynika głównie z zaburzonej migracji interneuronów do kory, a nie z nasilonej śmierci komórek czy zmniejszonego podziału komórek.
Przestawianie aktywności genów w komórkach powiązanych z drgawkami
Aby powiązać te zmiany strukturalne z kontrolą genów, zespół zastosował sekwencjonowanie pojedynczych jąder, które czyta zarówno aktywność genów, jak i dostępność DNA w pojedynczych komórkach. W embrionalnej przyśrodkowej wyniosłości zwojowej większość genów zmienionych u mutantów była wyciszona, w tym kluczowi regulatorzy kierujący komórki w stronę określonych hamujących losów. W dojrzałych interneuronach zachwiana została równowaga między podtypami, a grupy genów zaangażowanych w tworzenie połączeń i kontrolę prądów potasowych — przepływów, które pomagają ustawiać prędkość wyładowań — były źle regulowane. Analiza sieci podkreśliła skoordynowane zaburzenie genów kanałów potasowych, które już wiadomo, iż wpływają na padaczkę i rytmy mózgowe, dostarczając bezpośredniego molekularnego powiązania między utratą znacznika histonowego, zmienioną tożsamością interneuronów i podatnością na drgawki.
Nierównowaga podwzgórzowa i dwuetapowa krzywa wzrostu
Podwzgórze opowiadało uzupełniającą historię skoncentrowaną na wzroście ciała. Jako młode, szczenięta mutantów były mniejsze, a znaczna część z nich umierała wcześnie. Jednak ocalałe później jadły więcej, gromadziły tłuszcz i rozwijały wysokie poziomy hormonu leptyny, co wskazuje na otyłość i prawdopodobną odporność na leptynę. Analiza pojedynczych komórek embrionalnego podwzgórza ujawniła więcej właściwie dzielących się komórek progenitorowych, ale mniej komórek przeznaczonych dla kluczowych jąder związanych z jedzeniem, zwłaszcza regionów, które normalnie wyczuwają stan odżywienia i regulują hormon wzrostu. W dorosłym podwzgórzu skład komórkowy został przekształcony: astrocyty znacznie wzrosły, oligodendrocyty zmalały, a wyspecjalizowane komórki bariery zwane tanycytami i sąsiednie gleje straciły uporządkowaną organizację na styku mózgu z krążącymi hormonami i składnikami odżywczymi. Te zmiany strukturalne i w ekspresji genów prawdopodobnie zniekształcają sposób, w jaki mózg wyczuwa zapasy energii i kontroluje apetyt.
Behawioralne echo ludzkich zaburzeń neurorozwojowych
Zachowanie myszy odzwierciedlało symptomy obserwowane w wielu stanach neurorozwojowych. Wykazywały silniejsze zachowania przypominające lęk, zmienioną chód, zmniejszoną spontaniczną aktywność w domu i słabsze wyniki w zadaniach badających pamięć, rozpoznawanie obiektów i filtrowanie zaskakujących dźwięków. W niektórych testach ujawniono zwiększoną impulsywność. W wielu miarach samice wykazywały tendencję do silniejszych objawów niż samce, co sugeruje, że specyficzne dla płci systemy hormonalne i regulacja genów mogą wchodzić w interakcje ze znacznikami histonowymi i kształtować wrażliwość.
Co to oznacza dla zdrowia ludzi
W sumie wyniki pokazują, że osłabienie jednego zestawu znaczników histonowych w zaledwie dwóch embrionalnych ośrodkach mózgu wystarcza, by odtworzyć szeroką konstelację problemów: mniej hamujących „hamulców”, niestabilne sieci mózgowe, drgawki, zaburzone obwody regulujące odżywianie i nieprawidłowy wzrost ciała. Dla osób niebędących specjalistami kluczowe przesłanie jest takie, że znaki epigenetyczne, takie jak metylacja H3K4, nie są niejasnymi dodatkami, lecz precyzyjnymi pokrętłami kontrolnymi, które pomagają rozwijającym się komórkom mózgu stać się właściwym typem, we właściwym miejscu i czasie. Gdy te pokrętła są źle ustawione, jak w wielu rzadkich zespołach genetycznych, skutkiem może być ściśle powiązana kombinacja objawów poznawczych, behawioralnych i metabolicznych. Zrozumienie tych wspólnych korzeni może ostatecznie nakierować terapie, które korygują nie tylko jeden objaw, jak drgawki czy otyłość, lecz powiązany system, z którego one wynikają.
Cytowanie: Li, J., Tanzillo, A.F., Pizzirusso, G. et al. Reducing methylation of histone 3.3 lysine 4 in the medial ganglionic eminence and hypothalamus recapitulates neurodevelopmental disorder phenotypes. Nat Commun 17, 2984 (2026). https://doi.org/10.1038/s41467-026-69248-9
Słowa kluczowe: epigenetyka, interneurony, podwzgórze, drgawki, otyłość