Clear Sky Science · pl
Oddzielanie separacji fazowej od formowania fibryli zachowuje aktywność biomolekularnych kondensatów
Dlaczego ma to znaczenie dla zdrowia mózgu
Wiele chorób mózgu, w tym choroba Alzheimera, wiąże się z białkami, które z czasem zbrylają się w twarde, włókniste sploty. Te same białka mogą także tworzyć miększe, przypominające krople struktury wewnątrz komórek, które pomagają organizować reakcje chemiczne — nieco jak mikroskopijne, płynne stanowiska pracy. W tym badaniu postawiono kluczowe pytanie: czy można powstrzymać szkodliwe utwardzanie tych kropli w włókna, nie niszcząc ich użytecznej, codziennej funkcji? Autorzy pokazują, że powszechny metabolit komórkowy, aminokwas L-arginina, potrafi to zrobić w przypadku istotnego dla choroby Alzheimera białka Tau.
Od wolno pływającego białka do malutkich kropli
W komórkach pewne białka nie zawsze pozostają równomiernie rozproszone w płynnym wnętrzu. Zamiast tego mogą gromadzić się w kroplach, zwanych biomolekularnymi kondensatami, które zachowują się jak bardzo miękkie żele lub gęste ciecze. Zespół skupił się na Tau — białku, które normalnie pomaga budować i stabilizować mikrotubule — puste filamenty pełniące rolę „dróg” wewnątrz komórek nerwowych. Tau jest też znane z tworzenia włókien amyloidowych, sztywnych włókien obecnych w splątkach charakterystycznych dla wielu chorób neurodegeneracyjnych. Aby zbadać, jak krople Tau ewoluują w czasie, badacze skonstruowali wersję białka nazwaną SynTag-Tau, która tworzy aktywne kondensaty starzejące się do włókien amyloidowych w dogodnym, eksperymentalnym zakresie czasowym, bez konieczności stosowania silnych dodatków.
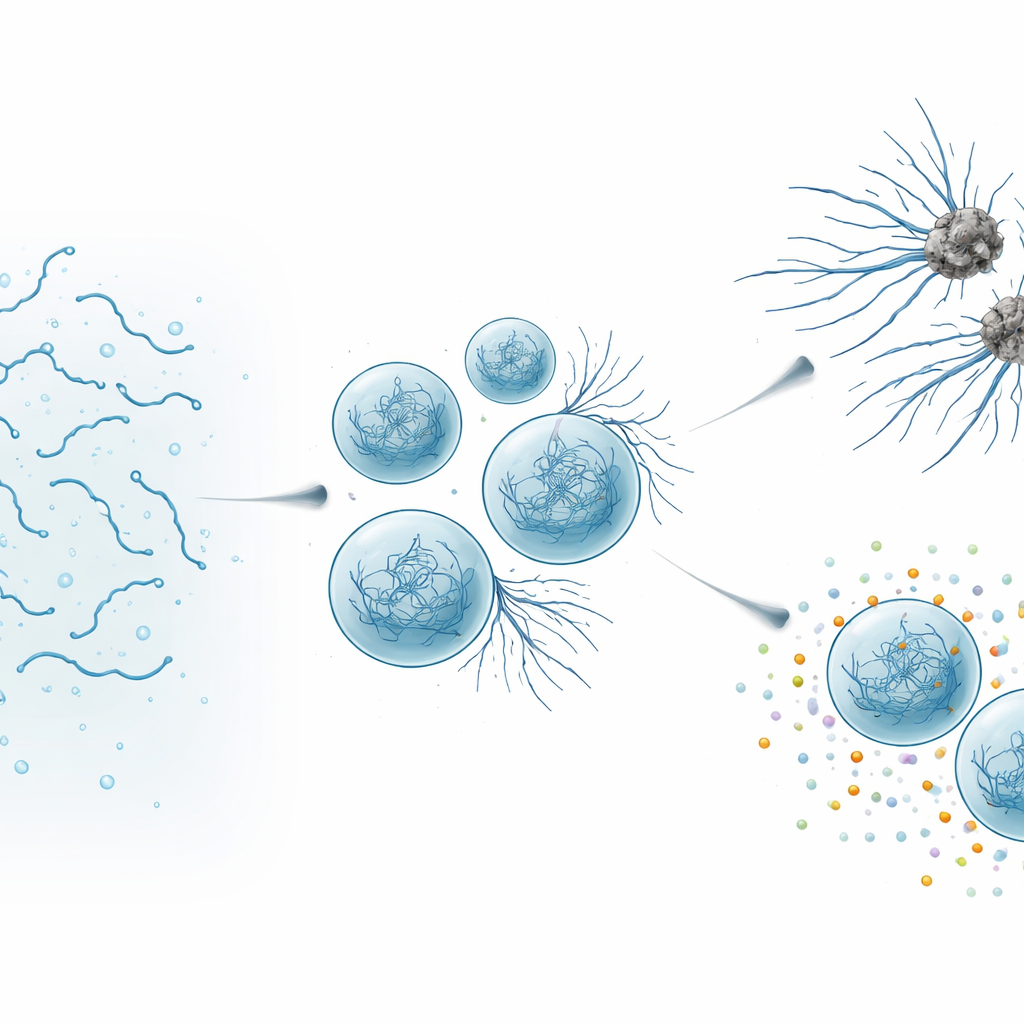
Kiedy pomocne krople stają się szkodliwe
Przy użyciu mikroskopii o wysokiej rozdzielczości i pomiarów biofizycznych autorzy obserwowali zmiany kropli SynTag-Tau w ciągu godzin. Świeże krople zachowywały się jak ciecze: łatwo się scalały, ich cząsteczki poruszały się szybko i nie było oznak uporządkowanej struktury. Z czasem krople zwalniały i usztywniały się, a cienkie włókna zaczęły wyrastać z ich powierzchni w otaczający roztwór. Wrażliwe metody optyczne wykazały, że te włókna miały ściśle upakowaną architekturę „cross–beta” typową dla amyloidu. Co istotne, powierzchnia — granica między gęstą kroplą a otaczającym płynem — działała jako miejsce, w którym fibryle pojawiały się najpierw. W miarę starzenia się kropli i pojawiania się kolejnych włókien funkcja Tau ulegała pogorszeniu: kondensaty coraz mniej efektywnie przyciągały tubulinę, budulec mikrotubul, aż w końcu traciły zdolność wspierania ich składania.
Małe cząsteczki przechylające równowagę
Następnie badacze zapytali, czy proste metabolity mogą spowolnić lub zapobiec przejściu ze stanu płynnego w włókna, pozostawiając jednocześnie same krople nietknięte. Przesiewając kilka naturalnie występujących małych cząsteczek, odkryli, że dodatnio naładowane aminokwasy L-arginina i L-lizyna silnie opóźniały lub blokowały tworzenie włókien amyloidowych ze świecących się kropli SynTag-Tau, nie hamując jednocześnie tworzenia kropli w realistycznych, niskomolowych stężeniach. Dla kontrastu, ujemnie naładowane aminokwasy, takie jak glutaminian i asparaginian, przyspieszały powstawanie włókien, a ogólnie działające na białka środki chemiczne albo nie pomagały, albo zaburzały same kondensaty. Fluorescencyjny odpowiednik L-argininy wykazał, że cząsteczka ta woli osiadać wewnątrz kondensatów Tau niż na zewnątrz, co sugeruje, że działa tam, gdzie jest najbardziej potrzebna.
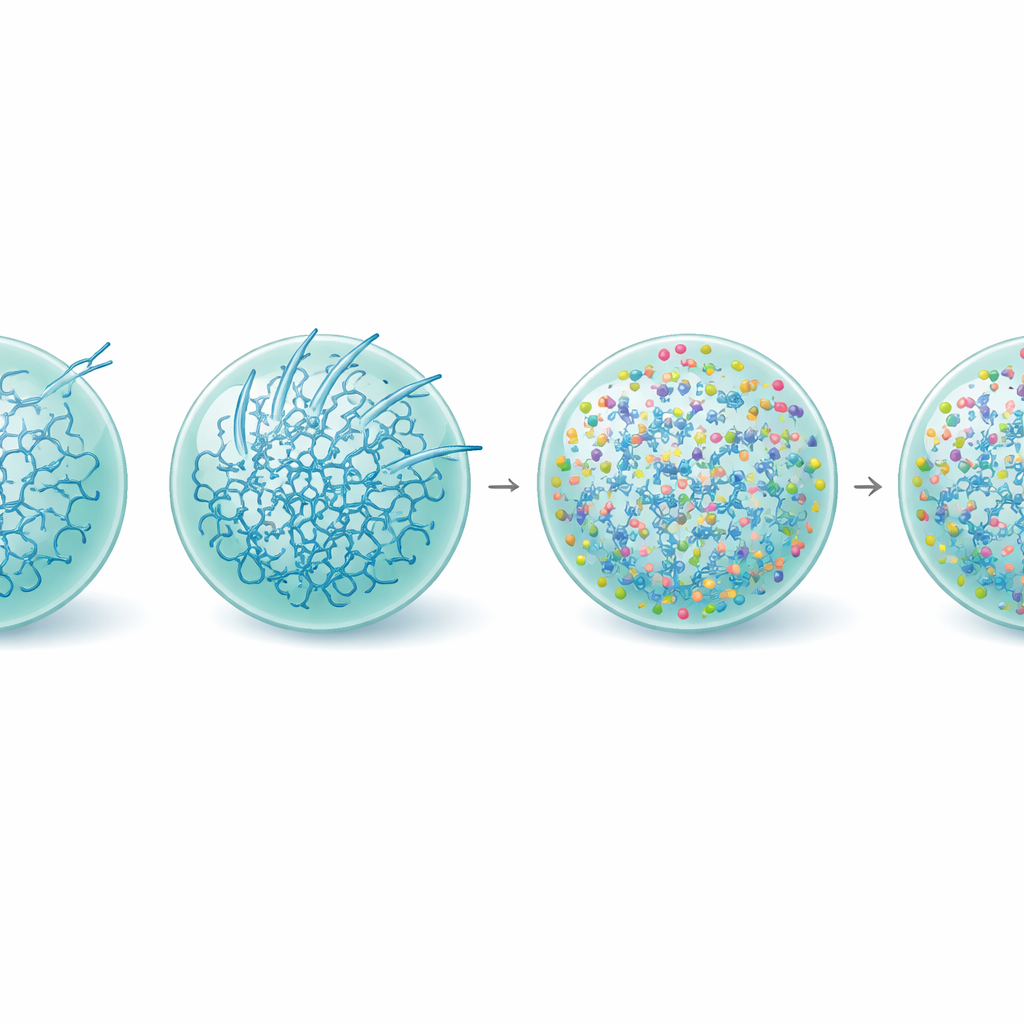
Usztywnienie kropli, uratowanie funkcji
Dążąc dalej, zespół zbadał, jak L-arginina przekształca wewnętrzne życie kropli Tau. Pomiary struktury białka pokazały, że w obecności L-argininy odsetek cząsteczek Tau przyjmujących sztywne, beta-bogate formy związane z amyloidem był zmniejszony, nawet w starszych kroplach. Nanoreologia w oparciu o wideo — śledzenie ruchu malutkich kulek wewnątrz kondensatów — ujawniła, że L-arginina faktycznie uczyniła krople Tau bardziej viskoelastycznymi, co oznacza, że ich wewnętrzna sieć stała się silniejsza i bardziej powiązana, zachowując jednocześnie płynną naturę. To wzmocnienie wydaje się utrzymywać układ w metastabilnym, funkcjonalnym stanie i zwiększać barierę energetyczną dla formowania włókien, szczególnie na powierzchni kropli. Zgodnie z tym, kondensaty traktowane L-argininą nadal równomiernie rekrutowały tubulinę i wspierały wzrost mikrotubul długo po tym, jak nieleczone krople przestały być aktywne.
Co to oznacza dla przyszłych terapii
Praca demonstruje, że siły napędzające tworzenie kropli białkowych i te napędzające tworzenie szkodliwych włókien są powiązane, ale rozłączne. Poprzez dostrojenie chemii wewnątrz kondensatów za pomocą metabolitu takiego jak L-arginina, możliwe jest zachowanie korzystnego, płynnego stanu przy jednoczesnym opóźnieniu lub zapobieganiu przejściu do powiązanych z chorobą włókien amyloidowych. Chociaż badanie wykorzystuje specjalnie zaprojektowany układ Tau in vitro, daje dowód zasady: małe cząsteczki, które selektywnie wzmacniają stabilność kondensatów, mogą pewnego dnia pomóc chronić komórki przed stopniowym gromadzeniem toksycznych agregatów białkowych, nie blokując przy tym normalnych, organizujących ról biomolekularnych kondensatów.
Cytowanie: Mahendran, T.S., Singh, A., Srinivasan, S. et al. Decoupling phase separation and fibrillization preserves activity of biomolecular condensates. Nat Commun 17, 2841 (2026). https://doi.org/10.1038/s41467-026-69244-z
Słowa kluczowe: białko Tau, biomolekularne kondensaty, włókna amyloidowe, L-arginina, neurodegeneracja