Clear Sky Science · pl
Mikro- i nanodomeny glikokaliksu w interakcjach komórka–komórka i komórka–macierz ujawnione dzięki ulepszonej chemii „click”
Jak komórki noszą cukrową powłokę
Każda komórka w naszym ciele jest otoczona cienką, bogatą w cukry warstwą zwaną glikokaliksem. Ta cukrowa powłoka pomaga komórkom wyczuwać otoczenie, przyczepiać się do sąsiadów lub ich odpychać, a także czasem unikać układu odpornościowego. W nowotworach powłoka ta często staje się grubsza i bardziej chaotyczna, co może sprzyjać wzrostowi i rozprzestrzenianiu się guza. Opisane tu badanie opracowuje ostrzejszą metodę obserwacji tej powłoki na żywych komórkach i ujawnia, że zamiast gładkiej osłony jest ona pełna drobnych szczelin i małoskalowych przerw dokładnie tam, gdzie komórki stykają się ze sobą i z otaczającą tkanką.
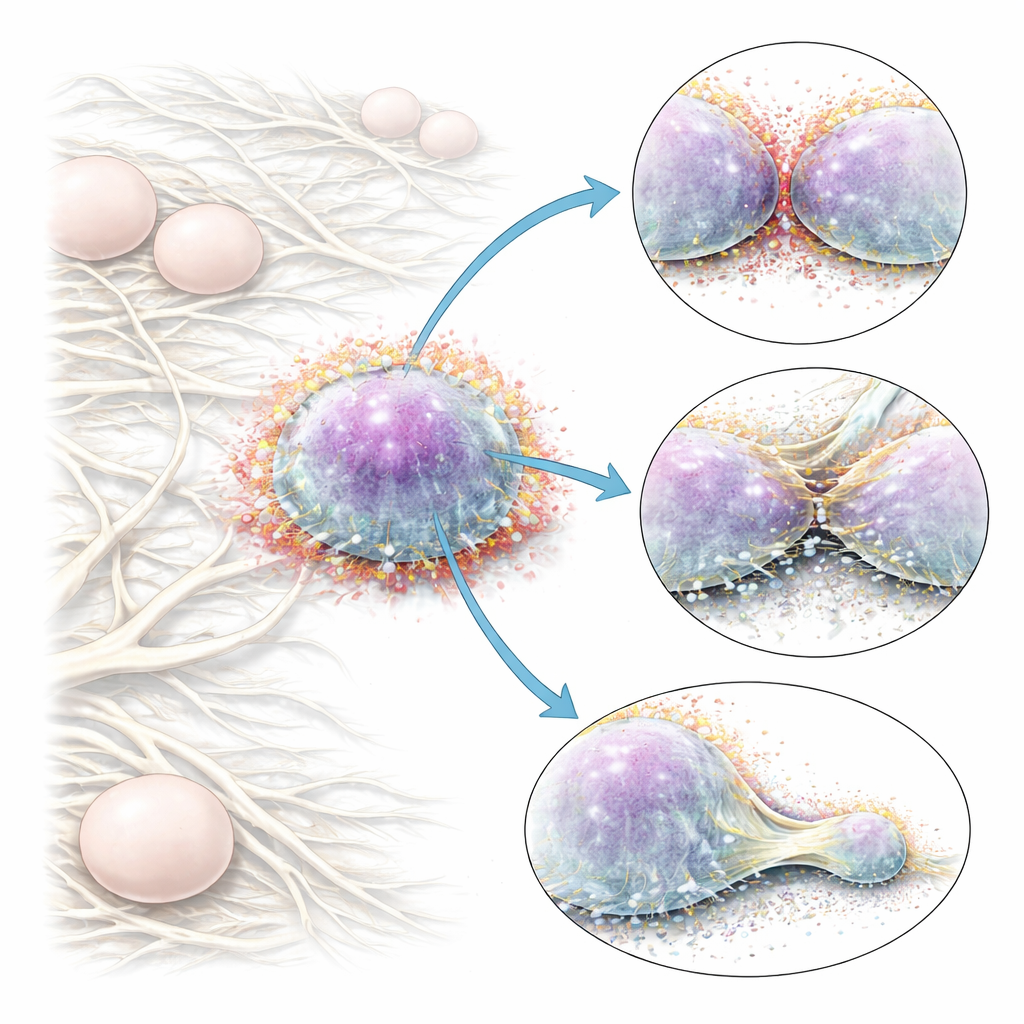
Nowy sposób rozświetlania cukrowej powłoki
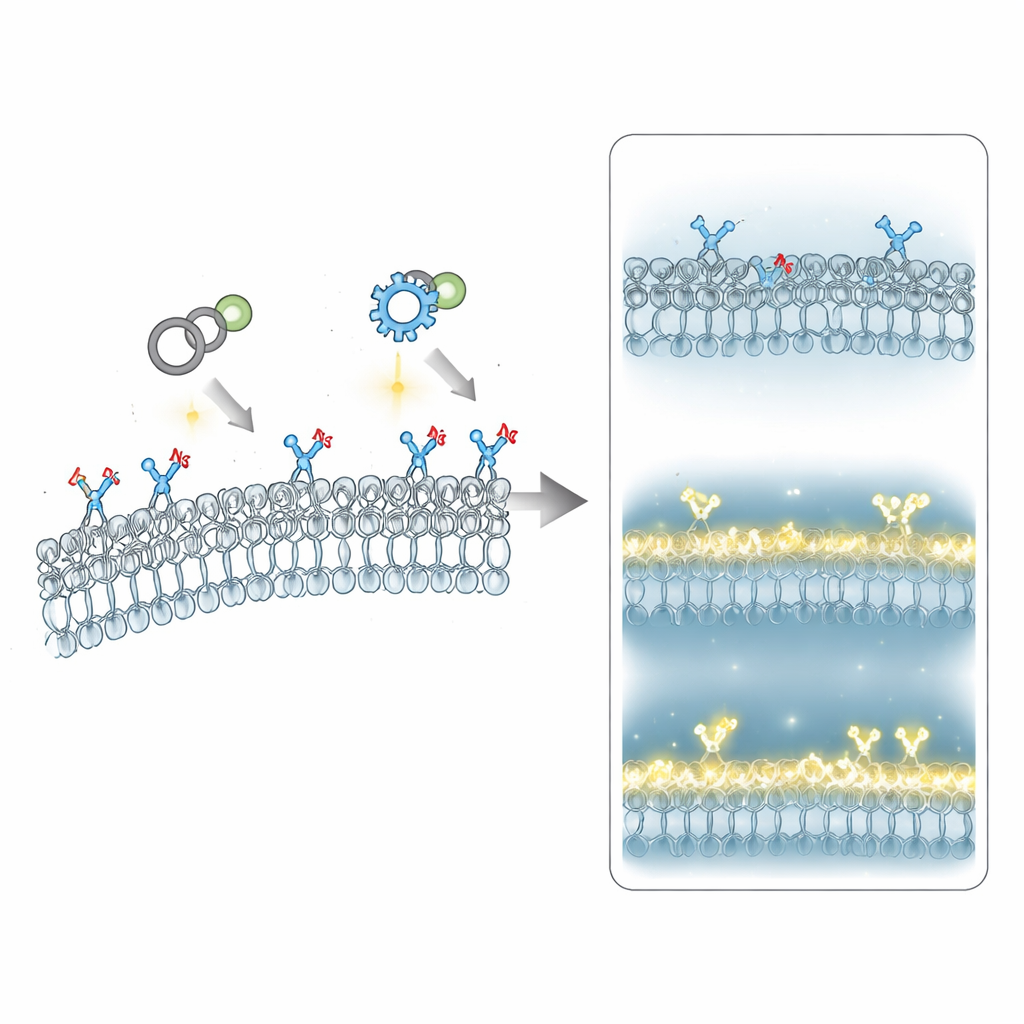
Tradycyjne metody wizualizacji glikokaliksu opierają się na przeciwciałach lub naturalnych białkach wiążących cukry. Te narzędzia mogą przyciągać związane molekuły, zbijać je w agregaty albo przeoczyć obszary o słabym sygnale. Autorzy zastosowali zamiast tego dwustopniową strategię „chemicznego znakowania”: komórkom nowotworowym podaje się najpierw nieszkodliwy budulec cukrowy z maleńkim uchwytem chemicznym. Komórki naturalnie wbudowują ten zmieniony cukier w swoją powłokę. W drugim kroku fluorescencyjny czujnik łączy się z tym uchwytem poprzez wysoce selektywną reakcję „click”. Zespół zastąpił powszechnie używany detektor click (DBCO) nowszym, siedmioczłonowym pierścieniowym sondem znanym jako THS, który reaguje szybciej i lepiej rozpuszcza się w wodzie. Ponieważ THS jest bardziej reaktywny i mniej „przylepny” wobec błon, znakowany jest większy obszar glikokaliksu, sygnały są jaśniejsze, a szum tła niski — wszystko to bez mierzalnego stresu czy uszkodzeń komórek.
Widzenie drobniejszych detali na żywych komórkach
Dzięki temu ulepszonemu znakowaniu, w połączeniu z mikroskopią wysokiej rozdzielczości Airyscan, badacze mogą mapować glikokaliks komórek nowotworowych na skalach mikro- i nano, gdy komórki są żywe. Potwierdzają, że ich metaboliczny znacznik oznacza większość głównych składników powłoki cukrowej, z wyjątkiem zewnętrznej warstwy jednego długiego łańcucha cukru (kwasu hialuronowego). W porównaniu ze starszą sondą THS ujawnia większy odsetek komórek z intensywnie znakowaną powłoką i poprawia stosunek sygnału do tła wielokrotnie, szczególnie w przypadku drobnych cech, takich jak pęcherzyki błonowe (bleby). Ta poprawa sprawia, że subtelne zmiany gęstości glikokaliksu, które wcześniej były zbyt słabe lub zaszumione, stają się teraz widoczne jako wyraźne wzory na powierzchni komórki.
Ukryte przerwy tam, gdzie komórki stykają się ze sobą i z macierzą
Wykorzystując te ostrzejsze obrazy, zespół bada, jak powłoka cukrowa zachowuje się w miejscach styku komórek z innymi komórkami oraz z otaczającym rusztowaniem włókien zwanym macierzą zewnątrzkomórkową. Na pierwszy rzut oka powłoka wydaje się dość równomierna na wolnych powierzchniach komórek. Jednak w strefach kontaktu między komórkami sygnał jest niższy niż oczekiwano, gdyby dwie niezmienione powłoki po prostu na siebie nachodziły, a od tych stref odchodzą delikatne gradienty. Pomiary szybkości odzyskiwania fluorescencji po wybieleniu wskazują, że cząsteczki cukrów poruszają się szybciej w tych rejonach, co jest zgodne z dynamicznym przerzedzaniem powłoki w miarę ściskania się komórek. W trójwymiarowych żelach kolagenowych imitujących miękką tkankę komórki nowotworowe wysuwają wypustki czołowe, bleby i długie włókna retrakcyjne podczas migracji. Wzdłuż tych struktur glikokaliks stopniowo przerzedza się ku końcom, czasem na przestrzeni wielu mikrometrów, tworząc obszary o niskiej zawartości cukru dokładnie tam, gdzie komórka naciska na lub ciągnie macierz. Na jeszcze mniejszych skalach, gdzie komórki obejmują pojedyncze włókna kolagenu, klastry białek adhezyjnych zwanych integrynami siedzą nieco na zewnątrz bogatszej wewnętrznej warstwy glikokaliksu, tworząc nanodomeny o wysokiej zawartości integryn i niskiej zawartości cukru obok obszarów bogatszych w cukry.
Dlaczego bezcukrowe plamy mają znaczenie dla komórek nowotworowych
Te obserwacje sugerują, że komórki nowotworowe nie noszą po prostu jednolicie grubej powłoki cukrowej; aktywnie ją kształtują. Lokalne przerzedzenie glikokaliksu na stykach komórka–komórka i w punktach uchwytu włókien kolagenowych może zmniejszać fizyczne zagęszczenie wokół kluczowych receptorów, ułatwiając tym receptorom wiązanie partnerów i przekazywanie sił mechanicznych. W wypustkach czołowych obniżona gęstość cukrów wydaje się iść w parze z silniejszym agregowaniem integryn, co potencjalnie zwiększa zdolność komórki do zaczepiania się i ciągnięcia za otaczające włókna. W blebach i włóknach retrakcyjnych gradienty powłoki współgrają z szybkim przepływem błony i ciśnieniem wewnętrznym, ponownie wskazując na dynamiczne przebudowywanie, a nie statyczną powłokę. Ogólnie praca pokazuje, że bardziej czuła „chemiczna latarka” — chemia click oparta na THS — może odsłonić mikro- i nano-wielkościowe „nagie miejsca” w powłoce cukrowej, które prawdopodobnie mają kluczowe znaczenie dla sposobu, w jaki komórki nowotworowe komunikują się, przylegają i poruszają się przez trójwymiarową tkankę.
Cytowanie: Smits, D., Damen, J.A.M., Li, T. et al. Glycocalyx micro- and nanodomains in cell-cell and cell-matrix interactions revealed by enhanced click chemistry. Nat Commun 17, 2645 (2026). https://doi.org/10.1038/s41467-026-69242-1
Słowa kluczowe: glikokaliks, chemia click, migracja komórek, komórki nowotworowe, adhezja komórek