Clear Sky Science · pl
Warianty FOXJ3 związane z padaczką łączą program transkrypcyjny szlaku PTEN–mTOR z określaniem losu neuronów i laminacją kory
Kiedy okablowanie mózgu delikatnie zbacza z kursu
Padaczka często zaczyna się w dzieciństwie, ale u wielu młodych pacjentów badania obrazowe nie wykazują niczego oczywiście nieprawidłowego. To badanie zajmuje się jedną ukrytą przyczyną: niewielkimi zmianami w genie FOXJ3, które po cichu przekształcają sposób, w jaki zbudowana jest zewnętrzna warstwa mózgu, kora. Śledząc działanie tego genu w rodzinach z ogniskową padaczką i w rozwijających się mózgach myszy, badacze pokazują, jak wczesne potknięcia przy narodzinach komórek, ich przemieszczaniu i układaniu warstw mogą ostatecznie prowadzić do napadów.
Drobna malformacja stojąca za trudnymi do leczenia napadami
Wiele dzieci z lekooporną ogniskową padaczką ma schorzenie zwane ogniskową dysplazją korową (FCD), w którym fragmenty kory są nieprawidłowo ukształtowane. Te obszary zawierają przesunięte i nieprawidłowo powiększone komórki nerwowe i są częstą przyczyną, dla której leki nie kontrolują napadów. Jednak molekularna przyczyna FCD często pozostaje nieznana, a standardowe MRI może nie wykryć małych lub płytkich defektów. Autorzy rozpoczęli od rodziny, w której kilku członków miało ogniskową padaczkę i objawy FCD. Dokładna analiza genomu wskazała na rzadkie zmiany w FOXJ3, genie wcześniej niepowiązanym z padaczką. Dodatkowe przypadki z dużych baz genetycznych ujawniły więcej osób z nietypowymi wariantami FOXJ3 i napadami ogniskowymi, co sugeruje, że gen ten może być powtarzającym się graczem w takich zaburzeniach.
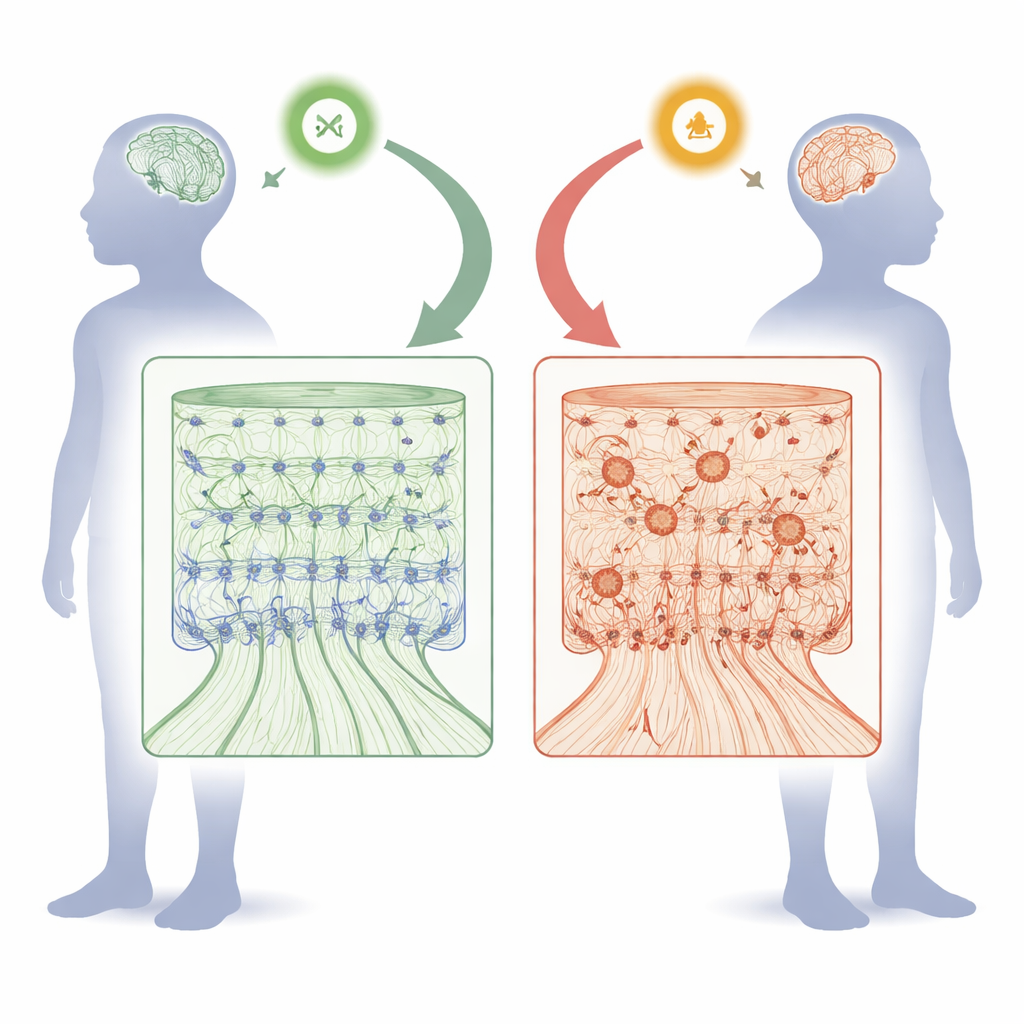
Jak FOXJ3 pomaga kształtować powierzchnię myślenia mózgu
W trakcie rozwoju płodowego kora jest składana jak wielopiętrowy budynek. Komórki macierzyste wyściełające wewnętrzną powierzchnię mózgu dzielą się, a następnie wysyłają nowo powstałe neurony na zewnątrz wzdłuż radialnych „rusztowań”, by utworzyć sześć uporządkowanych warstw. Zespół odkrył, że FOXJ3 jest aktywny zarówno w tych progenitorach przypominających komórki macierzyste, jak i w młodych neuronach, ale jego aktywność w progenitorach naturalnie spada po określonym punkcie w połowie ciąży. Używając narzędzi do wyciszania genów w embrionach myszy, badacze obniżyli poziomy Foxj3 na różnych etapach i obserwowali skutki. Wczesna utrata Foxj3 spowodowała, że nowo powstałe neurony migrowały wolniej i osiadały w niewłaściwych warstwach. Komórki, które powinny stać się neuronami warstw głębokich, zamiast tego przyjmowały tożsamość typową dla warstw górnych, a neurony projekcyjne spoidła, łączące dwie półkule mózgu, powstawały w nadmiarze. Jednak później w rozwoju zmniejszenie Foxj3 miało znacznie łagodniejsze efekty, co pokazuje, że jego rola jest silnie zależna od czasu.
Utrzymanie równowagi między podziałem a wzrostem komórek
Aby zrozumieć, dlaczego FOXJ3 ma taki wpływ, badacze połączyli kilka podejść na dużą skalę. Mapowali miejsca wiązania FOXJ3 na DNA oraz które geny są aktywne w tysiącach pojedynczych komórek kory. Wskazało to wyraźnie na geny kontrolujące cykl komórkowy i wzrost mózgu, w szczególności PTEN — główny hamulec szlaku wzrostu znanego jako mTOR. W komórkach progenitorowych wiązanie FOXJ3 podnosiło aktywność PTEN, co z kolei pomagało komórkom wychodzić z cyklu podziałów, przekształcać się w neurony i migrować na zewnątrz w uporządkowany sposób. Gdy Foxj3 został wyciszony, więcej progenitorów pozostawało w stanie dzielenia się, mniej wychodziło z cyklu na czas, a migracja zatrzymywała się w strefach pośrednich. Co kluczowe, przywrócenie poziomów PTEN w mózgach pozbawionych Foxj3 w dużej mierze odwróciło problemy z migracją, laminacją i losem komórek, podczas gdy zwiększenie innego regulatora wzrostu, TSC1, tego nie zrobiło. To umieszcza PTEN w centrum kontroli FOXJ3 nad budową kory.
Od zaburzonych szlaków do powiększonych neuronów
Zespół zapytał następnie, jak zachowują się warianty FOXJ3 podobne do spotykanych u pacjentów. Wersja FOXJ3 związana z chorobą nie podnosiła poziomów PTEN i pozwalała na nadmierną aktywność szlaku mTOR, co było widoczne poprzez wzrost fosforylacji kluczowego białka związanego ze wzrostem. U młodocianych myszy zaprojektowanych tak, by wyrażać ten mutant w rozwijającej się korze, neurony później wyglądały wyraźnie spuchnięte, z większymi ciałami i obwodami komórek, naśladując dysmorficzne komórki obserwowane w ludzkim FCD. Mimo to białko mutantowe wciąż prawidłowo docierało do jądra, co wskazuje, że problem leży w wadliwej regulacji genów, a nie w niewłaściwym lokalizowaniu. Razem te obserwacje łączą mutacje FOXJ3 z kaskadą zdarzeń — mniej PTEN, więcej sygnalizacji mTOR, opóźnione wychodzenie z cyklu komórkowego, pomieszana migracja i hipertroficzne neurony — które mogą tworzyć podłoże dla sieci epilptycznych.
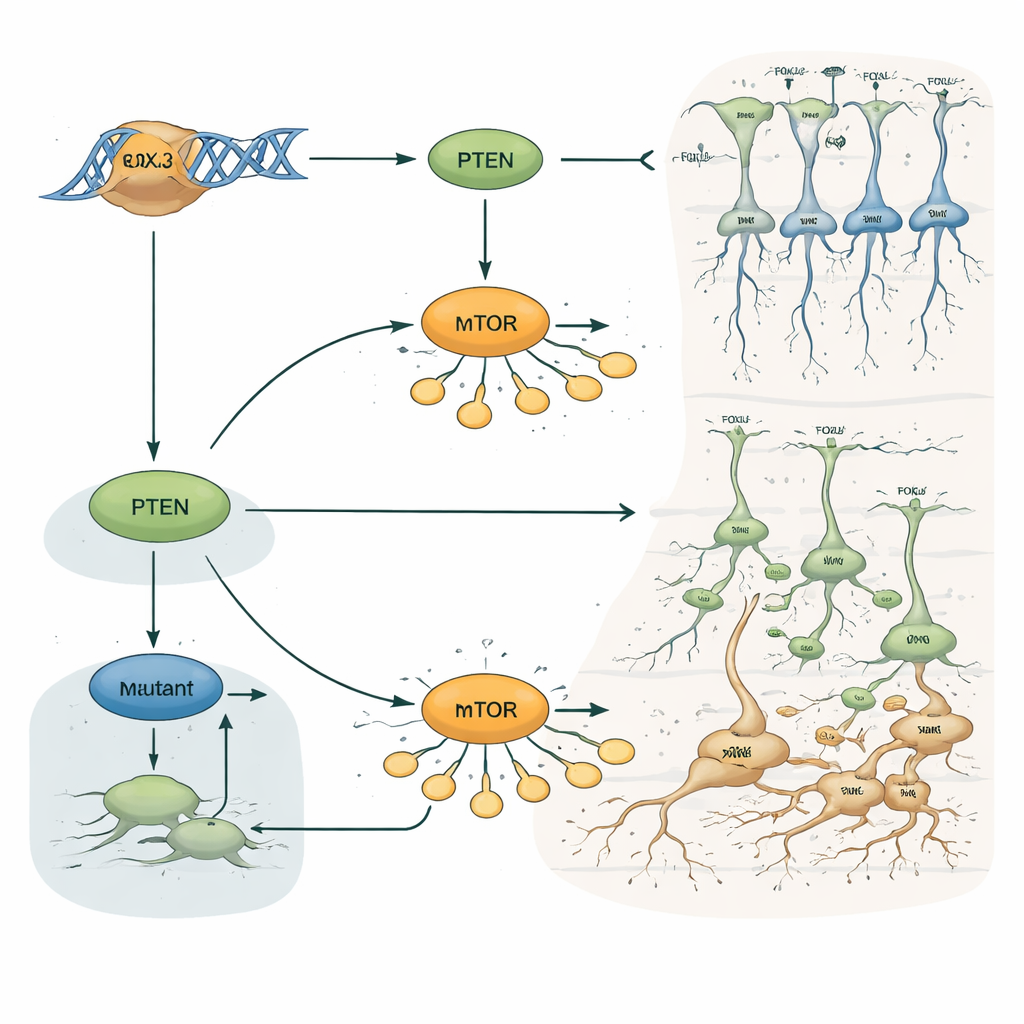
Dlaczego to ma znaczenie dla padaczki i ukrytych zmian w mózgu
Dla osoby niebędącej specjalistą kluczowy przekaz jest taki, że pojedynczy czynnik transkrypcyjny, FOXJ3, pomaga decydować, kiedy i gdzie rodzą się neurony kory, jak się poruszają i którą warstwę ostatecznie zajmują. Działając przez szlak wzrostu PTEN–mTOR, FOXJ3 utrzymuje harmonogram „budowy” mózgu. Rzadkie zmiany w tym genie mogą zachwiać tę równowagę, powodując małe ogniska nieprawidłowo ukształtowanej kory, nawet gdy badania MRI wydają się normalne. Ta praca nie tylko proponuje FOXJ3 jako nową przyczynę genetyczną ogniskowej dysplazji korowej i padaczki, ale także ilustruje, jak subtelne przesunięcia we wczesnym rozwoju mózgu mogą odbijać się dekady później jako trudne do leczenia napady.
Cytowanie: Cheng, HY., Liu, C., Nien, CW. et al. Epilepsy-associated FOXJ3 variants link a transcriptional program of the PTEN-mTOR pathway to neuronal specification and cortical lamination. Nat Commun 17, 1815 (2026). https://doi.org/10.1038/s41467-026-69241-2
Słowa kluczowe: ogniskowa dysplazja korowa, gen FOXJ3, szlak PTEN mTOR, rozwój kory, ogniskowa padaczka