Clear Sky Science · pl
Podstawa molekularna galaktozylacji kolagenu przez GLT25D1
Jak malutkie znaczniki cukrowe pomagają budować mocne tkanki
Kolagen to najpowszechniejsze białko w organizmie, tworzące rusztowanie dla skóry, kości, naczyń krwionośnych i wielu innych tkanek. Jednak kolagen nie działa samodzielnie: musi być ozdobiony małymi cząsteczkami cukru w precyzyjnych miejscach, by zyskać właściwą wytrzymałość i elastyczność. W tym badaniu ukazano, z detalami atomowymi, jak jeden kluczowy enzym, GLT25D1, przyłącza określony cukier do kolagenu i jak zaburzenia tego procesu mogą prowadzić do kruchej struktury naczyń, problemów mięśniowych, a być może nawet raka.
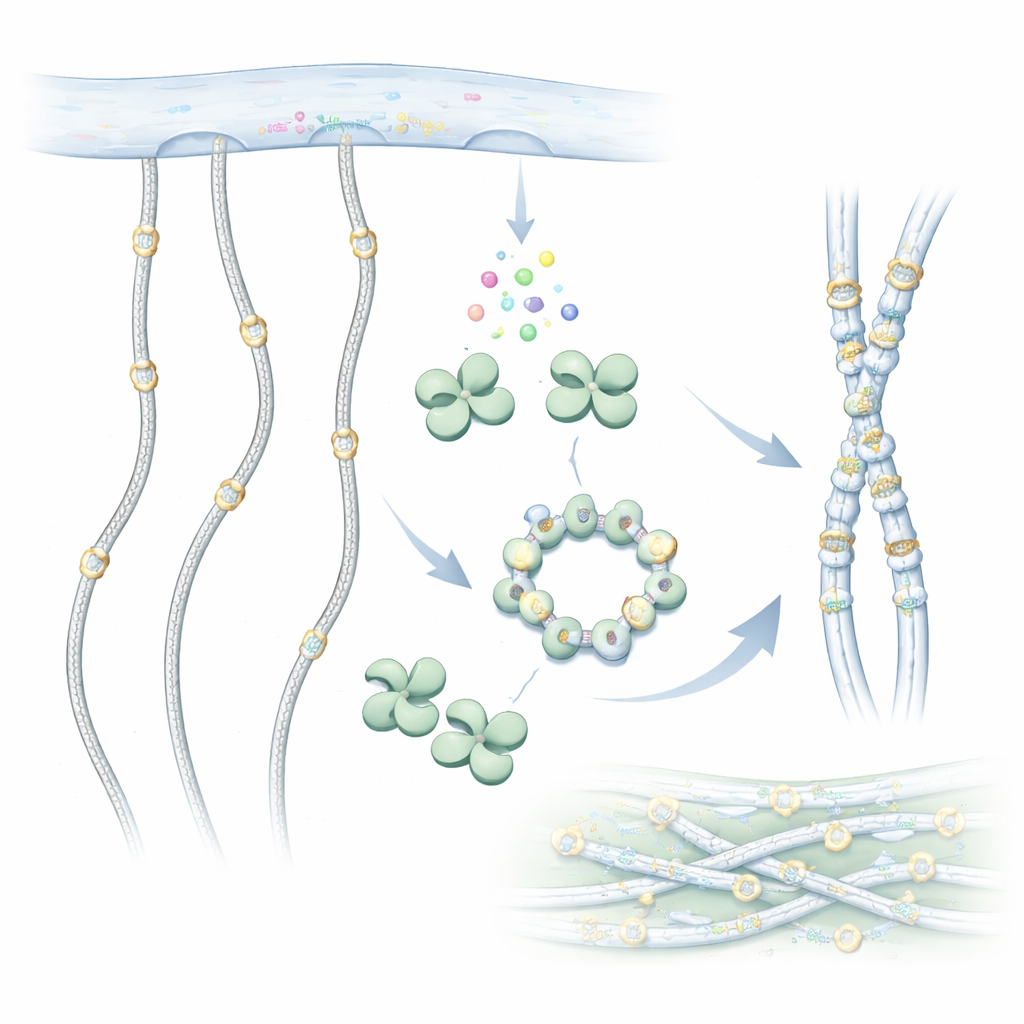
Bliższe spojrzenie na ukrytą metamorfozę kolagenu
Cząsteczki kolagenu to długie, przypominające liny łańcuchy, które poza komórkami grupują się w trwałe włókna. Zanim jednak opuszczą komórkę, są chemicznie modyfikowane. Jedną z ważnych modyfikacji jest dodanie grup cukrowych do specjalnych reszt zwanych hydroksylizynami wzdłuż łańcucha kolagenu. GLT25D1 przeprowadza pierwszy etap tego znakowania cukrowego, przenosząc cząsteczkę galaktozy z donora na hydroksylizynę. To cukrowe „upiększanie” jest zachowane od prostych zwierząt po ludzi i pomaga kolagenowi prawidłowo się fałdować, wchodzić w interakcje z komórkami i opierać się zużyciu.
Odkrycie kształtu dekoratora kolagenu
Aby zrozumieć, jak działa GLT25D1, badacze wykorzystali krio‑mikroskopię elektronową, aby zobrazować ludzki enzym w niemal atomowej rozdzielczości. Odkryli, że każda cząsteczka GLT25D1 ma dwie podobne płaty, oba związane z powszechnym fałdem enzymatycznym spotykanym w białkach przenoszących cukry. Te płaty łączą się, tworząc wydłużone dimery, a trzy dimery mogą dalej składać się w heksamer w kształcie pierścienia. W takich zespołach prawdziwymi pracownikami są centra katalityczne — usytuowane daleko od siebie, co może pozwalać na jednoczesne działanie kilku miejsc dodających cukier wzdłuż rozciągniętego łańcucha kolagenu.
Części robocze: gdzie naprawdę zachodzi transfer cukru
Zespół rozwiązał struktury GLT25D1 związane zarówno z donorowym cukrem, jak i z krótkim peptydem przypominającym kolagen zawierającym hydroksylizynę. Ten trójskładnikowy kompleks pokazał, że tylko drugi płat, zwany domeną C‑terminalną, rzeczywiście przeprowadza reakcję chemiczną. Tam cząsteczka donora mieści się w kieszeni stabilizowanej przez jon metalu, podczas gdy peptyd leży w wąskim rowku wymuszającym specyficzny lokalny wzorzec: hydroksylizyna bezpośrednio po niej ma maleńką glicynę. Pojedyncze reszta asparaginianu działa jako zasada chemiczna, aktywując grupę hydroksylową hydroksylizyny tak, by mogła ona zaatakować cukier i zakończyć transfer. Zmiany w dowolnym z tych kluczowych aminokwasów drastycznie obniżają lub znoszą aktywność, potwierdzając ich niezbędną rolę.
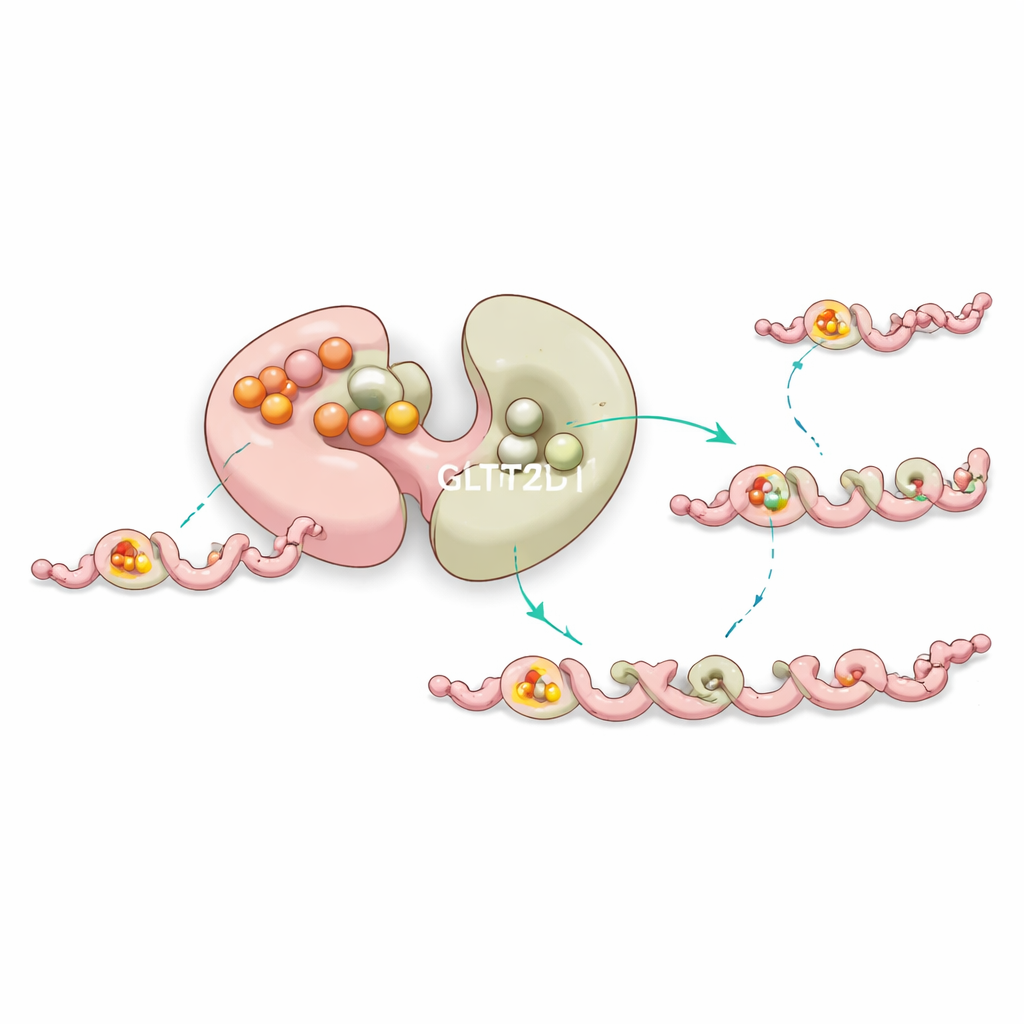
Wbudowany stabilizator i kontrola na odległość
Ciekawie, pierwszy płat GLT25D1 wiąże donor cukru bardzo mocno, ale nie przeprowadza transferu. Zamiast tego eksperymenty i symulacje komputerowe sugerują, że to „nieme” miejsce pomaga stabilizować enzym i subtelnie stroić zachowanie aktywnego płata poprzez komunikację na daleki zasięg w obrębie białka. Mutacje w pobliżu tej niekatalitycznej kieszeni często destabilizują enzym lub przesuwają jego wydajność, co sugeruje, że natura wykorzystuje to dodatkowe miejsce wiążące jako formę wewnętrznej kontroli jakości, by utrzymać modyfikację kolagenu w sprawnym trybie.
Kiedy dekorator zawodzi: powiązania z chorobami
Mapując mutacje pochodzące od pacjentów na ich model strukturalny, autorzy mogli wyjaśnić, jak błędy w GLT25D1 prowadzą do chorób u ludzi. Niektóre mutacje obcinają całą domenę katalityczną, inne destabilizują rdzeń białka, a jeszcze inne uderzają bezpośrednio w miejsca wiążące cukier lub kolagen. Te defekty zmniejszają lub eliminują dodawanie cukru do kolagenu i powiązano je z chorobami małych naczyń mózgu, problemami poznawczymi oraz wadami mięśniowo‑szkieletowymi. Mutacje związane z rakiem także skupiają się w kluczowych obszarach, co sugeruje, że zmienione dekorowanie kolagenu może wpływać na wzrost i rozprzestrzenianie się nowotworu.
Dlaczego to ma znaczenie dla zdrowia i przyszłych terapii
Przedstawiając szczegółowy trójwymiarowy plan działania GLT25D1, ta praca wyjaśnia, jak precyzyjne znaczniki cukrowe są dodawane do kolagenu i dlaczego ten etap jest tak ważny dla integralności tkanek. Dla odbiorców niebędących specjalistami kluczowy wniosek jest taki, że drobne zmiany chemiczne w kolagenie mogą mieć ogromne konsekwencje dla naczyń krwionośnych, kości, a być może także ryzyka nowotworowego. Mapę strukturalną GLT25D1 można teraz wykorzystać jako przewodnik do diagnozowania szkodliwych wariantów oraz projektowania terapii — od małych cząsteczek stabilizujących wadliwe enzymy po strategie oparte na genach — które w przyszłości mogłyby korygować defekty znakowania cukrowego kolagenu u źródła.
Cytowanie: Sun, H., Zhang, M., Shi, Y. et al. Molecular basis of collagen galactosylation by GLT25D1. Nat Commun 17, 2426 (2026). https://doi.org/10.1038/s41467-026-69234-1
Słowa kluczowe: glikozylacja kolagenu, GLT25D1, macierz zewnątrzkomórkowa, choroba naczyń, struktura cryo-EM