Clear Sky Science · pl
Niedobór sklerostyny uczula białe adipocyty na sygnały termogeniczne indukujące beiging u myszy
Dlaczego rozgrzewanie tłuszczu może chłodzić choroby
Większość z nas traktuje kość i tłuszcz jako oddzielne światy: jedna daje strukturę, drugi magazynuje energię. Badanie na myszach pokazuje, że kość i tłuszcz prowadzą stałą chemiczną rozmowę, a białko produkowane przez komórki kostne może decydować, czy nasz „biały” tłuszcz pozostaje zwykłym magazynem kalorii, czy przekształca się w bardziej aktywny, spalający kalorie tłuszcz „beżowy”. Zrozumienie tego ukrytego dialogu może otworzyć nowe możliwości jednoczesnego zwalczania otyłości, cukrzycy i utraty masy kostnej.
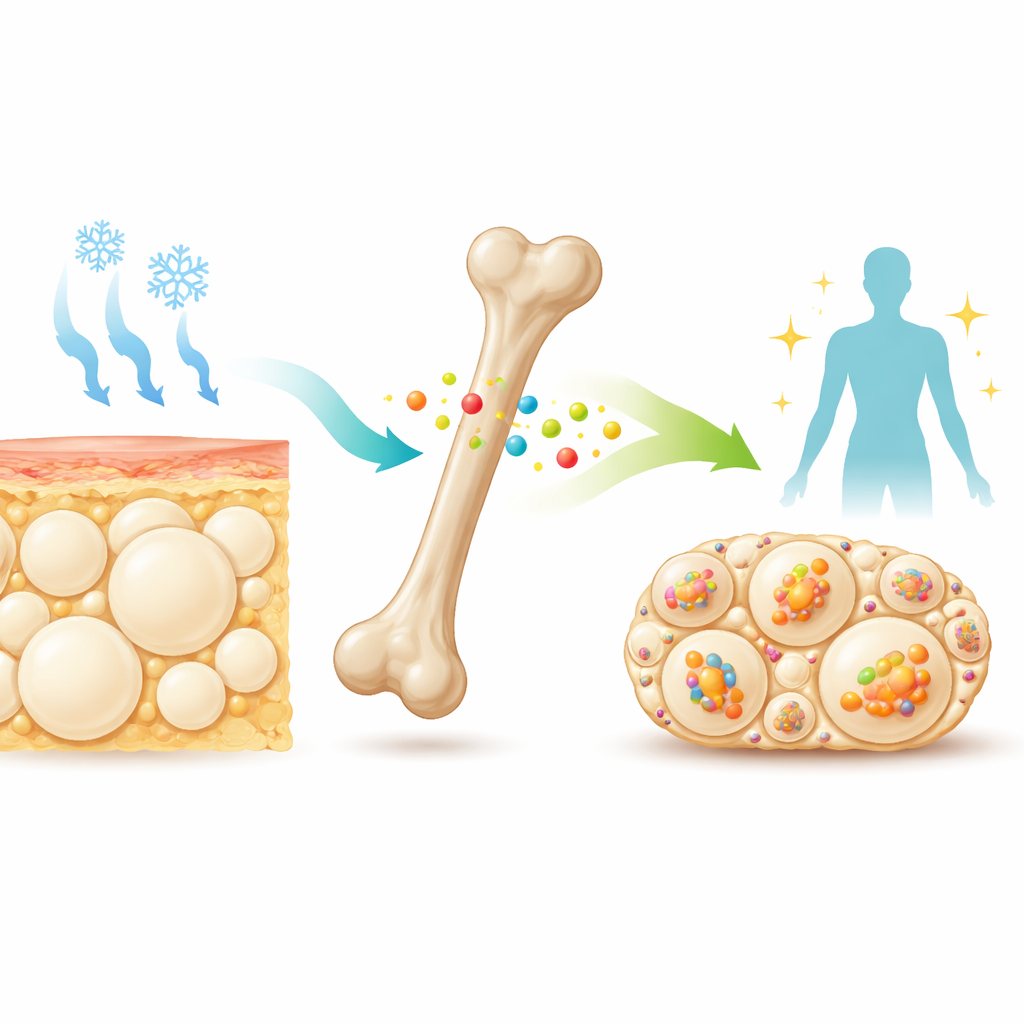
Cichy posłaniec z kości
Głęboko wewnątrz kości wyspecjalizowane komórki uwalniają do krwi niewielkie białko zwane sklerostyną. Lekarze już celują w sklerostynę lekami, by wzmacniać kości u pacjentów zagrożonych złamaniami. Wcześniejsze prace wykazały, że myszy pozbawione sklerostyny są nie tylko bardzo silne kostnie, ale też szczuplejsze i bardziej wrażliwe na insulinę. Ich podskórny tłuszcz, zwłaszcza w okolicy bioder (inguinalny biały tłuszcz), zawiera drobne, wielokomorowe komórki tłuszczowe przypominające tłuszcz beżowy, który może spalać paliwo, by wytwarzać ciepło. Te wskazówki skłoniły badaczy do pytania, czy sklerostyna normalnie działa jako hamulec zdolności organizmu do konwertowania białego tłuszczu w beżowy w odpowiedzi na zimno lub na leki naśladujące sygnały nerwowe do tłuszczu.
Sygnały zimna, sygnały z kości i zapłon tłuszczu
Zespół poddał normalne myszy oraz myszy pozbawione genu sklerostyny (Sost-/-) działaniu leku aktywującego konkretny receptor w komórkach tłuszczowych (receptor β3-adrenergiczny) albo łagodnemu zimnu. U zwierząt kontrolnych te sygnały termogeniczne zwiększały produkcję sklerostyny w kości i podnosiły jej poziom we krwi. Wzrost ten wiązał się z utratą gąbczastej tkanki kostnej, ale tylko z umiarkowanymi zmianami w podskórnym tłuszczu. Natomiast myszy pozbawione sklerostyny wykazywały znacznie silniejszą odpowiedź: ich tłuszcz inguinalny pobierał więcej glukozy, uwalniał więcej kwasów tłuszczowych, kurczył się i wypełniał komórkami przypominającymi beżowe, bogatymi w mitochondria — elektrownie komórkowe. Kluczowe geny termogeniczne włączały się silniej u tych myszy, szczególnie w tłuszczu podskórnym, podczas gdy klasyczny tłuszcz brunatny pozostawał w dużej mierze niezmieniony.
Dostrajanie spalania tłuszczu przez wspólny przełącznik
Aby zrozumieć, jak sklerostyna sprawuje tę kontrolę, badacze skupili się na β-kateninie, białku zaangażowanym w szlak sygnalizacyjny Wnt, który sklerostyna zwykle hamuje w kości. W tłuszczu aktywacja β-kateniny po urodzeniu przesuwała białe komórki w stronę stanu przypominającego beżowy i zwiększała ich reakcję na sygnały β3-adrenergiczne, ale efekt ten znikał, gdy myszy przebywały w cieple, w warunkach termoneutralnych, kiedy organizm nie potrzebuje dodatkowego ciepła. Odwrotnie, usunięcie β-kateniny specyficznie w komórkach tłuszczowych myszy pozbawionych sklerostyny znosiło ich tłuszcz beżowy, przywracało większe białe adipocyty i odwracało poprawę poziomów insuliny i kwasów tłuszczowych. Te eksperymenty sugerują, że gdy sklerostyna jest niska, β-katenina w komórkach tłuszczowych staje się ważną wewnętrzną dźwignią, która czyni biały tłuszcz bardziej podatnym na sygnały termogeniczne.
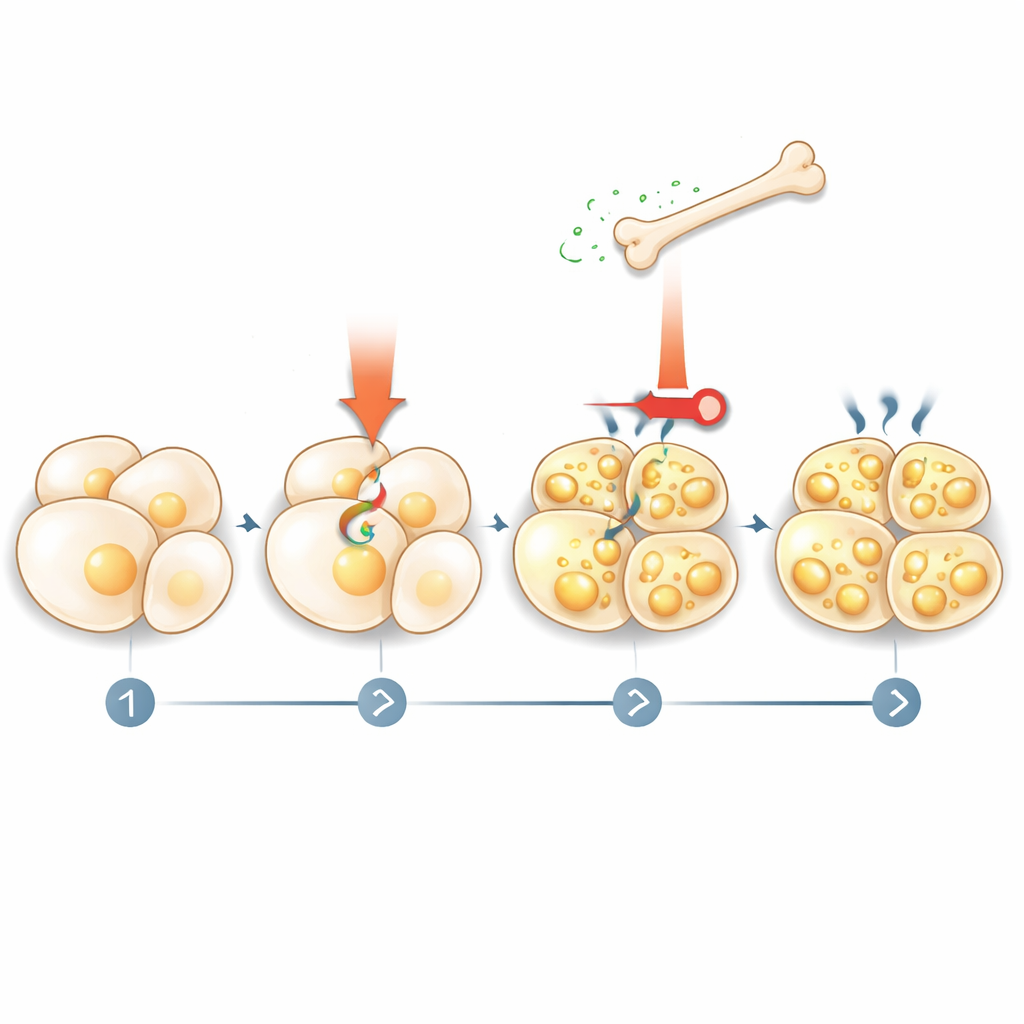
Jak tłuszcz odzywa się do kości
Historia nie kończyła się na tym, że kość mówi tłuszczowi, co ma robić. Zespół odkrył, że stymulacja termogeniczna aktywuje rozkład tłuszczu (lipolizę), uwalniając kwasy tłuszczowe do krwi. Te kwasy tłuszczowe działają następnie na komórki kostne przez receptor jądrowy zwany PPARγ, zwiększając produkcję sklerostyny. Gdy badacze zablokowali lipolizę w komórkach tłuszczowych lub usunęli PPARγ z komórek kostnych, leki naśladujące zimno nie podnosiły już poziomu sklerostyny. To ujawnia pętlę sprzężenia zwrotnego: sygnały termogeniczne powodują, że tłuszcz uwalnia paliwo; to paliwo instruuje kość do wydzielania więcej sklerostyny; a sklerostyna z kolei hamuje dalszą aktywację tłuszczu i beiging.
Łączenie leków na kość i tłuszcz dla zdrowia metabolicznego
Na koniec badacze sprawdzili, czy przerwanie tej pętli może pomóc w modelu chorobowym. Otyłe myszy na diecie wysokotłuszczowej otrzymały niską dawkę mirabegronu (leku β3-adrenergicznego stosowanego już w problemach z pęcherzem), przeciwciało neutralizujące sklerostynę (romosozumab, zatwierdzony w leczeniu osteoporozy) lub oba środki jednocześnie. Podczas gdy każdy z leków osobno dawał umiarkowane efekty, połączenie zmniejszyło masę tłuszczu w kluczowych depozytach, przesunęło skład tłuszczu w stronę mniejszych, bardziej aktywnych komórek, obniżyło insulinę, trójglicerydy i cholesterol oraz zachowało wytrzymałość kości. Ciepłe warunki chowu, które zmniejszają zapotrzebowanie organizmu na ciepło, w dużej mierze niwelowały korzyści metaboliczne związane z utratą sklerostyny, podkreślając, że ta ścieżka ma znaczenie przede wszystkim wtedy, gdy obecne są sygnały termogeniczne.
Co to oznacza dla przyszłych terapii
Mówiąc prosto, praca ta pokazuje, że kość nie jest tylko biernym szkieletem, lecz aktywnym regulatorem tego, ile energii spalają komórki tłuszczowe. Sklerostyna działa jak pokrętło głośności, które utrzymuje aktywność tłuszczu termogenicznego, a tym samym zużycie paliwa, pod kontrolą. Przyciszenie tego pokrętła — poprzez zmiany genetyczne lub leki — sprawia, że niektóre zasoby białego tłuszczu chętniej przełączają się w tryb wytwarzania ciepła, gdy organizm zostanie pobudzony zimnem lub specyficznymi lekami. Ponieważ ta sama interwencja może wzmocnić kości i poprawić zdrowie metaboliczne u myszy, starannie zaprojektowane kombinacje terapii ukierunkowanych na kość i tłuszcz mogą pewnego dnia pomagać leczyć otyłość, cukrzycę i osteoporozę jednocześnie, zamiast jednej choroby na raz.
Cytowanie: Choquette, G.M., Kim, S.P., Wilkinson, K.J. et al. Sclerostin deficiency sensitizes white adipocytes to thermogenic signals that induce beiging in mice. Nat Commun 17, 2394 (2026). https://doi.org/10.1038/s41467-026-69227-0
Słowa kluczowe: sklerostyna, tłuszcz beżowy, komunikacja kość–tłuszcz, termogeneza, choroby metaboliczne