Clear Sky Science · pl
Miejscowa synteza PI(4,5)P2 przez izoformy PIPKIγ związane z septynami kontroluje wiązanie centralspindlin z midbody podczas cytokinezy
Jak komórki kończą rozdzielanie na dwie
Cytokineza — końcowe zaciśnięcie, które dzieli jedną komórkę na dwie — łatwo uznać za oczywistość, lecz gdy zawodzi, może przyczyniać się do powstawania nowotworów i innych chorób. To badanie ujawnia, jak konkretny zestaw molekuł działa jak kierownicy budowy na wąskim moście łączącym dwie nowo powstałe komórki, dopilnowując, żeby podział zakończył się czysto, zamiast cofać się lub utknąć.
Ostatni most między komórkami potomnymi
Po tym, jak komórka zdubluje materiał genetyczny i rozdzieli chromosomy, musi się fizycznie podzielić. Pierścień kurczliwy z włókien białkowych zaciska się wokół środka komórki, tworząc głęboką bruzdę zwaną bruzdą podziałową. W miarę jak bruzda ściąga, dwie komórki potomne pozostają połączone cienkim mostkiem międzykomórkowym, zawierającym gęste centrum — midbody. Midbody to maleńka, lecz złożona struktura z ułożonych pęczków mikrotubul, białek szkieletowych i lipidów sygnałowych; pełni rolę kotwicy i centrum sterowania koordynującego ostatnie etapy podziału oraz finalne przecięcie. 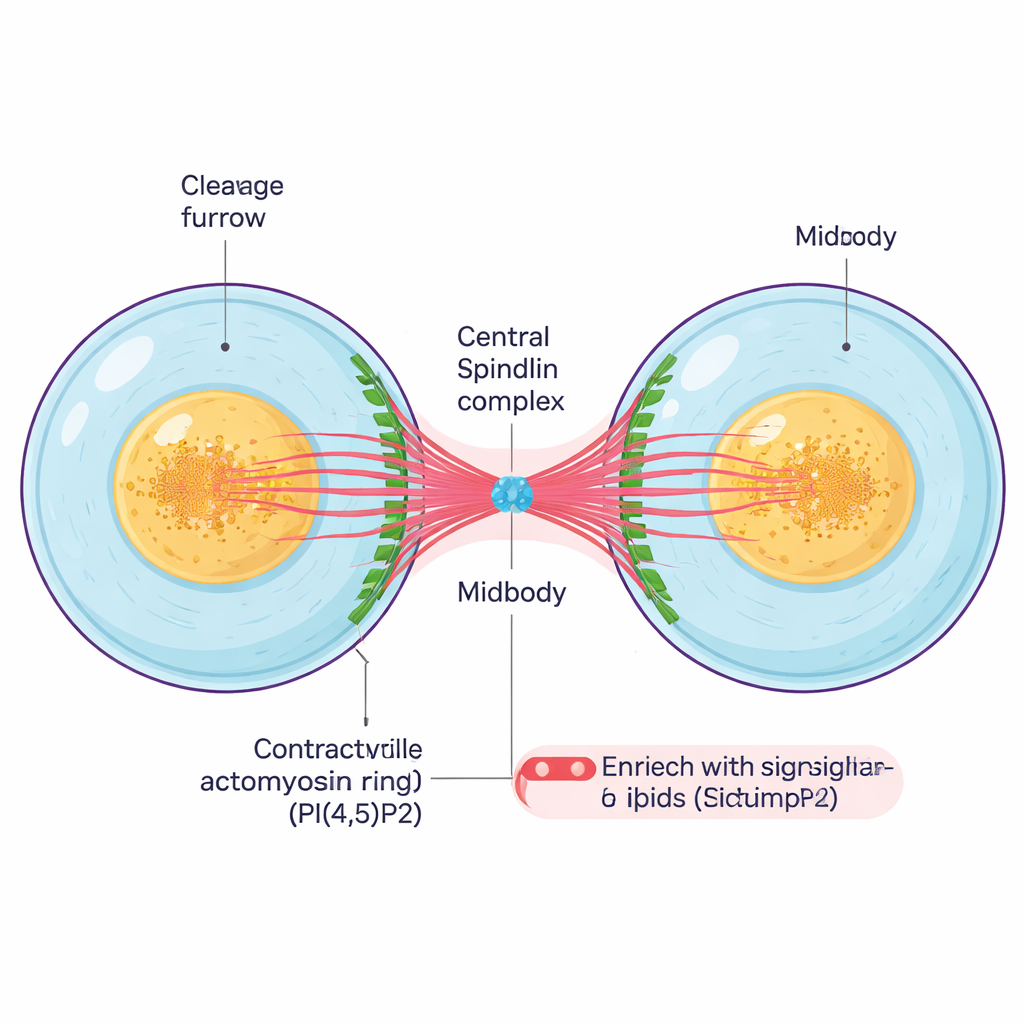
Sygnał lipidowy, który musi być we właściwym miejscu
Kluczowym graczem w tym procesie jest sygnałowy lipid błonowy zwany PI(4,5)P2. Ten lipid pomaga zakotwiczać wiele białek, które budują i kurczą pierścień oraz stabilizują mostek. Zagadką było, jak komórki kontrolują miejsce i czas pojawienia się PI(4,5)P2, skoro może on dyfundować w błonie. Autorzy skupili się na enzymach zwanych kinazami PIP typu I, które tworzą PI(4,5)P2, a w szczególności na jednym genie, PIPKIγ, występującym w kilku delikatnie różniących się formach wynikających ze splicingu. Poprzez selektywne obniżanie poziomów każdej kinazy w komórkach ludzkich i obserwacje za pomocą zaawansowanej mikroskopii wykazali, że PIPKIγ odgrywa szczególną rolę późno w cytokinezie, gdy tworzy się mostek i midbody, mimo że nie zmienia znacząco ogólnego poziomu PI(4,5)P2 na powierzchni komórki.
Septynowe rusztowania rekrutują wyspecjalizowany enzym
Zespół odkrył, że dwie wersje splicingowe PIPKIγ, nazwane i3 i i5, działają jak narzędzia precyzyjne, sprowadzane we właściwe miejsce przez białka strukturalne znane jako septyny. Septyny tworzą włókna i pierścienie, które pomagają kształtować mostek i organizować inne składniki. Wyciągi biochemiczne i obrazowanie komórek wykazały, że PIPKIγ-i3 i PIPKIγ-i5 fizycznie wiążą się ze złożeniami septyn i dekorują włókna septynowe, podczas gdy inne warianty PIPKIγ tego nie robią. Gdy badacze zmienili dwa konkretne aminokwasy w tych wstawkach splicingowych, enzymy nie mogły już wiązać septyn. W dzielących się komórkach prawidłowe PIPKIγ-i3/i5 przechodzą z rozproszonego wzoru błonowego do koncentracji w bruzdzie podziałowej, a następnie obrysowują mostek i midbody w synchronii z septynami i innym białkiem szkieletowym, anilliną. Usunięcie tylko wariantów i3 i i5 rozpraszało anillinę i septyny z midbody wzdłuż mostka, a wiele komórek nie kończyło cytokinezy i kończyło z wieloma jądrami.
Miejscowa produkcja lipidów utrwala maszynerię podziału
Aby sprawdzić, czy te efekty zależą od miejscowej produkcji PI(4,5)P2, autorzy zmierzyli PI(4,5)P2 wokół midbody i manipulowali enzymami, które ten lipid dodają lub usuwają. Zubożenie PIPKIγ-i3/i5 zmniejszało PI(4,5)P2 w midbody, podczas gdy zablokowanie enzymu degradującego PI(4,5)P2 miało efekt przeciwny. Co ważne, przywrócenie normalnej, wiążącej septyny i katalitycznie aktywnej formy splice PIPKIγ odtwarzało prawidłowe skupienie anilliny i septyn na mostku, natomiast enzymy „nieme kinetycznie” lub mutanty niezdolne do wiązania septyn tego nie robiły. Dzięki obrazowaniu na żywo i technice mikroskopii ekspansyjnej, która fizycznie „nadmuchuje” próbkę, aby ujawnić drobne detale, zespół pokazał, że bez PIPKIγ-i3/i5 septyny przestają przemieszczać się na mikrotubule mostka, mostek staje się krótszy i mniej pęczkowany, a kluczowy kompleks zwany centralspindlin przestaje pozostawać ściśle związany z midbody. 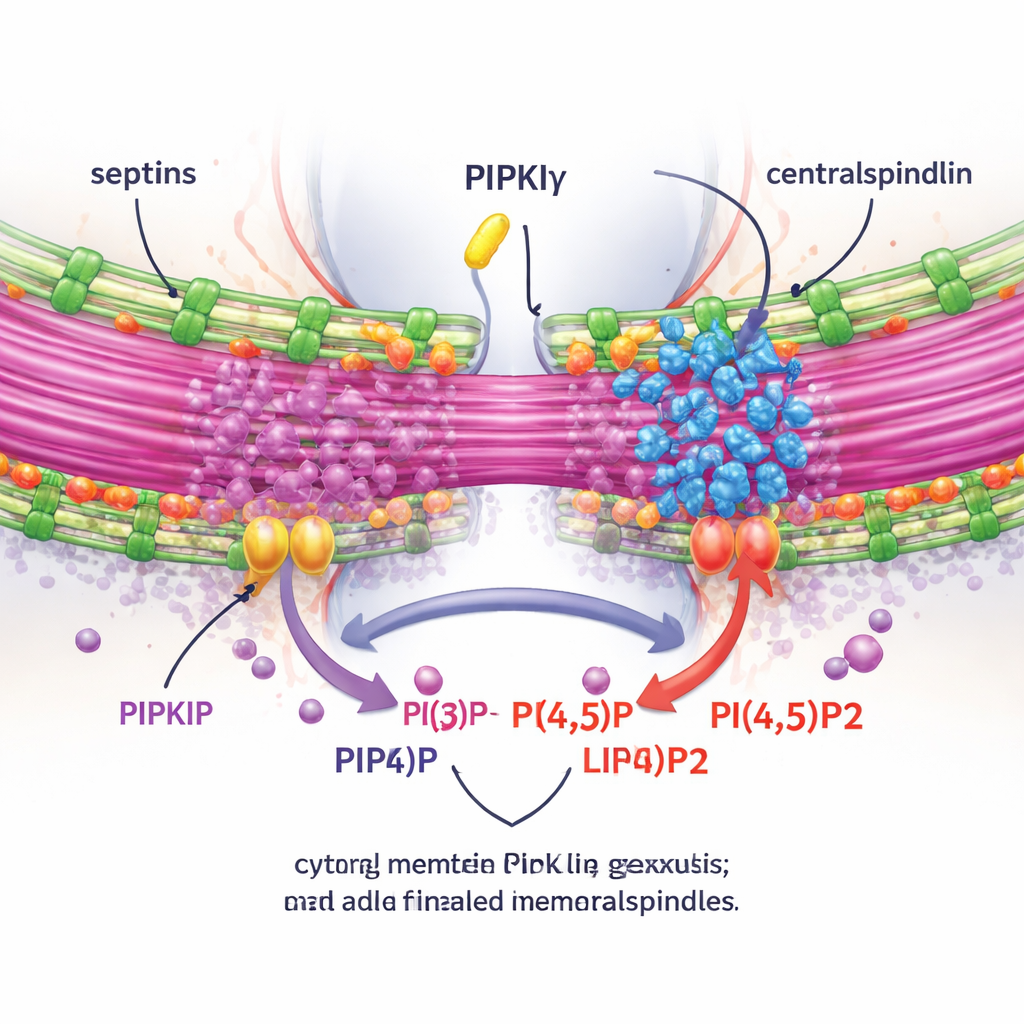
Budowanie punktu kontrolnego dla czystego przecięcia
Centralspindlin pomaga łączyć mikrotubule midbody z otaczającą błoną i reguluje małe przełączniki molekularne kontrolujące kształt komórki. Badanie pokazuje, że centralspindlin wiąże się zarówno z septynami, jak i PIPKIγ, i że utrata któregokolwiek z partnerów podobnie osłabia jego obecność w midbody. Autorzy proponują, że septyny rekrutują PIPKIγ-i3/i5 do wciągniętej bruzdy, gdzie te enzymy tworzą skoncentrowaną łatkę PI(4,5)P2. Miejscowa pula tego lipidu stabilizuje z kolei anillinę, centralspindlin i septyny w pobliżu midbody, sprzyja pęczkowaniu i stabilizacji mikrotubul mostka oraz pozwala, by mostek międzykomórkowy dojrzewał aż do końcowego przecięcia (abscission). Jeśli ten system zostanie zakłócony, PI(4,5)P2 pojawia się w niewłaściwych miejscach, białka rusztowania się rozpraszają, mikrotubule są słabo pęczkowane, a cytokineza często zawodzi.
Dlaczego to ma znaczenie poza podstawową biologią komórki
Wskazując, jak konkretne warianty splice PIPKIγ i septyny współpracują, by wygenerować miejscowy sygnał lipidowy w midbody, praca ta wyjaśnia, jak komórki nadają precyzję przestrzenną wysoce ruchliwemu molekułowi sygnałowemu. Ta precyzja jest kluczowa dla bezpiecznego zakończenia podziału komórki, pomagając zapobiegać błędnej segregacji chromosomów i nieprawidłowej liczbie komórek, co może sprzyjać powstawaniu guzów. Te same struktury midbody wpływają też na los komórek i proliferację po podziale, więc zrozumienie ich montażu otwiera nowe drogi do badania, jak błędy w tych nanoskaliowych rusztowaniach mogą przyczyniać się do raka i potencjalnie do manipulowania komórkami macierzystymi.
Cytowanie: Russo, G., Hümpfer, N., Jaensch, N. et al. Local PI(4,5)P2 synthesis by septin-associated PIPKIγ isoforms controls centralspindlin association with the midbody during cytokinesis. Nat Commun 17, 1482 (2026). https://doi.org/10.1038/s41467-026-69224-3
Słowa kluczowe: podział komórki, cytokineza, lipidy sygnałowe, septyny, biologia nowotworów