Clear Sky Science · pl
Pan‑inhibitor RAF exarafenib celuje w raka płuca NSCLC z mutacjami BRAF klasy II/III i ujawnia oporność zależną od ARAF‑KSR1 oraz strategie kombinacyjne
Dlaczego te badania mają znaczenie dla pacjentów z rakiem płuca
Większość osób słyszała o lekach ukierunkowanych, które trafiają w konkretne zmiany genetyczne. Jednak u wielu pacjentów z rakiem płuca, zwłaszcza u tych, których guzy noszą rzadsze mutacje w genie BRAF, dostępne dziś terapie celowane po prostu zawodzą. W tym badaniu przedstawiono nowy lek eksperymentalny, exarafenib, zaprojektowany tak, by trafiać szerszy zestaw nowotworów napędzanych przez BRAF, oraz opisano mechanizmy, dzięki którym komórki nowotworowe próbują mu się wymknąć — ujawniając kombinacje leczenia, które mogłyby dłużej kontrolować te guzy.
Ukryta większość pomijanych mutacji
Naukowcy zaczęli od prostego pytania: jak często występują różne typy mutacji BRAF w zaawansowanych nowotworach, a w szczególności w niedrobnokomórkowym raku płuca (NSCLC)? Korzystając z bardzo dużej bazy płynnych biopsji obejmującej ponad 160 000 pacjentów, przeanalizowali fragmenty DNA nowotworowego krążące we krwi. Stwierdzili, że w raku płuca mutacje BRAF występują u około 4–5% pacjentów, co i tak przekłada się na wiele tysięcy osób na całym świecie. Co istotne, około dwie trzecie tych guzów płucnych nosiło tzw. mutacje BRAF klasy II i III — typy, na które zatwierdzone obecnie leki przeciw BRAF nie działają skutecznie. Pacjenci z jedną z tych klas, zwłaszcza klasy II, mieli tendencję do krótszego przeżycia niż ci z bardziej znaną mutacją klasy I, prawdopodobnie dlatego, że pacjenci z klasą I mają dostęp do ustalonych terapii celowanych, podczas gdy pacjenci z klasą II/III otrzymują głównie chemioterapię lub immunoterapię.
Lek następnej generacji, który celuje w całą ścieżkę
BRAF jest częścią łańcucha białek (szlaku MAPK), który przekazuje sygnały wzrostu z powierzchni komórki do jądra. Wiele istniejących leków przeciw BRAF zostało zaprojektowanych tak, by blokować tylko jedną zmutowaną formę i mogą nawet przypadkowo pobudzać pokrewne białka w komórkach prawidłowych. Exarafenib został zbudowany inaczej: jest „pan‑inhibitorem RAF” mającym na celu wyłączyć kilku członków rodziny RAF (ARAF, BRAF i CRAF) zarówno w formach pojedynczych, jak i paru, przy jednoczesnym oszczędzaniu większości innych enzymów komórkowych. W testach biochemicznych obejmujących setki ludzkich kinaz exarafenib silnie blokował wszystkie trzy białka RAF, ale miał niewiele efektów pozaszkieletowych, co sugeruje czystszy profil bezpieczeństwa w porównaniu z wcześniejszymi związkami pan‑RAF.
Mocne działanie w modelach trudnych do leczenia guzów
Zespół testował exarafenib w szeregu linii komórkowych i modelach mysich niosących różne mutacje BRAF i RAS, w tym realistyczne guzy pochodzące od pacjentów. W hodowlach komórkowych exarafenib hamował wzrost i wyłączał sygnalizację MAPK nie tylko w klasycznych komórkach nowotworowych z mutacją BRAF V600E, ale także w komórkach z mutacjami klasy II i III oraz w wielu komórkach z mutacjami RAS, dla których obecnie brak dobrych opcji celowanych. U myszy z guzami płucnymi o tych zmianach exarafenib zmniejszał lub spowalniał wzrost guzów w sposób zależny od dawki i wykazywał wyraźne korelacje między poziomami leku, tłumieniem szlaku a odpowiedzią guza. Wczesne dane kliniczne od dwóch pacjentów z zaawansowanym rakiem płuca z mutacją BRAF — jednego z rzadką fuzją BRAF i drugiego z punktową mutacją klasy II — wykazały częściowe odpowiedzi i istotną ulgę w objawach, co potwierdza znaczenie badań przedklinicznych.
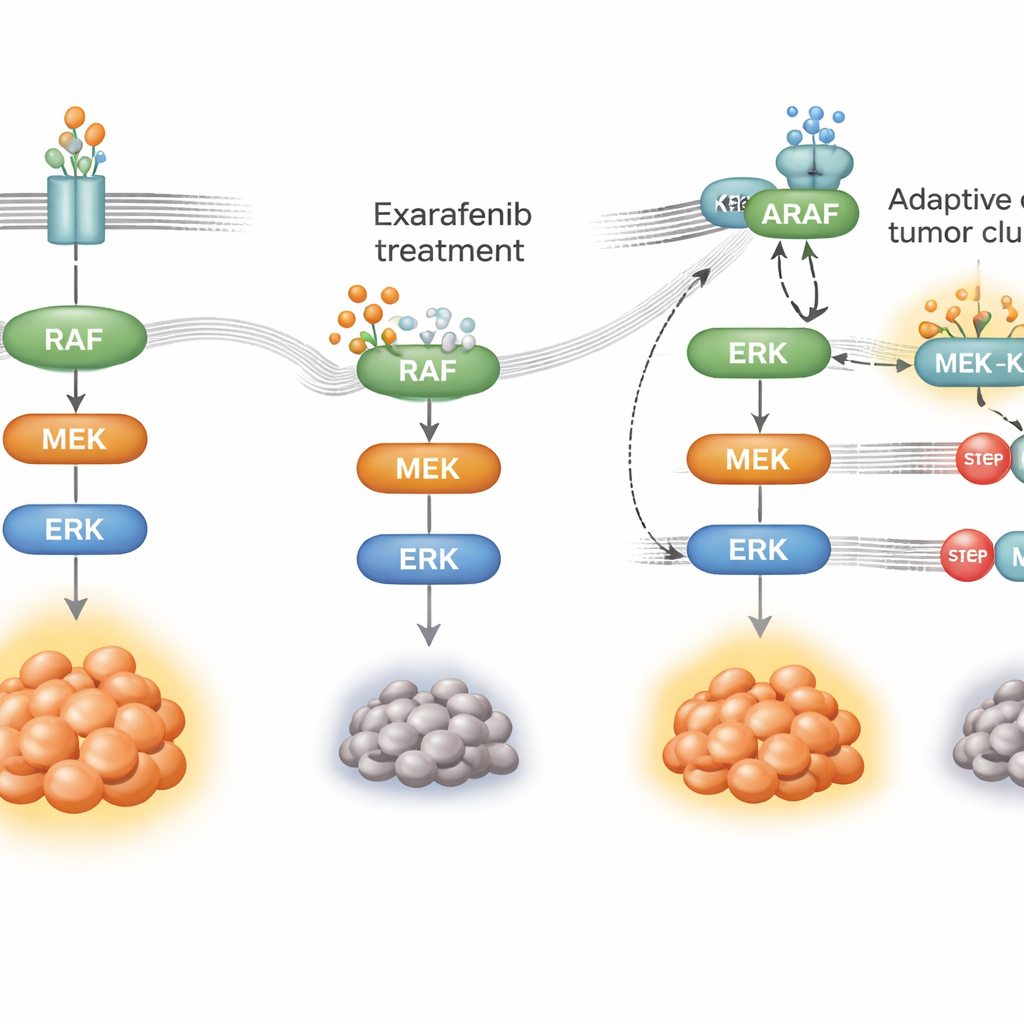
Jak nowotwór uczy się omijać lek
Żadna terapia ukierunkowana nie działa wiecznie; komórki nowotworowe adaptują się. Aby zobaczyć, jak guzy mogą stać się oporne na exarafenib, badacze eksponowali komórki raka płuca z mutacją BRAF na działanie leku przez miesiące, aż pojawiły się populacje oporne. Komórki te nadal polegały na tym samym szlaku wzrostu, ale przeorganizowały jego wykorzystanie. Zamiast zależeć głównie od zmutowanego BRAF, zwiększyły aktywność górnego przełącznika zwanego RAS i przestawiły się na używanie innego członka rodziny, ARAF, razem ze białkiem rusztującym KSR1. Pod presją leku ARAF i KSR1 tworzyły ciasne kompleksy, które pomagały utrzymać przekaźnictwo MAPK, nawet gdy exarafenib był związany. Gdy naukowcy selektywnie wyciszyli ARAF lub KSR1 albo zmniejszyli aktywność RAS, komórki oporne ponownie stały się wrażliwe na exarafenib, a sygnały przeżycia upadły.
Strategie kombinacyjne, by uprzedzić oporność
Uzbrojeni w tę mapę mechanistyczną, badacze poszukali leków partnerskich, które mogłyby zablokować szlak w punktach krytycznych wspólnych dla pierwotnej i obwodowej drogi. Odkryli, że łączenie exarafenibu z lekami hamującymi MEK lub ERK — kluczowe kroki w dółstrumieniowe szlaku MAPK — dawało silną synergiię w wielu modelach komórkowych i mysich, w tym w guzach, które były z natury mniej wrażliwe lub nabyły oporność. Takie kombinacje utrzymywały szlak dłużej zamkniętym, wywoływały więcej śmierci komórek i u zwierząt często działały równie dobrze lub lepiej niż wyższe dawki samego exarafenibu, bez wyraźnie dodanej toksyczności. Agenty celujące bezpośrednio w RAS również wzmacniały efekty exarafenibu w modelach, w których RAS wyraźnie napędzał oporność, co sugeruje kolejny obiecujący taktycznie kierunek kliniczny.
Co to oznacza dla pacjentów
Dla osób z NSCLC niosącymi mutacje BRAF klasy II lub III — lub złożone fuzje BRAF i współistniejące mutacje RAS — obecnie nie ma zatwierdzonych terapii celowanych, a wyniki leczenia pozostają gorsze niż u pacjentów z częstszymi zmianami. To badanie dostarcza mocnego naukowego uzasadnienia, że exarafenib mógłby wypełnić tę lukę, szeroko wyłączając sygnalizację napędzaną przez RAF. Wyjaśnia też, jak guzy mogą adaptować się poprzez obejście ARAF‑KSR1 i pokazuje, że blokowanie szlaku na kilku poziomach, szczególnie przez łączenie inhibitorów RAF i MEK lub dodanie inhibitorów RAS, może dać głębszą i trwalszą kontrolę nad guzem. Razem te spostrzeżenia wyznaczają drogę do badań klinicznych, które mają na celu dostarczenie spersonalizowanych, kombinowanych terapii dużej i wcześniej niedostatecznie obsłużonej grupie pacjentów z rakiem płuca.
Cytowanie: Manabe, T., Bergo, H.C., Li, Q. et al. Pan-RAF inhibitor exarafenib targets BRAF class II/III NSCLC and reveals ARAF-KSR1 resistance and combination strategies. Nat Commun 17, 2484 (2026). https://doi.org/10.1038/s41467-026-69216-3
Słowa kluczowe: nowotwór płuca z mutacją BRAF, pan‑inhibitor RAF, sygnalizacja MAPK, oporność na leki, kombinacje terapii celowanej