Clear Sky Science · pl
Inżynieria enzymu cytochromu P450 jako peroksydazy do selektywnej hydroksylacji steroidów
Tworzenie leków z trudnych do dopracowania cząsteczek
Leki steroidowe — od tabletek przeciwzapalnych po terapie hormonalne — należą do najpowszechniej stosowanych leków na świecie. Jednak precyzyjne dostosowanie tych cząsteczek, przez dodanie pojedynczego atomu tlenu w dokładnie określonym miejscu, jest zadaniem niezwykle trudnym przy użyciu tradycyjnej chemii. Niniejsze badanie pokazuje, jak naukowcy przeprojektowali naturalny enzym tak, by mógł precyzyjnie „wykończyć” cząsteczki steroidowe przy użyciu prostego nadtlenku wodoru, co potencjalnie umożliwia bardziej ekologiczne i tańsze ścieżki do ważnych leków.
Dlaczego steroidy trudno dostosować
Steroidy zbudowane są z zwartego stosu pierścieni węglowych, zawierającego wiele niemal identycznych wiązań węgiel–wodór. Konwencjonalne metody chemiczne mają trudność, by trafić tylko w jedno z tych wiązań, nie naruszając pozostałych, często wymagając ostrych reagenci, wysokich temperatur i wielokrotnych etapów ochrony, które generują odpady. Tymczasem drobne zmiany — na przykład dodanie pojedynczej grupy hydroksylowej (–OH) w określonej pozycji — mogą zdecydowanie zmienić zachowanie steroidu w organizmie. Enzymy z rodziny cytochromu P450 są w naturze specjalistami od tak precyzyjnej aktywacji wiązań C–H, ale w formie naturalnej zwykle potrzebują kosztownych koenzymów i aparatów przenoszących tlen, co ogranicza ich bezpośrednie zastosowanie w produkcji.
Odkrycie obiecującego enzymu wyjściowego
Wykorzystując poszukiwanie w genomach, badacze zidentyfikowali samowystarczalny enzym P450, nazwany P450stri, pochodzący z bakterii glebowej. W przeciwieństwie do klasycznego enzymu P450BM3, który preferuje małe kwasy tłuszczowe, P450stri naturalnie akceptuje obszerne cząsteczki steroidowe, takie jak testosteron. W warunkach swojego naturalnego działania, zasilany przez wewnątrzkomórkowy koenzym NADH, P450stri dodaje grupy hydroksylowe w trzech pozycjach testosteronu, wytwarzając mieszaninę produktów. Ta wrodzona zdolność rozpoznawania steroidów uczyniła P450stri atrakcyjnym „szkieletem wyjściowym” do zaprojektowania bardziej selektywnego i przyjaznego dla przemysłu katalizatora.
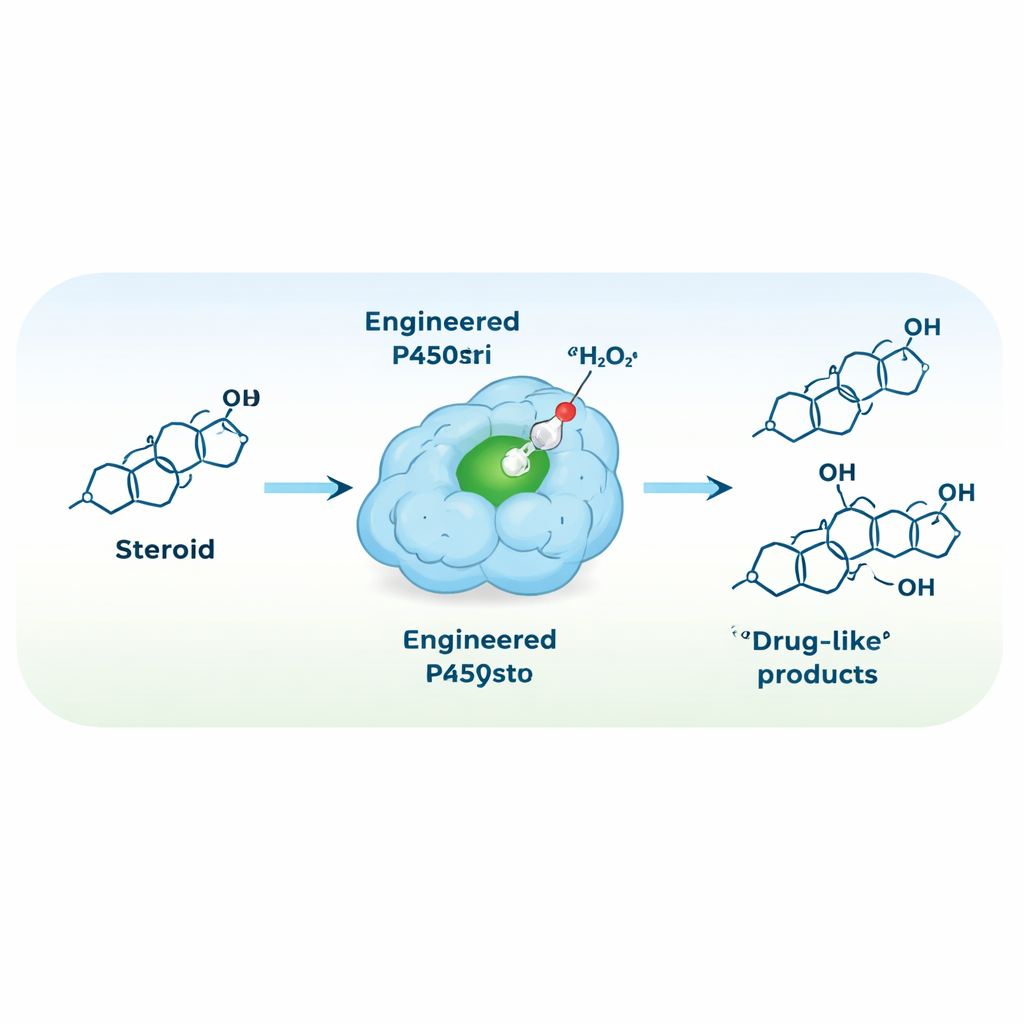
Przeprojektowanie enzymu do pracy na nadtlenku wodoru
Aby uprościć układ reakcyjny, zespół postawił sobie za cel przekształcenie P450stri w peroksydazę — enzym używający bezpośrednio nadtlenku wodoru jako utleniacza, eliminując potrzebę drogich koenzymów i białek pomocniczych. Jedna strategiczna mutacja, zastąpienie masywnego fenyloalaniny tuż nad centrum hemowym mniejszą alaniną, stworzyła wariant oznaczony M1. Ta zmiana otworzyła przestrzeń wokół reaktywnego centrum żelazowego i co zaskakujące uczyniła enzym zarówno bardziej odpornym na wysokie stężenia nadtlenku wodoru, jak i znacznie bardziej selektywnym. W nowym, napędzanym nadtlenkiem trybie M1 przekształcał testosteron głównie w jeden produkt, hydroksylowany w pozycji 15β, z selektywnością około 94% — w porównaniu z 35% w enzymie wyjściowym.
Model „Okrągłej Kolby” dla inteligentniejszego projektowania enzymów
Aby jeszcze poprawić działanie, autorzy wprowadzili koncepcję projektową nazwaną modelem „Okrągłej Kolby”. Traktują miejsce aktywne, gdzie zachodzi reakcja, jako zaokrągloną bazę, a wąskie kanały dostępu jako szyjkę i korek. Baza determinuje, która pozycja na sterydzie zostanie zmodyfikowana, podczas gdy szyjka kontroluje, jak łatwo steryd i nadtlenek wodoru dotrą do reaktywnego centrum. Kierowani symulacjami komputerowymi i oprogramowaniem mapującym tunele, systematycznie dostosowywali mały zestaw aminokwasów wyściełających te tunele, regulując ich rozmiar i hydrofobowość. Ta dwuwymiarowa strategia dała wyróżniający się wariant M4, który utrzymał wysoką selektywność 15β przy jednoczesnym znacznym zwiększeniu szybkości reakcji i tolerancji na stężenia nadtlenku wodoru sięgające kilkuset milimoli.
Od ławy laboratoryjnej do skalowalnej modyfikacji steroidów
Zmodyfikowany enzym M4 został następnie przetestowany w reakcjach na większą skalę z testosteronem i spokrewnionym steroidem stosowanym w kontekstach zwiększania wydolności. W prostych wodnych mieszaninach w temperaturze pokojowej, napędzanych wyłącznie nadtlenkiem wodoru, M4 przekształcił ponad 90% materiału wyjściowego i dostarczył izolowane produkty 15β-hydroksylowane z wydajnościami rzędu 75–80%. Warunki te są znacznie łagodniejsze i czystsze niż typowe drogi chemiczne. Wreszcie zespół pokazał, że przez przeszczepienie kluczowych mutacji do kilku pokrewnych enzymów P450 z tej samej gałęzi ewolucyjnej można ich niezawodnie uczynić podobnie selektywnymi i wydajnymi peroksydazami, co podkreśla ogólność zasad projektowania.
Co to oznacza dla przyszłych leków
Dla osoby niebędącej specjalistą, najważniejsza wiadomość jest taka, że badacze nauczyli naturalny enzym działać jak wysoce precyzyjna, napędzana nadtlenkiem „mikro‑fabryka” modyfikująca leki steroidowe. Łącząc prosty model koncepcyjny z ukierunkowanymi mutacjami, stworzyli enzym, który może dodać grupę OH we właściwym miejscu, w łagodnych i skalowalnych warunkach, a następnie przenieśli tę strategię na pokrewne białka. Podejście to może uprościć produkcję istniejących steroidów, otworzyć ścieżki do nowych kandydatów na leki i posłużyć jako plan dla inżynierii innych enzymów, które czysto aktywują oporne wiązania C–H w złożonych cząsteczkach.
Cytowanie: Tang, T., Wang, R. & Chen, Y. Engineering a cytochrome P450 enzyme as a peroxygenase for selective hydroxylation of steroids. Nat Commun 17, 1996 (2026). https://doi.org/10.1038/s41467-026-69211-8
Słowa kluczowe: biokataliza steroidów, inżynieria cytochromu P450, peroksydaza, kataliza nadtlenkiem wodoru, selektywna hydroksylacja