Clear Sky Science · pl
Biologia strukturalna pojedynczych komórek przy użyciu wewnątrzkomórkowej krystalografii elektronowej
Oglądanie kształtu życia, komórka po komórce
Białka to maleńkie maszyny, które utrzymują każdą komórkę przy życiu, ale aby naprawdę zrozumieć, jak działają, naukowcy muszą zobaczyć ich trójwymiarowe kształty w dużych detalach. Tradycyjnie oznaczało to oczyszczanie ogromnych ilości białka i hodowanie dużych, delikatnych kryształów poza komórką — często proces powolny i podatny na niepowodzenia. W tym badaniu przedstawiono nowy sposób odczytywania struktury białka bezpośrednio z pojedynczego kryształu wewnątrz pojedynczej komórki, używając elektronów zamiast promieni X. Wskazuje to drogę ku przyszłości, w której wysokorozdzielcza biologia strukturalna będzie możliwa w zwykłych laboratoriach, a nawet na poziomie pojedynczych komórek.
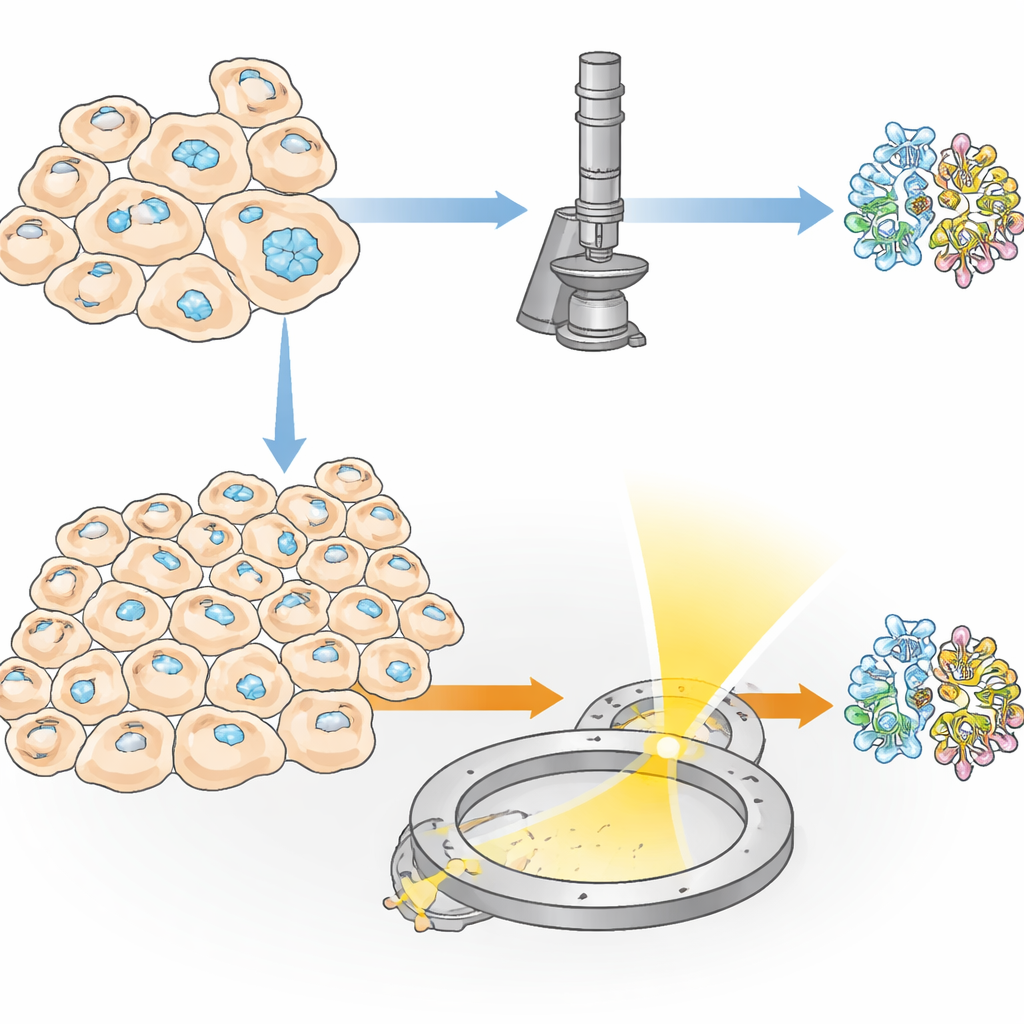
Kryształy ukryte w żywych komórkach
Niektóre białka naturalnie agregują w maleńkie kryształy wewnątrz żywych komórek, pełniąc funkcje takie jak magazynowanie, ochrona czy pomoc w odpowiedzi na stres. Naukowcy mogą też skłonić komórki do wytwarzania takich kryształów przez zaprojektowanie ich do produkcji dużych ilości wybranego białka. Ta „in‑cell” krystalizacja ma dwie duże zalety: białko nigdy nie opuszcza środowiska przypominającego naturalne, a delikatne cechy — na przykład modyfikacje cukrowe czy małe związane cząsteczki — mogą być zachowane w sposób, który często zawodzi w standardowej krystalizacji w probówce. Jednak pozostaje jedna poważna przeszkoda: w wielu doświadczeniach tylko niewielka część komórek faktycznie tworzy kryształy, więc tradycyjne metody rentgenowskie potrzebują dziesiątek tysięcy kryształów, a tym samym ogromnej liczby komórek.
Nowa droga: elektrony zamiast promieni X
Autorzy wprowadzają metodę nazwaną IncelluloED, łączącą krystalizację in‑cell z trójwymiarową dyfrakcją elektronów. Elektrony oddziałują z materią znacznie silniej niż promieniowanie rentgenowskie, co oznacza, że użyteczne dane można zebrać z kryształów mniejszych i w mniejszej liczbie. Zespół wybrał białko grzyba o nazwie HEX‑1, które normalnie tworzy heksagonalne kryształy pomagające zatykać maleńkie pory między komórkami grzyba pod wpływem stresu. Poprzez wytworzenie tego białka w komórkach owadzich uzyskali regularne mikroskopijne kryształy, które posłużyły jako przypadek testowy dla nowego procesu.
Zmiana jednego kryształu w szczegółową mapę
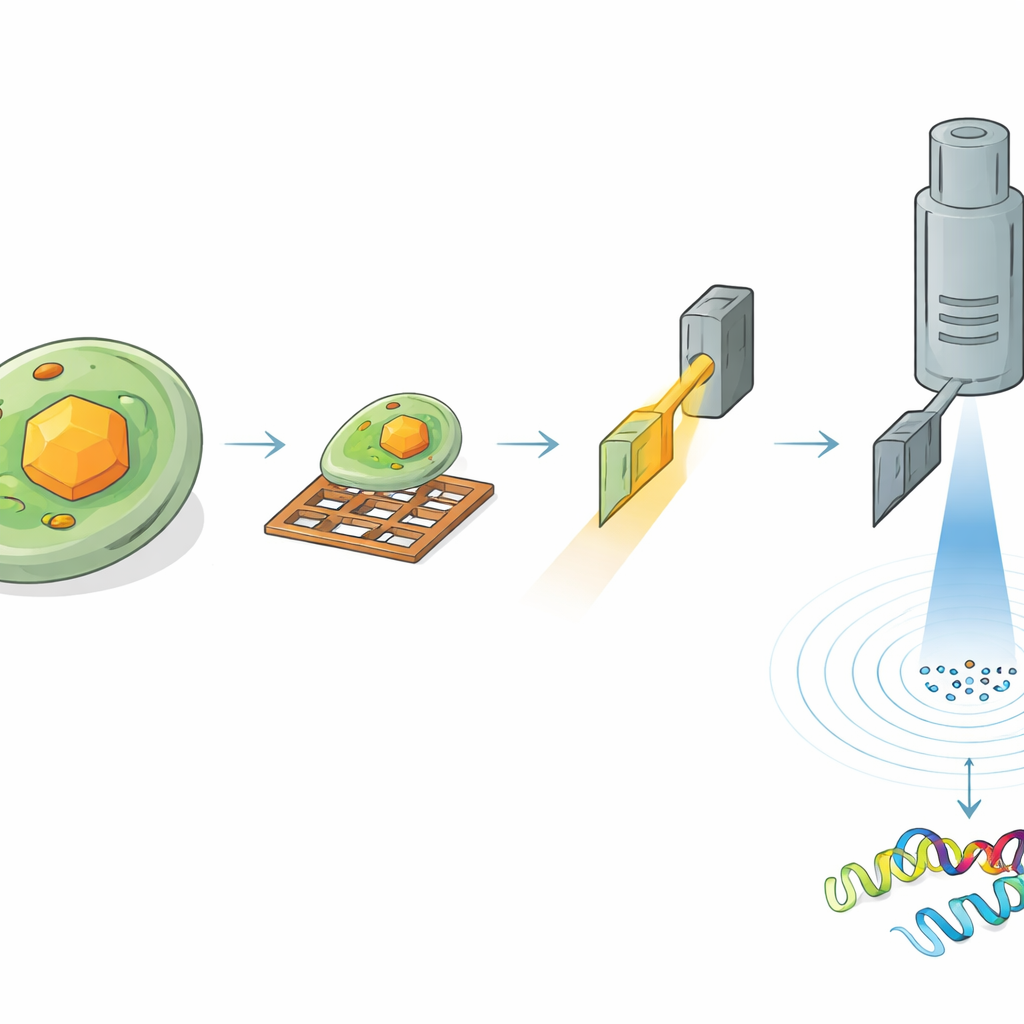
Aby odczytać strukturę HEX‑1 wewnątrz komórki, badacze musieli znaleźć i starannie zeszlifować właściwy obszar próbki. Najpierw zamrozili komórki zawierające kryształy na małych metalowych siatkach i pokryli powierzchnię cienką warstwą platyny. Korzystając z kriogenicznej mikroskopii świetlnej, skanowali duże obszary siatki, aby zlokalizować komórki z kryształami i zmierzyć trójwymiarowe położenie kryształów pod powierzchnią. Następnie przenieśli tę samą próbkę do specjalistycznego instrumentu łączącego skanujący mikroskop elektronowy z skoncentrowanym wiązką jonów. Kierowani wcześniejszymi obrazami świetlnymi, frezowali otaczający materiał, aby wydrążyć ultracienki plasterek, czyli lamelę, przechodzącą przez wybrany kryształ, o grubości zaledwie kilkuset nanometrów — idealny do przejścia elektronów.
Elektrony ujawniają atomowe szczegóły z mikroskopijnych objętości
Przygotowane lamelki przeniesiono następnie do wysokiej klasy mikroskopu elektronowego pracującego w temperaturach kriogenicznych. Gdy plasterek kryształu był powoli obracany w mikroskopie, precyzyjnie kontrolowana wiązka elektronów przechodziła przez niego, tworząc serię wzorów dyfrakcyjnych — delikatnych układów plamek kodujących położenia atomów. Z kryształowej objętości rzędu 1,6 mikrometra sześciennego zespół odtworzył pełną strukturę 3D HEX‑1 z rozdzielczością 1,9 angstroma, wystarczająco ostrą, by zamodelować większość łańcuchów bocznych białka. Jeszcze mniejsze objętości około 0,8 mikrometra sześciennego dały niemal identyczną strukturę przy nieznacznie niższej rozdzielczości. Co istotne, otrzymane modele bardzo dobrze zgadzały się z tymi uzyskanymi konwencjonalnym podejściem rentgenowskim seryjnym, które wymagało ponad 60 000 kryształów i łącznej objętości kryształów około siedem milionów razy większej.
Jak to zmienia zasady gry w biologii strukturalnej
Porównania „jeden do jednego” wykazały, że struktura określona z pojedynczego in‑cell kryształu dyfrakcyjnego elektronami jest zasadniczo taka sama jak ta uśredniona z dziesiątek tysięcy kryształów przy użyciu promieni X. Różnice były niewielkie i przeważnie dotyczyły elastycznych pętli, gdzie oczekiwany jest naturalny ruch. Badacze wykazali również, że dawki elektronów użyte w eksperymencie były wystarczająco niskie, by uniknąć poważnych uszkodzeń radiacyjnych, i że każdy kryształ, który przetwarzali, dostarczał danych wysokiej jakości. Choć przygotowanie cienkich lameli nadal wymaga umiejętności i czasu, niezbędne instrumenty — kriogeniczne mikroskopy świetlne, systemy z wiązką jonów oraz kriogeniczne mikroskopy elektronowe — są już szeroko dostępne w wielu ośrodkach badawczych.
Od wielu komórek do laboratorium strukturalnego pojedynczej komórki
Praca ta pokazuje, że obecnie możliwe jest określenie struktury białka na poziomie atomowym z zaledwie jednego kryształu wewnątrz jednej komórki, bez konieczności oczyszczania białka. IncelluloED może być szczególnie użyteczne, gdy tylko kilka komórek tworzy kryształy lub gdy białka trudno jest izolować bez utraty ważnych partnerów czy grup chemicznych. W miarę jak przepływ pracy stanie się bardziej zautomatyzowany i zostanie rozszerzony na inne białka, może umożliwić badanie, jak struktury różnią się między komórkami, badanie zmian związanych z chorobami w ich rodzimym środowisku, a nawet wspieranie odkrywania leków bezpośrednio w żywych komórkach. W istocie badanie przybliża wizję „laboratorium strukturalnego pojedynczej komórki” do rzeczywistości.
Cytowanie: Bílá, Š., Pinkas, D., Khakurel, K. et al. Single-cell structural biology with intracellular electron crystallography. Nat Commun 17, 2109 (2026). https://doi.org/10.1038/s41467-026-69205-6
Słowa kluczowe: dyfrakcja elektronów, krystalografia in cellulo, biologia strukturalna pojedynczych komórek, struktura białka, kriogeniczne EM