Clear Sky Science · pl
14-3-3ζ wchodzi w interakcję z domeną wiążącą DNA FOXO3a i konkurencyjnie odłącza DNA poprzez dwumotywowe tethering
Jak komórki nowotworowe wyłączają własny przełącznik samobójczy
Nasze komórki mają wbudowane systemy zabezpieczające, które mogą wywołać ich śmierć, gdy staną się zbyt uszkodzone lub niebezpieczne. Jednym z tych systemów kontroluje białko zwane FOXO3a, które uruchamia geny powodujące „samobójstwo” zbłąkanych komórek. Wiele nowotworów jednak znajduje sposoby, by uciszyć FOXO3a i nadal rosnąć. Niniejsze badanie zagłębia się w molekularne szczegóły tego, jak inne białko, 14-3-3ζ, pomaga komórkom nowotworowym odczepić FOXO3a od DNA i zneutralizować ten przełącznik samobójczy.
Białko‑strażnik, które odpycha przeciwnika
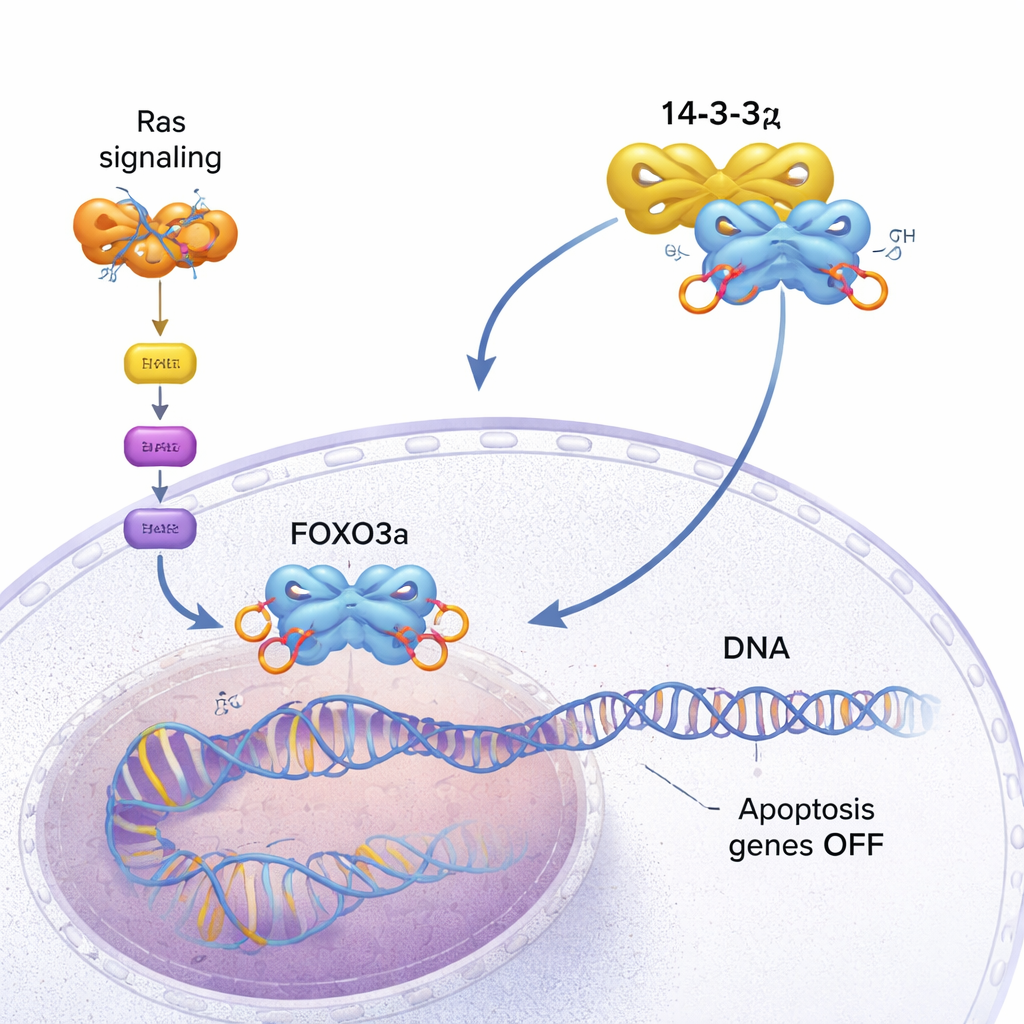
FOXO3a działa jak inspektor bezpieczeństwa komórki. Wiąże się z określonymi miejscami na DNA i aktywuje geny, które spowalniają wzrost lub wywołują zaprogramowaną śmierć komórki (apoptozę), gdy coś idzie nie tak. W zdrowych komórkach zapobiega to tworzeniu się guzów. W wielu nowotworach jednak aktywny jest trwale szlak promujący wzrost napędzany przez zmutowane białka Ras. Szlak ten aktywuje kinazę AKT, która chemicznie znakuję FOXO3a w kilku miejscach grupami fosforanowymi. Te znaczniki tworzą miejsca dokujące dla 14-3-3ζ, dimerycznego „adaptera” rozpoznającego sfosforylowane motywy u wielu celów. Gdy 14-3-3ζ zaczepia się o FOXO3a, wewnętrzne hamulce komórki zaczynają zawodzić.
Dlaczego sama siła wiązania nie wyjaśniała efektu
Wcześniejsze prace nad spokrewnionym białkiem FOXO4 sugerowały, że białka 14-3-3 odrywają czynniki FOXO od DNA po prostu dlatego, że wiążą się mocniej. Jednak FOXO3a preferuje swoje naturalne cele na DNA silniej niż zakładał starszy model. W tym badaniu badacze wyprodukowali wersję FOXO3a obejmującą domenę wiążącą DNA i dwa kluczowe miejsca fosforylacji. Zmierzyli, jak mocno to białko wiąże się z DNA lub z 14-3-3ζ i stwierdzili, że różnice w sile wiązania były umiarkowane: 14-3-3ζ było tylko około dwa razy silniejszym partnerem niż DNA. A jednak w eksperymentach mieszankowych śledzących migrację cząsteczek przez kolumnę chromatograficzną 14-3-3ζ potrafiło wypchnąć prawie całe DNA z FOXO3a, jakby było w przybliżeniu 100 razy bardziej konkurencyjne niż wynikałoby ze stosunku sił wiązania. Ta rozbieżność sugerowała, że działa dodatkowy mechanizm.
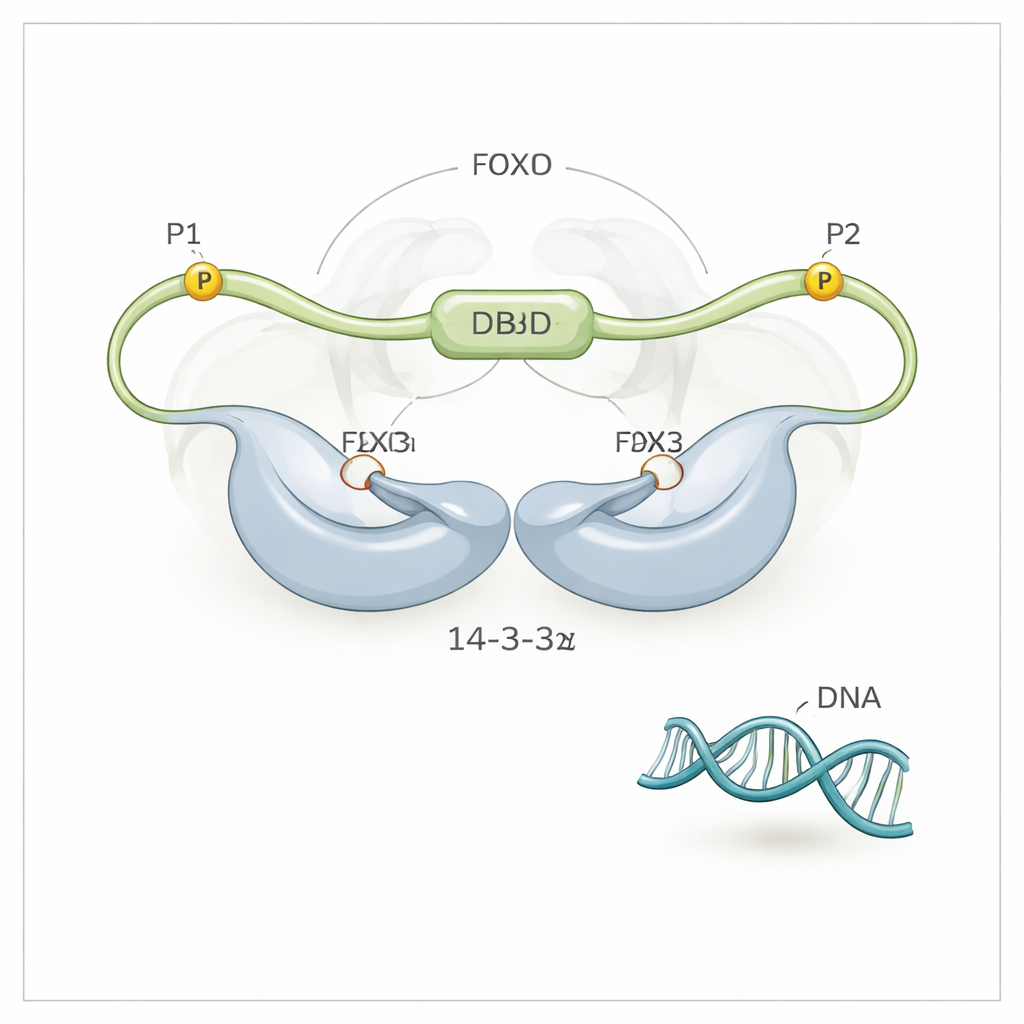
Trzypunktowy uchwyt, który wypiera DNA
Wykorzystując spektroskopię NMR o wysokiej rozdzielczości, zespół odkrył, że 14-3-3ζ robi więcej niż tylko chwyta FOXO3a za dwa sfosforylowane motywy (nazwane P1 i P2). Tworzy też bezpośredni, choć słabszy, kontakt z samą domeną wiążącą DNA (DBD) FOXO3a — tą powierzchnią, która normalnie obejmuje DNA. Białko 14-3-3ζ tworzy symetryczny dimer z dwoma rowkami. Każdy rowek zaciska się na jednym ze sfosforylowanych motywów FOXO3a, kotwicząc FOXO3a do 14-3-3ζ w dwóch punktach. Ponieważ jeden z tych motywów (P2) znajduje się bardzo blisko w łańcuchu względem domeny wiążącej DNA, to „dwumotywowe tethering” skutecznie trzyma 14-3-3ζ tuż obok DBD, znacznie zwiększając szansę, że DBD natrafi i związkuje powierzchnię 14-3-3ζ zamiast DNA. Badacze zaobserwowali nawet, że DBD przełącza się tam i z powrotem między dwoma stronami dimeru 14-3-3ζ, spędzając większość czasu osłonięte od DNA.
Które znaczniki fosforanowe mają największe znaczenie
Aby rozdzielić role obu miejsc fosforylacji, zespół skonstruował warianty FOXO3a, w których tylko jedno miejsce mogło być sfosforylowane naraz. Gdy aktywny był tylko P2, blisko DBD, 14-3-3ζ mogło częściowo odłączyć DNA, ale nie całkowicie. Gdy aktywny był tylko bardziej odległy P1, 14-3-3ζ potrafiło wiązać FOXO3a, lecz niemal nie wpływało na jego uchwyt na DNA. Pełne uwolnienie DNA wymagało współdziałania obu miejsc: P1 dostarcza wysokozauważalnego punktu początkowego dla 14-3-3ζ, a P2 ustawia dimer wystarczająco blisko DBD, by lokalne stężenie 14-3-3ζ w tym miejscu było efektywnie ogromne. Ten wieloetapowy tethering wzmacnia umiarkowaną preferencję wiązania w potężną zdolność do wypierania DNA.
Od molekularnej przeciągania liny do nowych pomysłów leków
Dla czytelnika nie‑specjalisty kluczowa konkluzja jest taka, że komórki nowotworowe wykorzystują sprytne zagranie geometryczne na poziomie molekularnym, a nie tylko siłę wiązania, aby uciszyć ważne białko supresorowe. 14-3-3ζ używa dwóch małych znaczników dokujących na FOXO3a jako punktów kotwiczenia, a następnie sięga, by zasłonić powierzchnię chwytającą DNA w domenie rdzeniowej FOXO3a, uniemożliwiając jej aktywację genów śmierci komórki. Ponieważ rodziny FOXO i 14-3-3 są szeroko wykorzystywane w wielu tkankach, ta strategia dwumotywowego tetheringu prawdopodobnie występuje także w innych nowotworach. Zakłócenie albo fosforanowo‑zależnych kotwic, albo słabszego kontaktu z powierzchnią wiążącą DNA FOXO3a mogłoby przywrócić jego zdolność do uruchamiania programów samobójczych w komórkach nowotworowych, oferując obiecujące nowe kierunki projektowania leków przeciwnowotworowych.
Cytowanie: Enomoto, S., Kuwayama, T., Nakatsuka, S. et al. 14-3-3ζ interacts with DNA-binding domain of FOXO3a and competitively dissociates DNA by dual-motif tethering. Nat Commun 17, 1503 (2026). https://doi.org/10.1038/s41467-026-69203-8
Słowa kluczowe: FOXO3a, białka 14-3-3, apoptoza, szlak Ras–AKT, terapie przeciwnowotworowe