Clear Sky Science · pl
Molekularne mechanizmy kompleksów flotylliny w organizacji mikrodomen błonowych
Ukryte pomieszczenia na powierzchni komórki
Każda komórka w twoim ciele jest otoczona cienką błoną, która na pierwszy rzut oka wydaje się prosta, ale w rzeczywistości jest podzielona na niezliczone maleńkie „sąsiedztwa”. Te strefy pomagają kontrolować odbiór sygnałów, wejście składników odżywczych i usuwanie odpadów. W tym badaniu ujawniono, jak para długo niejasnych białek, zwanych flotyllinami, buduje miniaturowe, osłonięte pomieszczenia po wewnętrznej stronie błony — struktury, które mogą wpływać na procesy tak różnorodne jak sygnalizacja komórkowa, transport ładunku, a nawet rozprzestrzenianie się raka. 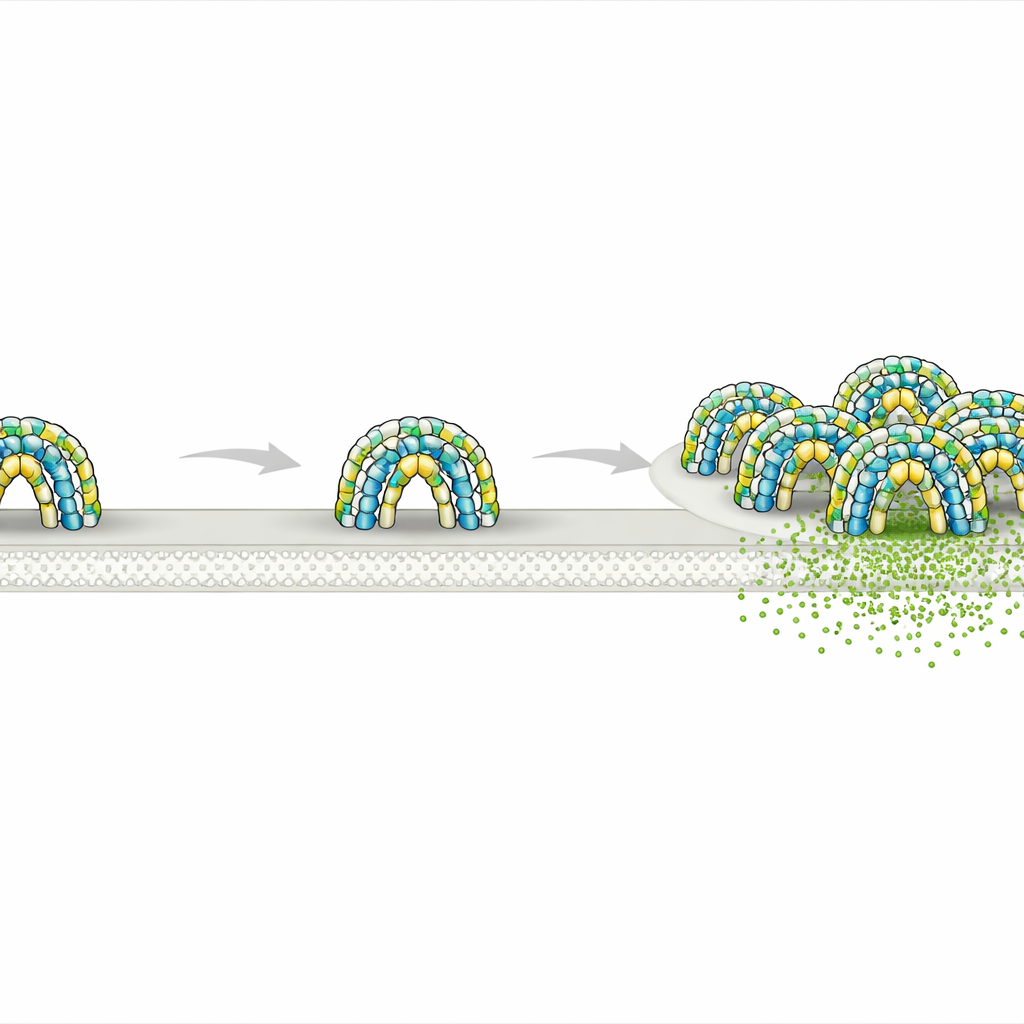
Bliższe spojrzenie na maleńkie sąsiedztwa błonowe
Biolodzy od dawna wiedzą, że błony komórkowe nie są jednorodne. Lipidy i białka grupują się w małe płaty, które działają jak odruchowe stanowiska pracy do określonych zadań, takich jak komunikacja czy sortowanie ładunku. Flotyllina‑1 i flotyllina‑2 to dwa białka, które niemal zawsze oznaczają takie płaty, tworząc jasne punkty na powierzchni komórki i biorąc udział w endocytozie — procesie, w którym komórki wciągają materiał do wnętrza — a także w sygnalizacji i transporcie białek. Nikt jednak nie wiedział, jak dokładnie wyglądają struktury flotyllin ani jak wyznaczają własne terytorium na błonie.
Wykorzystując wysokorozdzielczą kriomikroskopię elektronową na oczyszczonych ludzkich białkach, badacze odkryli, że flotyllina‑1 i flotyllina‑2 składają się w niezwykle duży kompleks złożony z 44 kopii białek, naprzemiennie obu typów. Razem tworzą sztywną kopułę osadzoną po wewnętrznej stronie błony. Podstawa tej kopuły zbudowana jest z segmentów kotwiczących w błonie, bogatych w hydrofobowe aminokwasy i przyczepy lipidowe, które częściowo wnikają w błonę. Powyżej długie helikalne trzonki tworzą ciasno upakowany ścienny walec, a dach z zazębiających się odcinków białkowych zamyka strukturę. Pierścień flotyllin u podstawy wyznacza okrągłą płytkę błony o średnicy około 30 nanometrów — w zasadzie ogrodzając mały dysk błony oraz przestrzeń tuż nad nim.
Elastyczne kopuły widziane w żywych komórkach
Aby sprawdzić, czy takie kopuły występują w prawdziwych komórkach, zespół zmodyfikował ludzkie limfocyty T tak, by produkowały fluorescencyjnie znakowane flotylliny‑1 i ‑2, a następnie obrazował je kombinacją mikroskopii świetlnej i kriotomografii elektronowej. Zaobserwowali puste, kopułowate struktury przylegające do wewnętrznej powierzchni błony plazmatycznej, ściśle odpowiadające kształtowi ustalonemu na oczyszczonych próbkach. Wiele kopuł było nieco zdeformowanych lub częściowo otwartych, a niektóre zawierały dodatkowe gęstości wewnątrz, prawdopodobnie reprezentujące inne białka tymczasowo uwięzione pod dachem. W niektórych rejonach kilka kopuł skupiało się razem na płaskich lub zakrzywionych błonach, w tym na endosomach i małych pęcherzykach zewnątrzkomórkowych, co sugeruje, że pojedyncze kopuły mogą łączyć się w większe platformy błonowe. 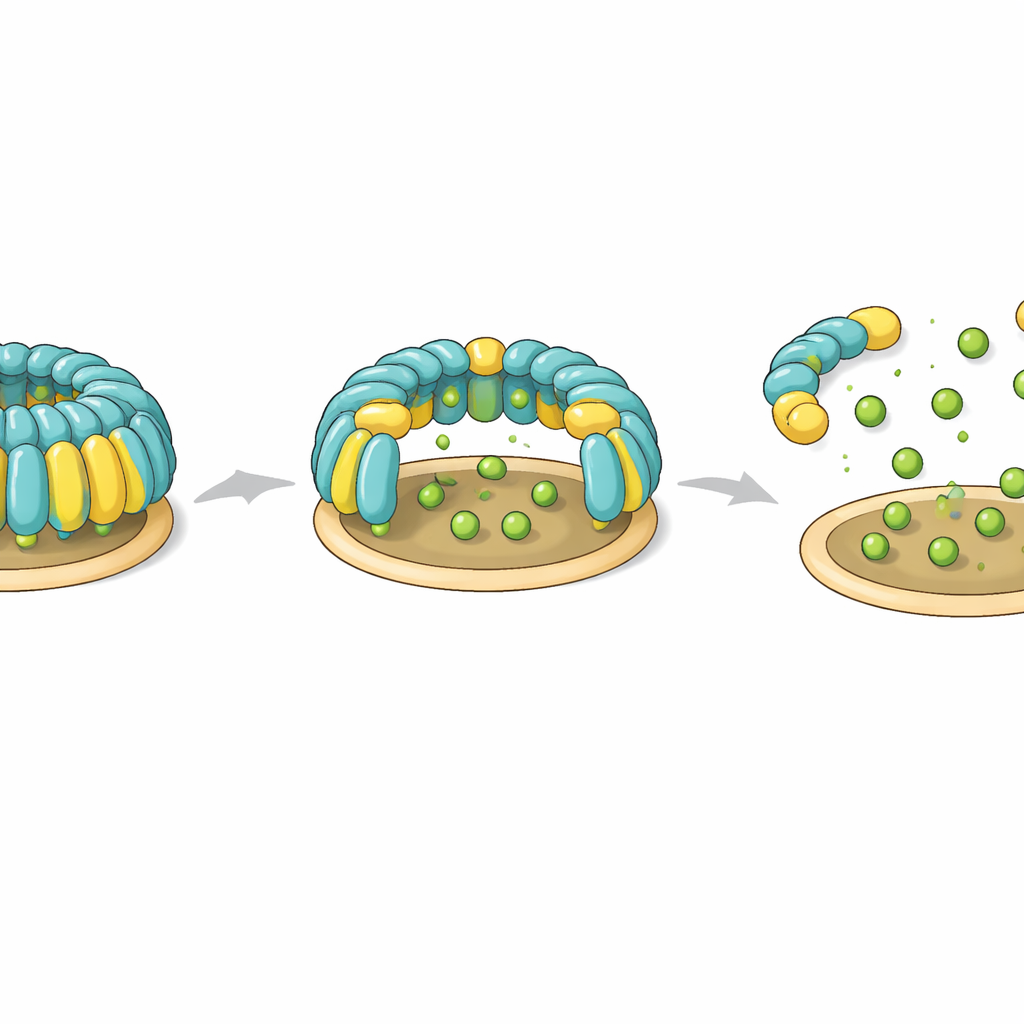
Molekularny wyłącznik do budowy i rozbierania kopuł
Badanie identyfikuje także potencjalne pokrętło kontrolne, którego komórki mogą używać do składania lub rozkładania kopuł flotyllinowych. Dwa specyficzne reszty tyrozyny — po jednej w każdej flotyllinie — znajdują się w pozycjach przypominających zawiasy, które łączą kotwiczącą w błonie podstawę ze ścianą helikalną. W integralnym kompleksie reszty te pomagają tworzyć dopasowane hydrofobowe jądro, które blokuje orientację domen. Gdy badacze wprowadzili mutacje naśladujące dodanie ładunku ujemnego, jakiego efektem byłoby fosforylowanie tych tyrozyn przez enzymy, cała kopuła nie zdołała się zmontować. Mutacje neutralne pozostawiły montaż nietknięty. Te obserwacje sugerują, że fosforylacja w tych miejscach zawiasowych może działać jako odwracalny przełącznik destabilizujący kopułę, otwierając ją lub rozbijając podczas procesów takich jak endocytoza zależna od flotyllin.
Przeformułowanie roli tych domen w kształtowaniu błony
Płatki flotyllin kiedyś uważano głównie za „lipidowe tratwy” bogate w cholesterol i pokrewne tłuszcze. Ku zaskoczeniu, gdy zespół zbadał olbrzymie pęcherze błonowe odklejone z komórek, flotylliny preferowały bardziej płynne, nie‑tratwowe regiony zamiast sztywnych, bogatych w cholesterol obszarów. Analiza lipidów wykazała jedynie skromne wzbogacenie jednej konkretnej cząsteczki, sfingozyny, w kompleksach flotyllin, podczas gdy inne lipidy kojarzone z tratwami nie były skoncentrowane. Wskazuje to na inną zasadę organizacji: zamiast być pasażerami na wcześniej istniejących lipidowych tratwach, kopuły flotyllin same działają jak strukturalne pojemniki, które bocznie segregują fragmenty błony, chwytając pewne białka i lipidy wewnątrz swojego ogrodzonego obszaru.
Dlaczego ta drobna architektura ma znaczenie
Mówiąc w prostszych słowach, kompleksy flotyllin zachowują się jak modułowe daszki, które komórki mogą rozstawić na swojej wewnętrznej powierzchni, by odgrodzić małe okrągłe działki błony. Każda kopuła może gościć odmienny zestaw partnerów białkowych i lipidowych i, poprzez skupianie się z innymi, może budować większe strefy funkcjonalne do sygnalizacji, sortowania ładunku czy formowania pęcherzyków. Ponieważ kopuły są elastyczne i wydają się otwierać oraz zamykać, a ich montaż jest wrażliwy na fosforylację, komórki mogą dynamicznie przebudowywać te struktury w odpowiedzi na sygnały. Ta praca zatem przekształca obraz flotyllin z niejasnych „znaczników tratw” w konkretne elementy architektoniczne, które pomagają rzeźbić błonę w wyspecjalizowane mikro‑stanowiska pracy.
Cytowanie: Lu, MA., Qian, Y., Ma, L. et al. Molecular mechanisms of flotillin complexes in organizing membrane microdomains. Nat Commun 17, 2541 (2026). https://doi.org/10.1038/s41467-026-69197-3
Słowa kluczowe: flotyllina, mikrodomeny błonowe, kriotransmisyjna mikroskopia elektronowa, endocytoza, lipidowe tratwy