Clear Sky Science · pl
Inżynieria metaboliczna biosyntezy doksorubicyny przez optymalizację P450‑partnerów redoksowych i analizę strukturalną DoxA
Dlaczego historia pochodzenia leku przeciwnowotworowego ma znaczenie
Doksorubicyna jest jednym z podstawowych leków współczesnej chemioterapii, stosowanym w leczeniu nowotworów od białaczek po guzy piersi. Mimo dekad użycia sposób jej wytwarzania bywa zaskakująco pośredni: przemysł zwykle konstruuje ją z pokrewnego związku, zamiast pozwolić rodzimemu mikroorganizmowi dokończyć syntezę. W tym badaniu wyjaśniono, dlaczego bakteria produkująca ma trudności z wykonaniem końcowych etapów chemicznych i pokazano, że przeprojektowanie jej wewnętrznego układu może znacząco zwiększyć wydajność produkcji pełnej doksorubicyny, otwierając drogę do bardziej niezawodnych i potencjalnie tańszych dostaw.
Od bakterii glebowych do ratującego życie leku
Doksorubicyna należy do antraklin — rodziny naturalnych cząsteczek wytwarzanych przez bakterie glebowe z rodzaju Streptomyces. Związki te mają sztywny, płaski szkielet węglowy, który wsuwa się między pary zasad DNA, oraz jednostkę cukrową, która wypełnia rowki DNA. Razem te cechy blokują mechanizmy obsługi DNA w komórce i ostatecznie wywołują jej śmierć — przydatne wobec szybko dzielących się komórek nowotworowych. Klasyczny producent, Streptomyces peucetius, naturalnie wytwarza głównie prekursorowy lek daunorubicynę i tylko umiarkowaną ilość bardziej skutecznej doksorubicyny, która różni się jedynie jednym dodatkowymi ugrupowaniem zawierającym tlen. Ta drobna zmiana strukturalna dramatycznie poprawia aktywność, lecz okazuje się zaskakująco trudna do osiągnięcia przez mikroba w sposób wydajny.
Znajdowanie właściwego okablowania elektrycznego wewnątrz komórki
Krytyczny enzym, który wykonuje trzy ostatnie etapy utleniania na szkielecie leku, nazywa się DoxA i należy do rodziny cytochromów P450. Jak miniaturowa fabryka chemiczna, DoxA potrzebuje stałego dopływu elektronów, by aktywować tlen i wprowadzać nowe atomy tlenu do cząsteczki leku. Wewnątrz bakterii elektrony są dostarczane przez przekaźnik pomocniczych białek znanych jako partnerzy redoksowi. Genom S. peucetius zawiera kilka kandydatów, co utrudnia określenie, które z nich faktycznie współpracują z DoxA. Porównując aktywność genów i metabolizm w szczepie referencyjnym, mutancie bogatym w daunorubicynę oraz mutancie bogatym w doksorubicynę, badacze wytypowali jeden ferredoksyn (Fdx4) i jedną ferredoksyn‑reduktazę (FdR3) jako naturalnych partnerów. Odtworzenie tej trójki w reakcjach in vitro potwierdziło, że DoxA działa najlepiej, gdy jest podłączony do tego konkretnego łańcucha transferu elektronów — podobnie jak dopasowanie właściwego adaptera zasilania do urządzenia.
Uwolnienie enzymu od samonakładanego spowolnienia
Nawet przy prawidłowym okablowaniu elektrycznym DoxA ma tendencję do zastoju na ostatnim etapie przekształcającym daunorubicynę w doksorubicynę. Wcześniejsze prace sugerowały, że sam produkt może zatykać enzym. Zespół zwrócił się ku sąsiedniemu genowi, dnrV, którego funkcja była niejasna. Testy biochemiczne wykazały, że białko DnrV silnie wiąże różne cząsteczki antraklinowe, w tym doksorubicynę, bez chemicznej modyfikacji ich. Dodanie DnrV do reakcji z DoxA znacznie poprawiło przebieg reakcji, umożliwiając pełną konwersję prekursorów do końcowego leku i ograniczając szkodliwe reakcje uboczne. W praktyce DnrV działa jak wewnętrzny gąbka, która pochłania świeżo wytworzoną doksorubicynę, zapobiegając blokowaniu enzymu lub uszkodzeniom DNA w komórce produkującej.
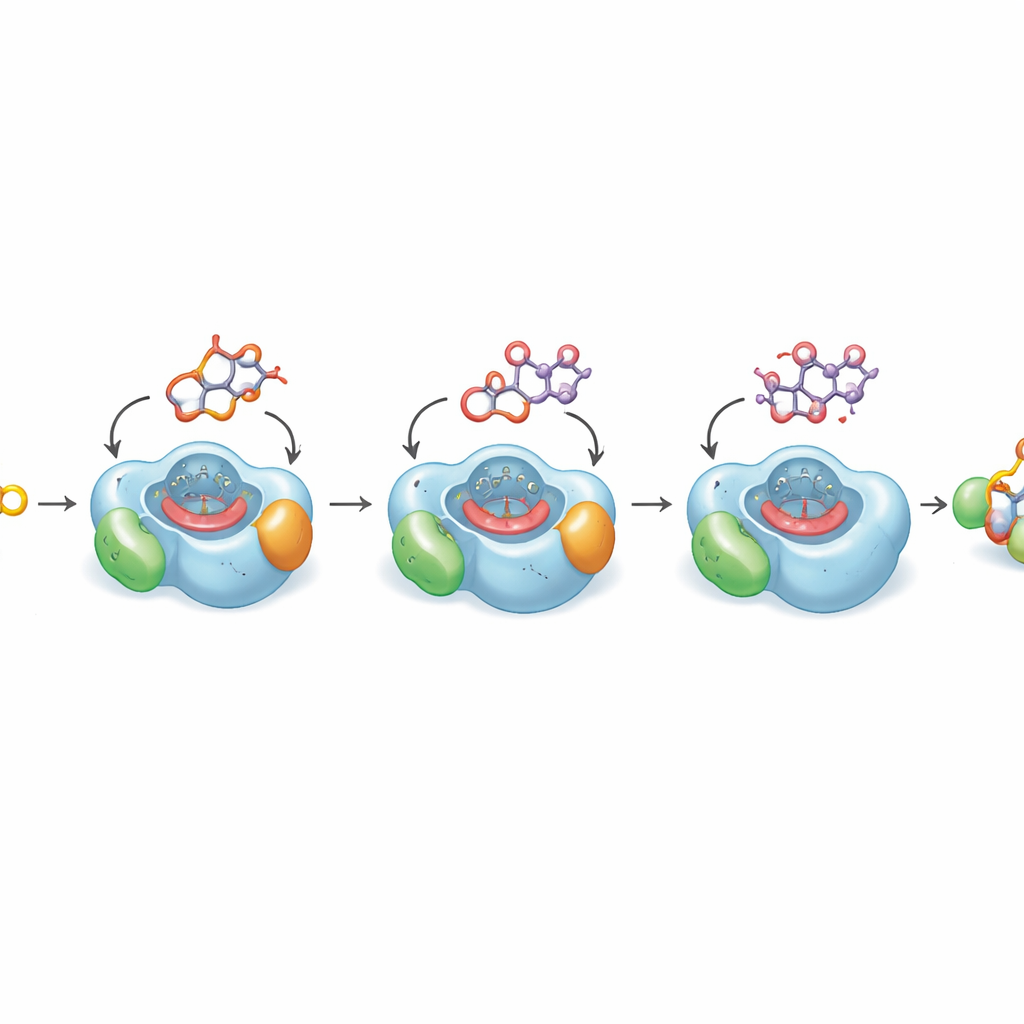
Wyjaśnienie, dlaczego ostatni etap jest tak wolny
Aby zrozumieć, dlaczego kluczowe ostatnie utlenianie przebiega naturalnie powoli, autorzy rozwiązywali struktury krystaliczne DoxA w wysokiej rozdzielczości związane z trzema kolejnymi pośrednimi produktami. Struktury te ukazują, jak płaskie jądro leku i dołączony do niego cukier mieszczą się w ciasnej kieszeni nad grupą hemową enzymu — reaktywnym centrum metalicznym przeprowadzającym utlenianie. Dla wcześniejszych etapów atom węgla do modyfikacji leży blisko hemu w idealnej pozycji do reakcji. Jednak w końcowym substracie, daunorubicynie, fragment cząsteczki, który musi zostać zhydroksylowany, odgina się od hemu do niewielkiej oleistej wnęki — układ, który obliczenia kwantowe pokazują jako energetycznie preferowany. Symulacje komputerowe na skalę mikrosekund potwierdzają, że cząsteczka tylko okazjonalnie przyjmuje produktywną konformację sprzyjającą ostatniemu wstawieniu tlenu. To strukturalne uprzedzenie tłumaczy, dlaczego konwersja do doksorubicyny jest z natury nieefektywna.
Budowanie lepszego szczepu wytwarzającego doksorubicynę
Uzbrojeni w te wnioski, badacze racjonalnie przeprojektowali bakterię zamiast polegać na losowej mutagenezie. Wprowadzili gen naprawy DNA, aby ustabilizować produkcję, następnie umieścili dodatkowe kopie doxA, optymalnych partnerów redoksowych fdx4 i fdr3 oraz pomocniczego białka wiążącego dnrV pod starannie dobranymi promotorami, aby zrównoważyć ich poziomy. Dostosowali też warunki hodowli i użyli specjalnych żywic do pochłaniania toksycznych i lepkich prekursorów. W kolbach laboratoryjnych i 20‑litrowym bioreaktorze najlepszy skonstruowany szczep wyprodukował 336 miligramów doksorubicyny na litr hodowli z relacją 81:19 doksorubicyna do daunorubicyny — wzrost o około 180% w porównaniu z wyjściowym szczepem i znacznie czystsza mieszanina produktów.
Co to oznacza dla przyszłych dostaw leków przeciwnowotworowych
Analizując zarówno system wsparcia elektronicznego, jak i trójwymiarową strukturę kluczowego enzymu, ta praca wyjaśnia, dlaczego medycznie istotny mikroorganizm słabo radzi sobie z produkcją naszej najcenniejszej antrakliny. Dopasowanie DoxA do jego naturalnych partnerów redoksowych, dodanie białka pomocniczego wiążącego lek i ponowne zbalansowanie ekspresji genów przekształciły niechętnego producenta w wydajnego. Choć dalsze strojenie enzymu mogłoby jeszcze przyspieszyć końcowy etap chemiczny, badanie to już przybliża w pełni biologiczną produkcję doksorubicyny do przemysłowej realności. Dla pacjentów i systemów opieki zdrowotnej takie postępy mogą przełożyć się na bezpieczniejszy, skalowalny i bardziej opłacalny dostęp do podstawowego leku chemioterapeutycznego.
Cytowanie: Koroleva, A., Artukka, E., Yamada, K. et al. Metabolic engineering of doxorubicin biosynthesis through P450-redox partner optimization and structural analysis of DoxA. Nat Commun 17, 2358 (2026). https://doi.org/10.1038/s41467-026-69194-6
Słowa kluczowe: produkcja doksorubicyny, biosynteza antraklin, inżynieria enzymów, mikrobowa produkcja leków, cytochrom P450