Clear Sky Science · pl
Aktywacja nietypowej kinazy białkowej C powoduje wydalanie glukozy przez jelito w cukrzycy
Zamiana jelita w zawór odprowadzający cukier
U osób z cukrzycą we krwi krąży zbyt dużo cukru. Operacje bariatryczne, takie jak bypass żołądkowy, potrafią zaskakująco szybko przywrócić prawidłowy poziom glukozy, nawet zanim pacjent straci znaczną wagę, ale mechanizm tego zjawiska długo pozostawał tajemnicą. To badanie ujawnia jelitowy „zawór cukrowy” — mechanizm, dzięki któremu jelito wyciąga glukozę z krwi i odprowadza część z niej z powrotem do wnętrza przewodu pokarmowego — sugerując nowy cel farmakologiczny, który mógłby naśladować korzyści operacji bez potrzeby zabiegu.
Dlaczego operacja tak szybko zmienia poziom cukru we krwi
Lekarze od dawna wiedzą, że metoda Roux-en-Y, powszechna operacja odchudzająca, jest też jedną z najskuteczniejszych terapii cukrzycy typu 2. Krótko po zabiegu poziom glukozy u pacjentów często poprawia się dramatycznie, jeszcze zanim znacząco stracą na wadze. Wcześniejsze prace tego zespołu wykazały, że po bypassie niektóre odcinki jelita zaczynają działać jak gąbka, wchłaniając glukozę z krwi i uwalniając jej część do światła jelita. To nietypowe zachowanie, nazwane wydalaniem glukozy przez jelito, wydawało się zależeć od białka transportującego GLUT1. Kluczowe pytanie brzmiało: jaki molekularny wyłącznik nakazuje jelitu przełączyć się na tryb oczyszczania cukru?
Wykorzystanie dużych danych do znalezienia molekularnego wyłącznika
Aby znaleźć ten wyłącznik, badacze użyli dużej, komputerowej platformy odkrywania leków opartej na Connectivity Map — bazie danych opisującej, jak tysiące związków wpływa na aktywność genów w komórkach. Porównali wzorce ekspresji genów z pięciu sytuacji, w których wydalanie glukozy przez jelito jest wysokie — w tym tkanek od szczurów po zabiegu i komórek traktowanych sygnałem wzrostowym jelita — z wzorcami wywołanymi przez znane leki. Jedna klasa związków wyróżniała się konsekwentnie: aktywatory kinazy białkowej C (PKC), rodziny enzymów przekazujących sygnały wewnątrzkomórkowe. W dalszym badaniu zespół skupił się na podgrupie „nietypowej” PKC, zwłaszcza na enzymie PKCζ, którego aktywność w komórkach jelitowych najlepiej odpowiadała stanowi podobnemu do tego po bypassie, sprzyjającemu wydalaniu glukozy.
Pompka cukrowa w komórkach jelitowych w działaniu
Przyglądając się pojedynczym komórkom jelitowym za pomocą sekwencjonowania RNA pojedynczych komórek, autorzy stwierdzili, że po operacji bypass rośnie zarówno PKCζ, jak i GLUT1 w konkretnych komórkach wchłaniających składniki odżywcze wyściełających dalsze odcinki jelita cienkiego. W hodowlach komórkowych i w ludzkich organoidach jelitowych sztuczne zwiększenie PKCζ lub leczenie prostratyną — związkiem roślinnym bezpiecznie aktywującym te nietypowe PKC — powodowało przemieszczenie GLUT1 na powierzchnię komórek. Tam GLUT1 działał jak dwukierunkowa pompa: pobierał więcej glukozy ze strony komórek zwróconej do krwi i umożliwiał nadmiarowi glukozy opuszczenie komórki do światła jelita. Co ważne, to przekierowanie cukru nie przyspieszyło znacząco samego spalania glukozy przez komórki (glikolizy), co wskazuje, że główny efekt polegał na usuwaniu glukozy, a nie na zwiększaniu produkcji energii.
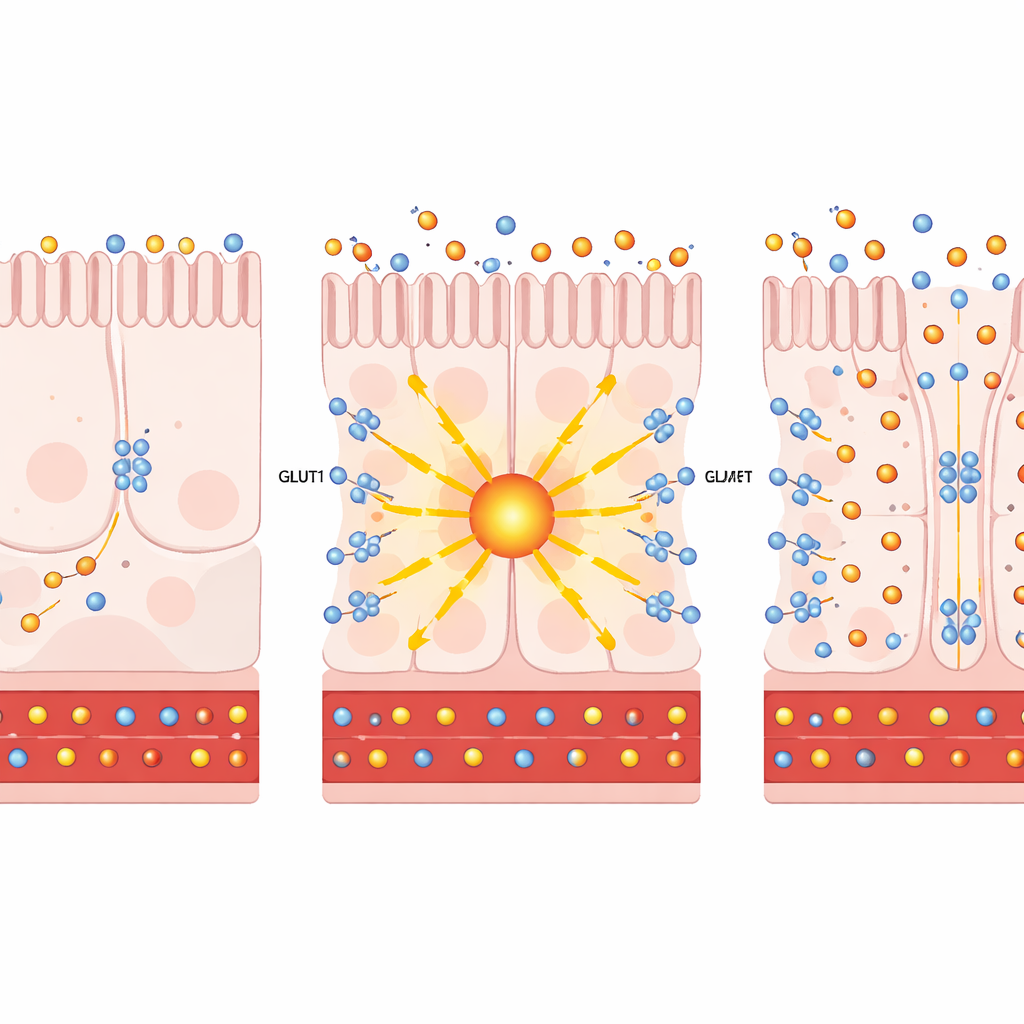
Od komórek do myszy: naśladowanie operacji bez skalpela
Zespół sprawdził następnie, czy aktywacja tej ścieżki u żywych zwierząt poprawi przebieg cukrzycy. U otyłych, opornych na insulinę myszy dostarczenie dodatkowego PKCζ specyficznie do jelita spowodowało wolniejszy przyrost masy, niższy poziom glukozy na czczo i lepszą tolerancję glukozy. Śledzenie radioaktywnymi znacznikami glukozy wykazało większe pochłanianie cukru przez dalsze odcinki jelita i jego wypłukiwanie do światła jelita. Podobne wyniki zaobserwowano w modelach mysich z cukrzycą leczonych prostratyną: zyskiwały mniej masy, lepiej radziły sobie z obciążeniem cukrem i kierowały więcej glukozy do przewodu pokarmowego, bez zmian poziomu insuliny, spożycia pokarmu ani integralności bariery jelitowej. W preparatach tkankowych GLUT1 pojawiał się zarówno po stronie zwróconej do krwi, jak i po stronie skierowanej do światła jelita — idealnie usytuowany, by pobierać cukier z krążenia i wypychać go do jelita.
Co to może znaczyć dla przyszłej opieki nad cukrzycą
Dla osoby niebędącej specjalistą kluczową informacją jest to, że jelito można przekształcić w kontrolowaną drogę ucieczki dla nadmiaru cukru z krwi. Poprzez aktywację specyficznego enzymu w komórkach jelitowych — nietypowej PKC — badacze przekonali komórki do przemieszczenia większej liczby nosników GLUT1 na ich powierzchnię, sprawiając, że zachowują się jak odwracalny odpływ: pobierają cukier z krwi i odprowadzają część z powrotem do jelita. U myszy takie jelitowe usuwanie glukozy poprawiło poziomy cukru i ograniczyło przyrost masy bez nadmiernej stymulacji insuliny, zmiany apetytu czy uszkodzenia jelita. Chociaż prostratyna i związki pokrewne nie są jeszcze zatwierdzonymi lekami na cukrzycę, praca ta wskazuje ścieżkę aPKC–GLUT1 jako obiecujący cel dla przyszłych leków, które mogłyby częściowo odtworzyć metaboliczne korzyści bypassu żołądkowego bez konieczności operacji.
Cytowanie: Kang, C.W., Hong, ZY., Oh, J.H. et al. Atypical protein kinase C activation drives intestinal glucose excretion in diabetes mellitus. Nat Commun 17, 2417 (2026). https://doi.org/10.1038/s41467-026-69193-7
Słowa kluczowe: wydalanie glukozy przez jelito, cukrzyca typu 2, nośnik GLUT1, nietypowa kinaza białkowa C, prostratyna