Clear Sky Science · pl
Autokrynny sygnał TGFβ1 wywołany przez MerTK reguluje odpowiedź mikrogleju na neurodegenerację
Jak sprzątaczki mózgu kształtują przebieg choroby
Gdy komórki nerwowe w mózgu i nerwie wzrokowym obumierają, pozostawiają po sobie ślad szczątków. Specjalistyczne komórki układu odpornościowego zwane mikroglejem działają jak sprzątaczki mózgu, pochłaniając te resztki. Mikroglej robi jednak więcej niż tylko sprząta: jego reakcja może albo chronić obwody nerwowe, albo pogorszyć przebieg chorób, takich jak choroba Alzheimera. W tym badaniu odkryto ukrytą pętlę autokomunikacji wewnątrz mikrogleju, uruchamianą przez szczątki obumierających włókien nerwowych, która pomaga określić siłę reakcji tych komórek na uszkodzenie.
Wyzwalacz ukryty w obumierających włóknach nerwowych
Aby zbadać ten proces, naukowcy użyli modelu mysiego, w którym nerw wzrokowy jest zmiażdżony, powodując degenerację długich wypustek neuronów oka bez zabijania ich ciał komórkowych. Pozwala to czysto wyizolować następstwa rozpadu aksonów. Na powierzchni tych degenerujących włókien lipidowy związek odwraca się na zewnątrz i działa jako sygnał „zjedz mnie” dla pobliskiego mikrogleju. Te sygnały są wykrywane przez receptor na mikrogleju zwany MerTK, jeden z niewielu białek rozpoznających szczątki. Poprzez selektywne usunięcie MerTK w mikrogleju zespół wykazał, że bez tego receptora mikroglej nie uruchamiał zwykłej reakcji na uraz: dzielił się mniej, poruszał się mniej i włączał mniej genów związanych z kontrolą uszkodzeń i stanem zapalnym.
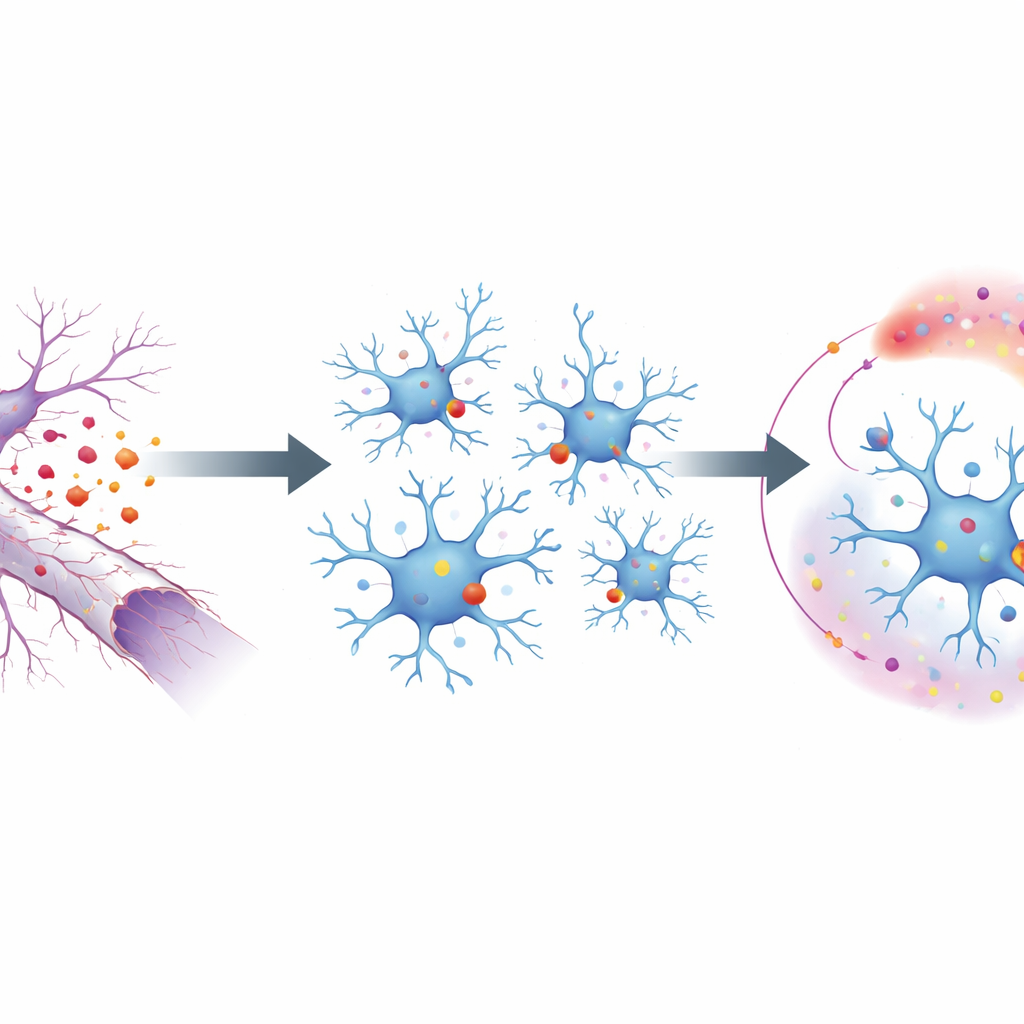
Od sygnału powierzchniowego do reprogramowania genetycznego
Patrząc wewnątrz mikrogleju, naukowcy prześledzili, jak sygnał z MerTK na powierzchni przekształca się w zmiany aktywności genów. Stwierdzili, że MerTK aktywuje przekaźnik molekularny zwany fosfolipazą C, który z kolei wzmacnia dwie główne białka kontrolne w jądrze — PU.1 i IRF8. Czynniki te działają jak majstrowie na linii produkcyjnej mikrogleju, włączając wiele genów potrzebnych do stanu aktywowanego. Dzięki mapom wiązania DNA zespół odkrył, że PU.1 i IRF8 wiążą się bezpośrednio ze specyficznym miejscem w genie kodującym TGFβ1, potężne białko sygnałowe. Gdy to miejsce wiązania zostało zmienione tak, że „majstrowie” nie mogli się tam zadokować, mikroglej w uszkodzonych nerwach nie był w stanie zwiększyć produkcji TGFβ1, mimo że inne funkcje podstawowe pozostały nienaruszone.
Pętla autoodżywiania się mikrogleju
Następne pytanie brzmiało, co właściwie robi TGFβ1 w tym kontekście. Badanie pokazuje, że mikroglej produkuje TGFβ1, a następnie sam na niego reaguje, tworząc pętlę autokrynną, czyli samowiedzącą. Gdy TGFβ1 lub jego receptory zostały genetycznie usunięte wyłącznie z mikrogleju, uraz nadal powodował degenerację aksonów, ale mikroglej już nie wykazywał pełnego programu aktywacji. Mniej się proliferował i wyrażał mniej genów odpowiedzi na uszkodzenie i zapalnych, chociaż wiele markerów tożsamości homeostatycznej nadal było tłumionych przez inne sygnały. Kluczowa cząsteczka będąca spadkobiercą sygnalizacji TGFβ, fosforylowany SMAD2, pojawiała się specyficznie w jądrach mikrogleju po urazie i w dużej mierze znikała po usunięciu TGFβ1 lub jego receptorów, co potwierdza zerwanie pętli autokrynnej.
Od mysiego nerwu wzrokowego do mózgów chorych na Alzheimera
Aby sprawdzić, czy ta ścieżka ma znaczenie poza sztucznym modelem urazu, autorzy zbadali powszechnie stosowany mysiego model choroby Alzheimera. U tych zwierząt mikroglej skupiający się wokół blaszek amyloidowych wykazywał wysokie poziomy PU.1, IRF8, TGFβ1 i aktywnej sygnalizacji TGFβ, co odzwierciedlało obserwacje w nerwie wzrokowym. Zespół zwrócił się następnie do danych ludzkich z pojedynczo-jądrowego sekwencjonowania RNA tkanki mózgowej od pacjentów z chorobą Alzheimera. Tam mikroglej wyróżniał się jako główne komórki wyrażające ludzkie odpowiedniki MerTK, PU.1, IRF8 i TGFB1. W sekcjach mózgów pośmiertnych pacjentów mikroglej także wykazywał silne oznaki aktywnej sygnalizacji TGFβ, w przeciwieństwie do tkanek od dawców kontrolnych. Razem te obserwacje wskazują, że ta sama pętla autokomunikacji działa w ludzkiej chorobie.
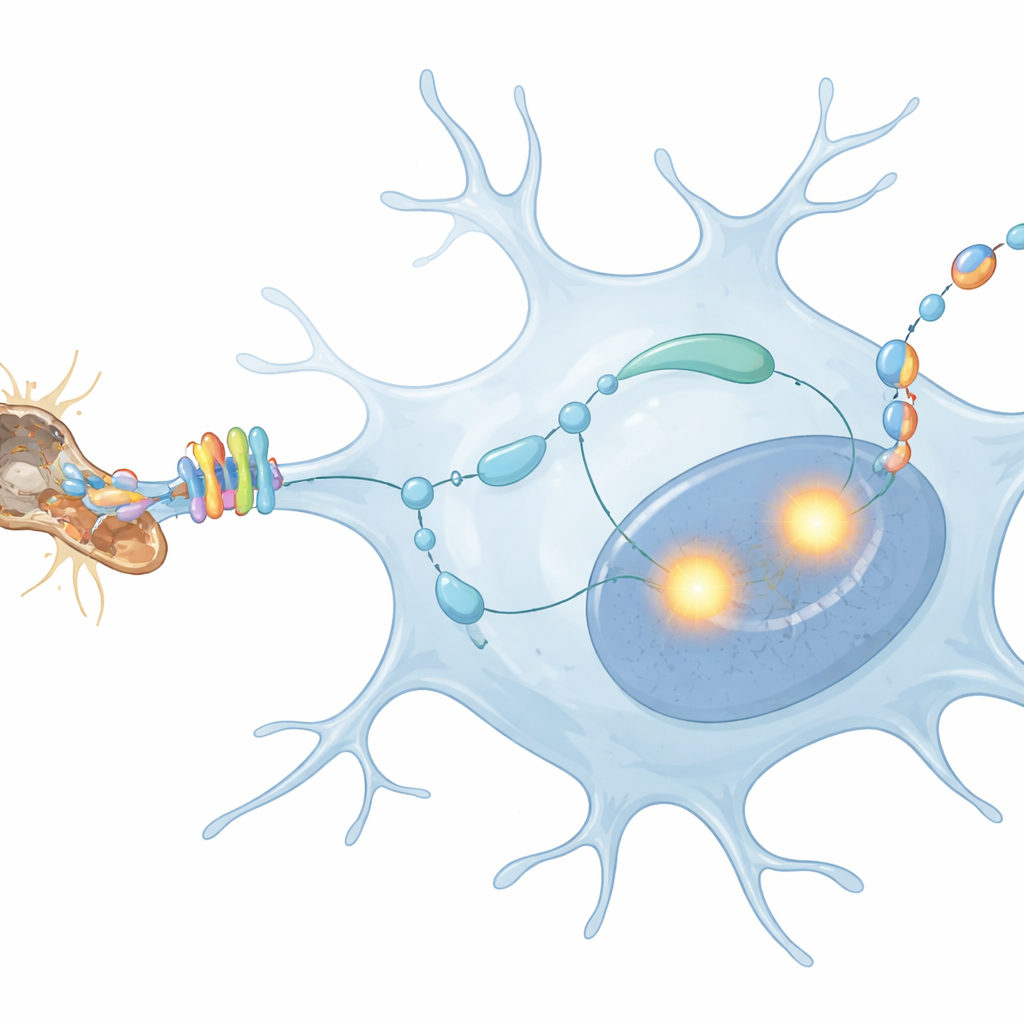
Dlaczego ta wewnętrzna rozmowa ma znaczenie dla zdrowia mózgu
Praca ujawnia łańcuch zdarzeń, w którym szczątki degenerujących włókien nerwowych aktywują MerTK na mikrogleju, co następnie wzmacnia PU.1 i IRF8, które z kolei napędzają produkcję TGFβ1 przez mikroglej — a ten sygnał zwrotny oddziałuje na same komórki. Ta wewnętrzna rozmowa wzmacnia i utrzymuje ich odpowiedź na neurodegenerację. Dla czytelnika nietechnicznego kluczowe przesłanie jest takie: komórki „sprzątające” mózgu nie są jedynie biernymi porządkowaczami; aktywnie nasłuchują własnych sygnałów, a ta pętla zwrotna może wpływać na to, czy ich działania chronią neurony, czy przyczyniają się do postępu chorób takich jak Alzheimer. Zrozumienie i ewentualne modulowanie tego obwodu może otworzyć nowe drogi do łagodzenia szkodliwego zapalenia przy jednoczesnym zachowaniu korzystnego sprzątania przez mikroglej.
Cytowanie: Huang, Y., Deng, Z., Zhou, Z. et al. MerTK-triggered TGFβ1 autocrine signal regulates microglial response to neurodegeneration. Nat Commun 17, 2312 (2026). https://doi.org/10.1038/s41467-026-69189-3
Słowa kluczowe: mikroglej, neurodegeneracja, choroba Alzheimera, zapalanie mózgu, sygnalizacja TGF-beta