Clear Sky Science · pl
Mechanizm pompowania Na+ napędzany reakcjami redoks w dehydrogenazie NADH-chinonu Vibrio cholerae opiera się na dynamicznych zmianach konformacyjnych
Jak elektrownia cholery stała się celem leków
Bakteria wywołująca cholerę, Vibrio cholerae, przetrwa i rozmnaża się dzięki maleńkiej molekularnej „elektrowni” zakotwiczonej w błonie komórkowej. Niniejsze badanie ujawnia z bezprecedensową szczegółowością, jak jeden z jej kluczowych silników — enzym nazywany Na⁺-NQR — zmienia kształt w trakcie pracy, wypompowując jony sodu na zewnątrz komórki. Zrozumienie tej maszynerii molekularnej nie tylko zaspokaja podstawową ciekawość dotyczącą przekształcania pokarmu w użyteczną energię, lecz także wskazuje nowe drogi projektowania antybiotyków, które wyłączają szkodliwe bakterie bez wpływu na komórki ludzkie.
Sodowy silnik w bakteriach
Wiele bakterii morskich i patogennych polega na Na⁺-NQR jako pierwszym ogniwie łańcucha oddechowego — serii reakcji wydobywających energię z substancji odżywczych. Na⁺-NQR osadzony jest w błonie wewnętrznej i pobiera elektrony z cząsteczki paliwowej zwanej NADH, przekazując je przez łańcuch zabarwionych „pomocniczych” cząsteczek (koenzymów) do chinonu, innej małej cząsteczki w błonie. W miarę przepływu elektronów enzym wykorzystuje tę energię do wypychania jonów sodu (Na⁺) z wnętrza na zewnątrz komórki, tworząc gradiencję sodową. Gradient ten działa jak naładowana bateria: napędza silnik wici bakteryjnej do pływania, pomaga w syntezie ATP (waluty energetycznej komórki) oraz wspomaga pobieranie składników i wypompowywanie leków. Ponieważ Na⁺-NQR występuje tylko w bakteriach i znacznie różni się od pokrewnego enzymu w mitochondriach ludzi, stanowi atrakcyjny cel dla wysoce selektywnych antybiotyków.
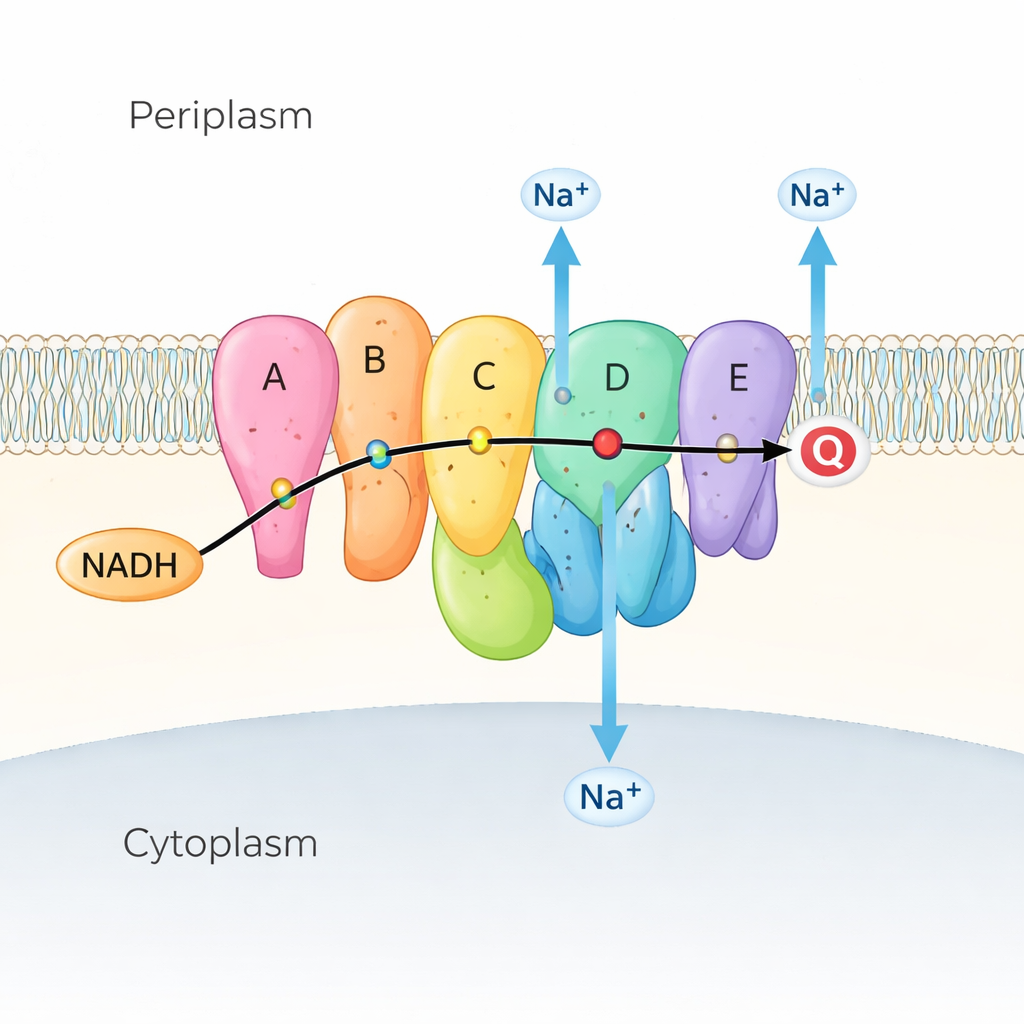
Obserwowanie ruchu maszyny
Poprzednie obrazy rentgenowskie i kryo‑elektronowej mikroskopii pokazały położenie podjednostek i kofaktorów Na⁺-NQR, ale ujawniły też zagadkę: niektóre krytyczne przeskoki elektronów były zbyt dalekie, by mogły zachodzić wydajnie, chyba że białko zmieniło swój kształt. Autorzy podjęli to wyzwanie, utrwalając Na⁺-NQR w wielu nieco różnych stanach. Użyli mutantów usuwających konkretne kofaktory, leków blokujących reakcję na określonych etapach oraz roztworów z i bez sodu. Dzięki wysokorozdzielczej kryo-EM i zaawansowanej analizie obrazów potrafili wyodrębnić i zrekonstruować wiele konformacji tego samego enzymu, skutecznie zamieniając statyczne „migawki” w film jego cyklu pracy.
Elastyczne ramię i przestawny zacisk
Jedno z kluczowych odkryć dotyczy elastycznej podjednostki cytoplazmatycznej, NqrF, która niesie dwa kofaktory przenoszące elektrony. Zespół zidentyfikował trzy pozycje dla jej domeny „podobnej do ferredoksyny” — nazwane „góra”, „środek” i „dół”. W rzadkim, lecz istotnym stanie „dół” mała domena wsuwa się w kieszeń utworzoną przez dwie podjednostki błonowe, NqrD i NqrE, zbliżając swój klaster żelazo‑siarkowy na odległość umożliwiającą przekazanie elektronów dalej. Tymczasem periplazmatyczna (zewnętrzna) podjednostka NqrC działa jak ruchomy zacisk. W jednej konformacji („stabilna”) przylega do innej podjednostki błonowej, NqrB, ustawiona do przekazania elektronów w kierunku końcowego akceptora chinonu. W drugiej („przesuniętej”) NqrC przesuwa się w stronę NqrD/E, przybliżając swój kofaktor flawinowy, by przyjąć elektron z ich centrum żelazo‑siarkowego. Te ruchy pokazują, że NqrF i NqrC zachowują się jak dynamiczni kurierzy, wypełniający duże przerwy w łańcuchu kofaktorów.
Jak zmiany kształtu pompują sód
Rdzeń pompy sodowej leży w parach podjednostek NqrD i NqrE, które tworzą centralny pęk helis przenikających błonę. Na podstawie struktur i symulacji dynamiki molekularnej na poziomie atomowym autorzy pokazują, że gdy klaster żelazo‑siarkowy w NqrD/E ulega redukcji (przyjmuje elektron), powstaje ujemnie naładowane miejsce przyciągające jon Na⁺ i kilka cząsteczek wody z cytoplazmatycznej strony, tworząc przejściową kieszeń wiążącą. Hydrofoobowe aminokwasy powyżej i poniżej tej kieszeni zachowują się jak bramka wewnętrzna i zewnętrzna, kontrolując dostęp do jonu. Gdy NqrD/E przełączają się ze stanu „otwartego do wnętrza” na „otwarte do zewnątrz”, Na⁺ przesuwa się w kierunku periplazmy i zostaje ostatecznie uwolniony w miarę ponownej utlenienia klastra żelazo‑siarkowego. Symulacje pokazują, że Na⁺ pozostaje częściowo uwodniony, ale nigdy nie tworzy ciągłego tunelu wypełnionego wodą, co sugeruje, że enzym jest szczelnie zamknięty i zapobiega niepożądanym przeciekom protonów.
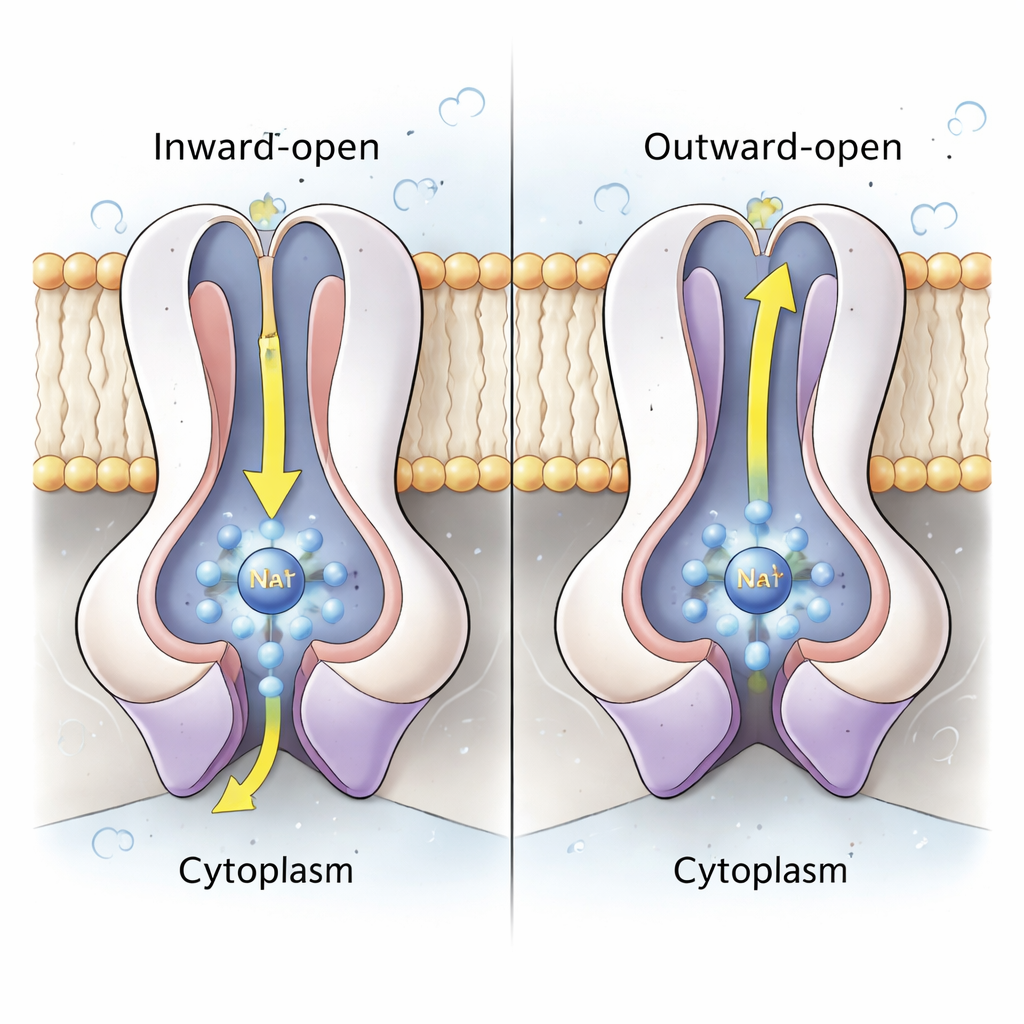
Skorelowany cykl, który utrwala kierunek
Łącząc wszystkie stany strukturalne i symulacje, badacze proponują sześciostopniowy cykl. Najpierw przyłącza się NADH i oddaje elektrony do NqrF, który następnie przekazuje jeden elektron do NqrD/E, wywołując wychwyt Na⁺ z cytoplazmy i załadowanie centralnej kieszeni. Wynikająca z tego zmiana konformacji NqrD/E do formy otwartej na zewnątrz zarówno wypycha Na⁺ do periplazmy, jak i sprzyja przemieszczeniu się NqrC na pozycję umożliwiającą przyjęcie elektronu. Kolejne kroki przenoszą elektrony dalej do końcowych kofaktorów flawinowych i ryboflawinowych, a w końcu do chinonu, który musi otrzymać dwa elektrony, by stać się chinolem. Co ważne, te same zmiany kształtu, które przemieszczają Na⁺, jednocześnie naprzemiennie rozluźniają i usztywniają NqrF i NqrC, sprawiając, że przepływ elektronów w przód jest prawdopodobny tylko wtedy, gdy Na⁺ jest wypompowywany na zewnątrz, a cofanie jest zniechęcane. To sprzężenie pomaga enzymowi pompować Na⁺ przeciw istniejącemu gradientowi, utrzymując „baterię” bakterii naładowaną.
Dlaczego to ma znaczenie dla medycyny i biologii
Dla laika praca ta pokazuje, jak życie buduje misternie zorganizowane maszyny z białek, gdzie drobne zmiany ładunku wywołują duże, użyteczne ruchy. Dla badań nad chorobami zakaźnymi wyjaśnia, że translokacja Na⁺ w Na⁺-NQR zachodzi głównie przez rdzeń NqrD/E, a nie przez wcześniej podejrzewany podjednostkę NqrB. Ta wiedza zawęża miejsce, gdzie przyszłe leki powinny wiązać się, by najskuteczniej zakłócić silnik zasilający Vibrio cholerae i inne patogeny, oszczędzając enzymy ludzkie. Szerzej, badanie dostarcza strukturalnego planu, jak reakcje redoks mogą być połączone z pompami jonowymi — zasada konstrukcyjna, którą natura wielokrotnie wykorzystuje w różnych formach maszynerii bioenergetycznej.
Cytowanie: Ishikawa-Fukuda, M., Seki, T., Kishikawa, Ji. et al. The redox driven Na+-pumping mechanism in Vibrio cholerae NADH-quinone oxidoreductase relies on dynamic conformational changes. Nat Commun 17, 1394 (2026). https://doi.org/10.1038/s41467-026-69182-w
Słowa kluczowe: pompa sodowa, oddychanie bakteryjne, Na+-NQR, kryo-EM, cele antybiotyków