Clear Sky Science · pl
Syntetyczny układ do RNA-czułej pyroptozy oparty na nukleazie‑proteazie CRISPR typu III‑E
Zmiana zabójczych eksplozji komórek w narzędzia celowane
Nasze ciało czasem broni się, powodując, że zakażone lub uszkodzone komórki eksplodują w rodzaj zapalnej autodestrukcji. Ta eksplozja nie tylko usuwa niebezpieczne komórki, lecz także przyciąga układ odpornościowy. Nowe badanie przedstawia syntetyczny obwód genetyczny nazwany DAMAGE, który potrafi odczytywać wiadomości RNA wewnątrz komórki i decydować, czy dana komórka powinna zostać zniszczona. Poprzez połączenie bakteryjnego systemu obronnego z naszymi mechanizmami śmierci komórki, autorzy pokazują sposób selektywnego eliminowania komórek zakażonych wirusem, nowotworowych lub stareńcznych, oszczędzając zdrowe sąsiadki. 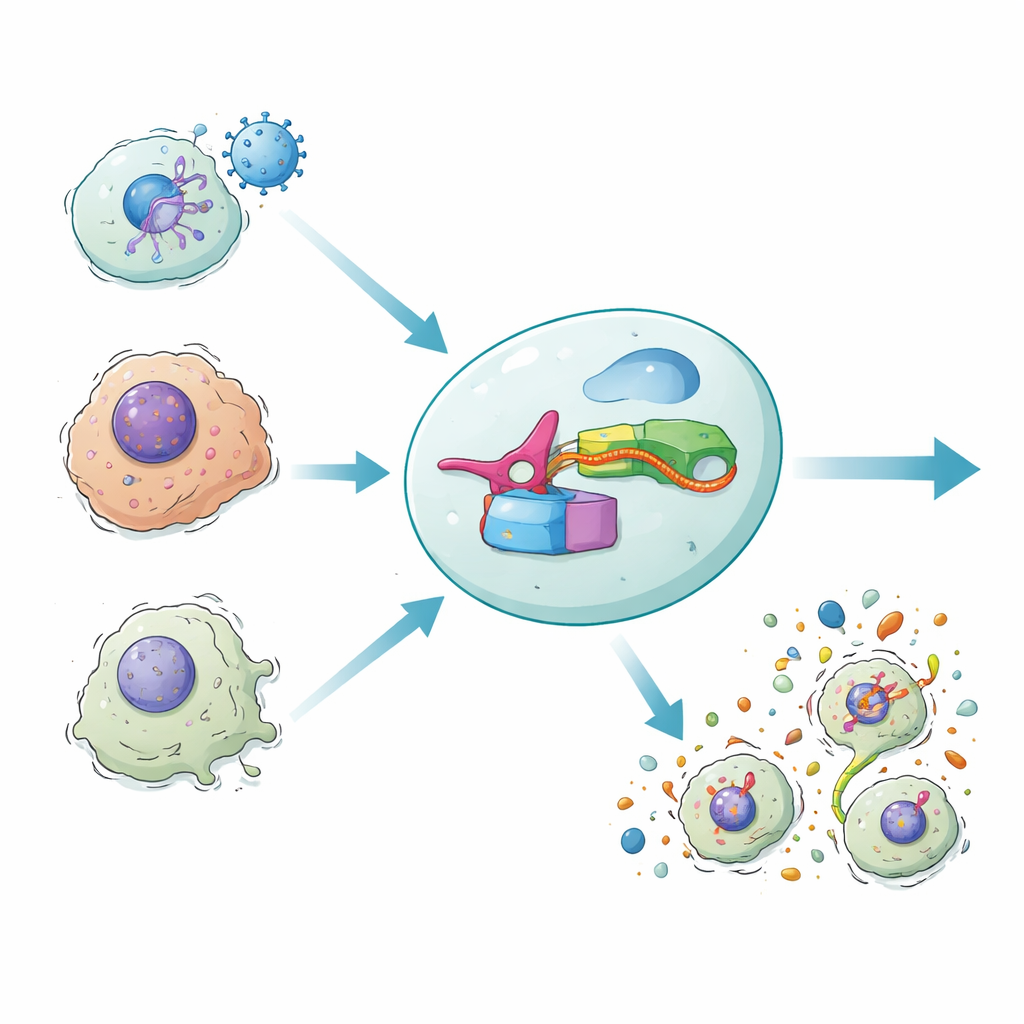
Jak komórki zwykle się wysadzają
W zapalnej śmierci komórki rodzina białek zwanych gasderminami leży w komórkach jak naładowane ładunki. Każda gasdermina ma „zabójczą” przednią połowę, która może przebijać błony komórkowe, oraz tylnią połowę działającą jak „zabezpieczenie”, które powstrzymuje zabójcę. Gdy czujniki odpornościowe wykrywają zagrożenie, enzymy przecinają gasderminy na dwie części, uwalniając przednią połowę do składania porów w błonie komórkowej. Komórka pęcznieje, pęka i wyrzuca sygnały alarmowe, które mobilizują komórki odpornościowe. Ten silny mechanizm pomaga zwalczać infekcje i guzy, ale jego naturalna sieć regulacyjna jest złożona i trudna do przeprogramowania w celach terapeutycznych.
Zapożyczanie bakteryjnej obrony do odczytu RNA
Bakterie wykształciły zwarte moduły obronne znane dziś dzięki technologii CRISPR. Jeden z nich, system typu III‑E, wykorzystuje białko o nazwie Cas7‑11, które przy pomocy krótkiego RNA przewodnika może wiązać konkretne sekwencje RNA. Gdy Cas7‑11 znajdzie zgodny docelowy RNA, aktywuje towarzyszący enzym Csx29, który tnie białko partnera Csx30. Autorzy zauważyli, że Csx30 może działać jako konfigurowalny „zawias” między dowolnymi dwiema częściami białka. Połączyli ten zawias pomiędzy zabójczą i zabezpieczającą połową ludzkich gasdermin, tworząc sztuczne egzekutory, które rozdzielają się tylko wtedy, gdy czujnik podobny do CRISPR wykryje wybrane RNA wewnątrz komórki.
Programowalny przełącznik śmierci dla chorych komórek
Projekt ten, nazwany DAMAGE (Death Manipulation Gene), zbudowano z pięciu elementów: czujnika Cas7‑11, tnącego Csx29, fuzji gasderminy z Csx30, RNA przewodnika i docelowego RNA w komórce. Gdy pojawi się właściwa wiadomość RNA, Cas7‑11 się z nią wiąże, aktywuje Csx29, a Csx29 tnie zawias Csx30 we fuzji białkowej. Zabójcza część gasderminy zostaje uwolniona, wykonuje otwory w błonie, a komórka umiera w zapalnej eksplozji. Zmieniając jedynie RNA przewodnikowy, zespół przekierował DAMAGE na różne cele komórkowe. Pokazali, że rozpoznawał RNA wirusa RSV, wysokiego ryzyka wirusa brodawczaka ludzkiego w komórkach raka szyjki macicy oraz kilka mutacji KRAS napędzających nowotwór, które różniły się od normalnego RNA tylko jedną literą. W każdym przypadku komórki zawierające podejrzane RNA były selektywnie eliminowane, podczas gdy pobliskie komórki kontrolne pozostawały nietknięte. 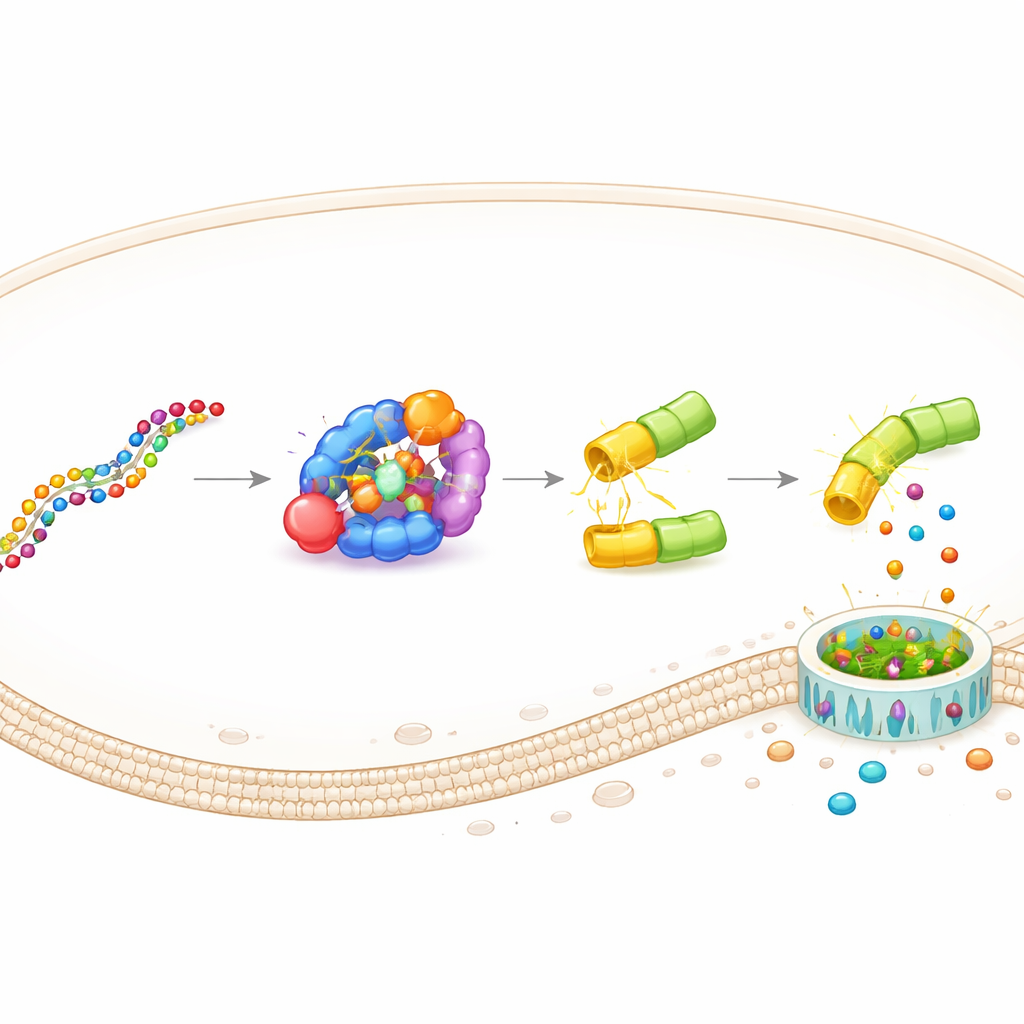
Namierzenie komórek starzejących się
Autorzy sprawdzili także, czy DAMAGE potrafi polować na komórki senescentne — stare lub zestresowane komórki, które przestają się dzielić, lecz gromadzą się w tkankach i przyczyniają do osłabienia i chorób przewlekłych. Takie komórki często podnoszą produkcję dwóch białek‑strażników, p16 i p21. Programując prowadnice przeciw RNA p16 i p21, zespół stworzył wersję nazwaną DAMAGE‑Aging. Ten obwód zabijał komórki z wysokim poziomem tych transkryptów, oszczędzając komórki, w których p16 zostało genetycznie usunięte, potwierdzając, że system odczytuje bieżącą obfitość RNA, a nie stałe zmiany w DNA. Leczenie lekami podnoszącymi poziom p16 lub p21 uczulało komórki na tę ukierunkowaną autodestrukcję.
Opakowanie systemu dla przyszłych terapii
Aby przybliżyć się do zastosowań praktycznych, autorzy skompresowali liczne elementy DNA DAMAGE do uproszczonej konstrukcji, DAMAGE‑Plus, i wykazali, że nadal działała niezawodnie. Następnie przepisali tę konstrukcję na syntetyczne mRNA, zapakowali je w lipoproteinowe nanocząstki podobne do tych używanych w szczepionkach przeciw COVID‑19 i dostarczyli do komórek w hodowlach. Wersja mRNA skutecznie złożyła obwód i wywołała ukierunkowaną zapalną śmierć w komórkach zawierających wirusowe lub nowotworowe RNA. Chociaż cały system wciąż jest duży i przetestowany jedynie w liniach komórkowych, wyniki sugerują, że programowalne, prowadzone przez RNA zabijanie komórek może kiedyś być wdrażane przez wstrzykiwalne formulacje mRNA.
Nowy sposób odczytu i reagowania na wiadomości komórkowe
Mówiąc prosto, DAMAGE to molekularny bramkarz, który sprawdza wewnętrzne „ID” RNA każdej komórki i wyrzuca tylko te, które wyglądają niebezpiecznie — zakażone wirusem, niosące mutacje lub senescentne — zmuszając je do wybuchowej autodestrukcji. Praca demonstruje, że bakteryjne sensory RNA można połączyć z ludzkimi mechanizmami śmierci komórki z dużą precyzją, nawet rozróżniając różnice jednej litery w komunikatach genetycznych. Choć potrzeba jeszcze wiele inżynierii, zanim taki system będzie bezpiecznie użyty u zwierząt czy ludzi, kreśli on potężną nową strategię: odczytywanie bieżącej rozmowy RNA wewnątrz komórek i tłumaczenie jej bezpośrednio na decyzje o życiu lub śmierci.
Cytowanie: He, M., Wang, W., Zhou, H. et al. A synthetic system for RNA-responsive pyroptosis based on type III-E CRISPR nuclease-protease. Nat Commun 17, 2565 (2026). https://doi.org/10.1038/s41467-026-69179-5
Słowa kluczowe: pyroptoza, CRISPR, terapia ukierunkowana na RNA, immunoterapia nowotworowa, starzenie komórek