Clear Sky Science · pl
hnRNPM współpracuje z BCAS2 przy modulowaniu splicingu alternatywnego podczas rozwoju oocytu
Dlaczego jakość komórki jajowej ma znaczenie
Każde ludzkie życie zaczyna się od jednej komórki jajowej, a naukowcy wciąż odkrywają, jak te niezwykle duże komórki przygotowują się do momentu zapłodnienia. Na długo przed przybyciem plemników rosnące komórki jajowe gromadzą tysiące komunikatów RNA, które poprowadzą ich dojrzewanie i pierwsze dni rozwoju zarodka. Badanie to ujawnia, jak mało znane białko, współdziałając z partnerem, precyzyjnie edytuje te komunikaty w komórkach jajowych myszy — oraz co się dzieje, gdy ten system edycji zawodzi.
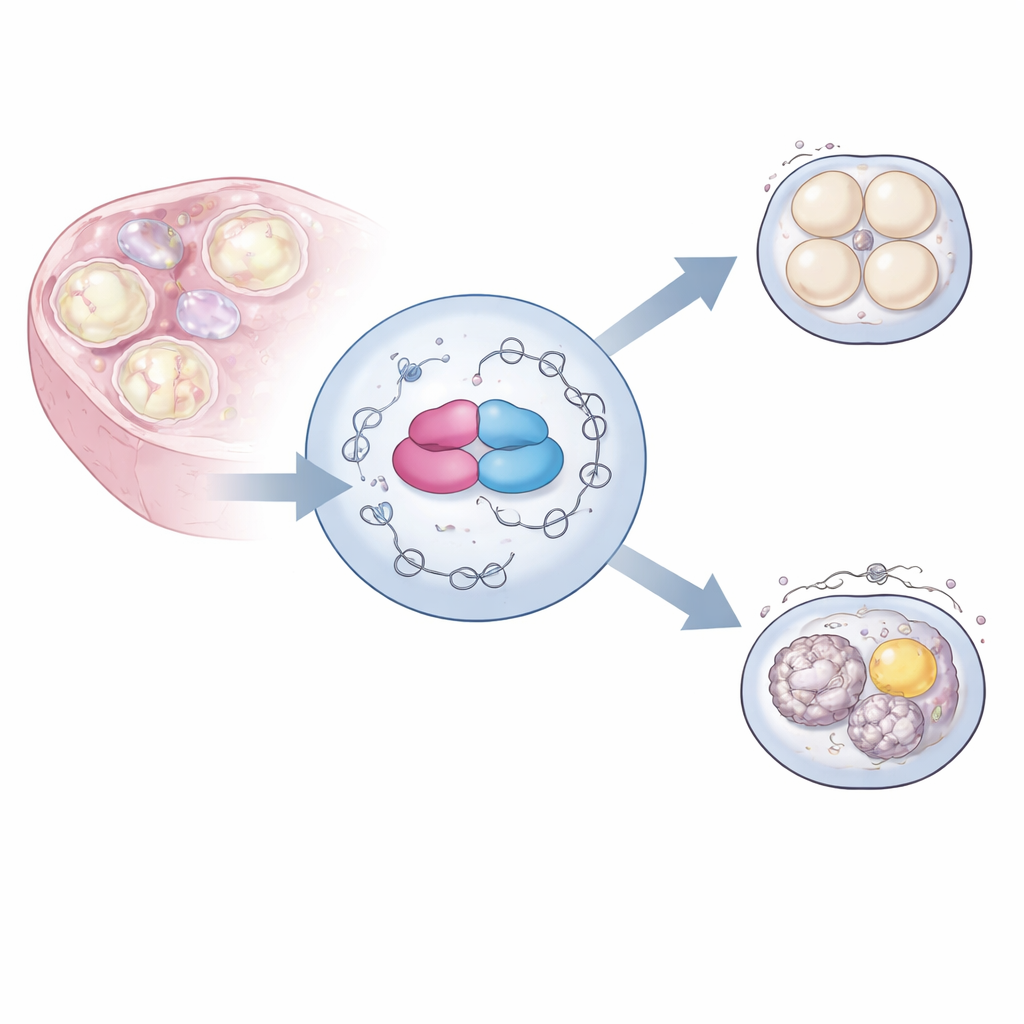
Bramkarze komunikatów genetycznych
Komórki jajowe przez tygodnie rosną w jajniku, podczas gdy ich DNA w dużej mierze pozostaje nieaktywne. W tym czasie akumulują olbrzymią bibliotekę macierzystych komunikatów RNA skopiowanych wcześniej z genomu. Te komunikaty trzeba przycinać i łączyć na różne sposoby — proces nazywany splicingiem alternatywnym — by wytworzyć odpowiednią mieszaninę wariantów białek we właściwych fazach. Autorzy skupili się na białku o nazwie hnRNPM, należącym do dużej rodziny wiążącej RNA, oraz na jego partnerze BCAS2, które są obfite w żeńskim układzie rozrodczym. Wcześniejsze prace sugerowały, że te białka wiążą wiele RNA w komórkach jajowych, ale ich dokładna rola w kształtowaniu płodności pozostawała niejasna.
Co idzie nie tak bez tego „edytora”
Aby zbadać funkcję hnRNPM, zespół zastosował inżynierię genetyczną, usuwając gen Hnrnpm specyficznie z prekursorów komórek jajowych myszy. Jajniki tych samic wyglądały normalnie i produkowały podobną liczbę jaj w porównaniu z kontrolami. Jednak gdy te jaja zapłodniono w laboratorium, niemal nigdy nie rozwijały się dalej niż pierwsze podziały, co czyniło samice całkowicie bezpłodnymi. Dokładniejsze oględziny niedojrzałych jaj ujawniły ciemne grudki w normalnie przejrzystej cytoplazmie. Mikroskopia elektronowa pokazała, że delikatny wewnętrzny ruszt zwany lattice cytoplazmatycznym był w dużej mierze nieobecny, a kluczowe organelle, takie jak mitochondria i krople tłuszczu, były nieprawidłowo skupione, zamiast równomiernie rozproszone. Zmiany te wskazywały na poważne zaburzenie wewnętrznej organizacji komórki jajowej.
Uszkodzony mechanizm podziału komórkowego
Te same mutantne jaja miały też trudności z ukończeniem mejozy — specjalnego podziału komórkowego, który redukuje liczbę chromosomów o połowę. Gdy badacze dojrzewali jaja w hodowli, mogły one zainicjować mejozę, ale zwykle zatrzymywały się przed jej zakończeniem. Pod mikroskopem struktury odpowiadające za rozdzielanie chromosomów — wrzeciona podziałowe — były skręcone, wielobiegunowe lub słabo zakotwiczone. Białko o nazwie pericentrin, które pomaga organizować bieguny wrzeciona, pojawiało się późno i w niewłaściwych miejscach. Wspólnie te defekty oznaczały, że jaja nie mogły prawidłowo ustawiać i rozdzielać chromosomów, co prawdopodobnie jest przyczyną całkowitej porażki rozwojowej po zapłodnieniu.
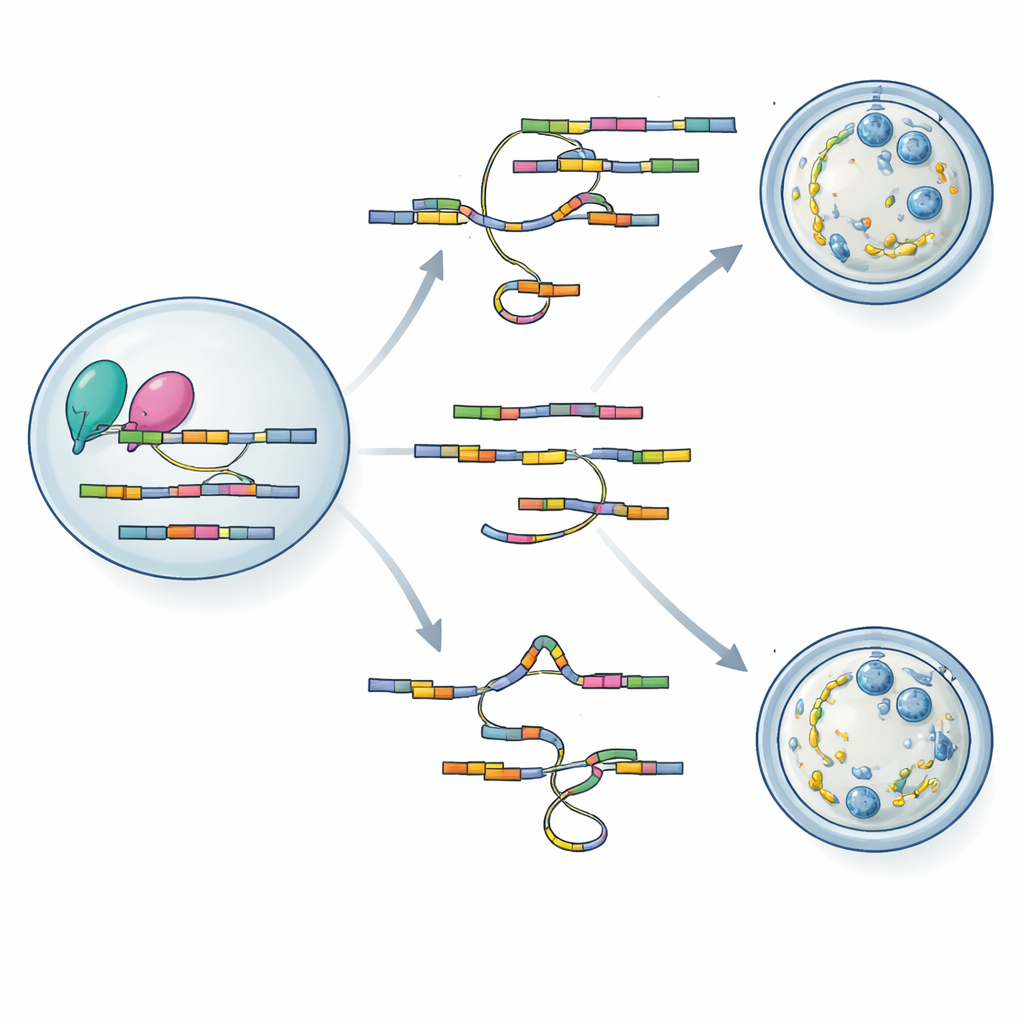
Odczytywanie i przepisywanie instrukcji RNA
Aby zrozumieć, jak utrata hnRNPM prowadzi do tak rozległych defektów, zespół sięgnął po dwa potężne narzędzia sekwencjonowania dostosowane do bardzo małych próbek jaj. Korzystając z SCAN-seq, które odczytuje cząsteczki RNA w pełnej długości z pojedynczych oocytów, odkryli ponad tysiąc zmian splicingowych w mutantnych jajach, w tym wiele wcześniej nieznanych wariantów RNA. Szczególnie dotknięte były geny zaangażowane w budowę lattice cytoplazmatycznego, kontrolę zachowania wrzeciona i regulację cyklu komórkowego mejozy. Druga metoda, LACE-seq, odwzorowała dokładne miejsca, gdzie hnRNPM wiąże się z RNA, ujawniając preferencję dla sekwencji bogatych w GU wewnątrz eksonów. Nakładając oba zestawy danych, autorzy pokazali, że hnRNPM znajduje się bezpośrednio na wielu komunikatach, których splicing zmienia się po utracie białka, wiążąc jego aktywność wiążącą z dokładnością splicingu.
Model współpracy przy kontroli komórki jajowej
Badania interakcji białek wykazały, że hnRNPM fizycznie wiąże się z BCAS2 oraz z podstawowymi składnikami aparatu splicingowego. Obaj partnerzy wiążą wiele tych samych celów RNA i często modyfikują je w podobny sposób, gdy którykolwiek z nich zostaje zaburzony. Co interesujące, utrata hnRNPM zmniejszała poziomy białka BCAS2 i osłabiała przyczepność BCAS2 do wspólnych celów RNA, co sugeruje, że hnRNPM nie tylko edytuje komunikaty, lecz także pomaga stabilizować partnera na tych komunikatach. Autorzy proponują model, w którym hnRNPM i BCAS2 tworzą kompleks współpracujący, który dopasowuje kluczowe macierzyste RNA podczas wzrostu oocytu, zapewniając prawidłowy montaż lattice cytoplazmatycznego i niezawodne podziały mejotyczne.
Co to oznacza dla płodności
Mówiąc prosto, ta praca pokazuje, że molekularny zespół edytorski — hnRNPM i BCAS2 — działa w tle, przygotowując komórki jajowe na życie po zapłodnieniu. Gdy ten zespół jest nieobecny, wewnętrzny szkielet komórki jajowej się zapada, mechanizmy segregacji chromosomów zawodzą, i choć jajo jest wytwarzane w normalnej liczbie, nie jest w stanie podtrzymać rozwoju zarodka. Ponieważ hnRNPM jest wysoce podobny u myszy i u ludzi, wyniki te wskazują na zachowany system kontroli jakości, który może leżeć u podstaw niektórych form niewyjaśnionej żeńskiej niepłodności i oferować nowe punkty wejścia do diagnostyki lub terapii.
Cytowanie: Zhou, S., Liu, D., Gan, S. et al. hnRNPM cooperates with BCAS2 to modulate alternative splicing during oocyte development. Nat Commun 17, 2681 (2026). https://doi.org/10.1038/s41467-026-69176-8
Słowa kluczowe: rozwój oocytu, splicing alternatywny, bezpłodność u kobiet, białka wiążące RNA, lattice cytoplazmatyczny