Clear Sky Science · pl
Ensembles o rozdzielczości atomowej dla białek wewnętrznie nieuporządkowanych z Alphafold
Dlaczego białka zmieniające kształt mają znaczenie
W naszych komórkach znajduje się wiele białek, które nigdy nie przyjmują jednej, sztywnej formy. Te „wewnętrznie nieuporządkowane” białka zachowują się raczej jak wiotkie nitki niż starannie złożone maszyny, a mimo to odgrywają kluczowe role w procesach od sygnalizacji komórkowej po choroby neurodegeneracyjne. Ponieważ nieustannie się poruszają i wyginają, uchwycenie całego ich zestawu kształtów z dokładnością atomową jest niezwykle trudne i zwykle wymaga lat eksperymentów oraz intensywnych obliczeń. W artykule przedstawiono nowy sposób łączenia sztucznej inteligencji i zasad fizyki, który pozwala mapować te niespokojne cząsteczki znacznie wydajniej.
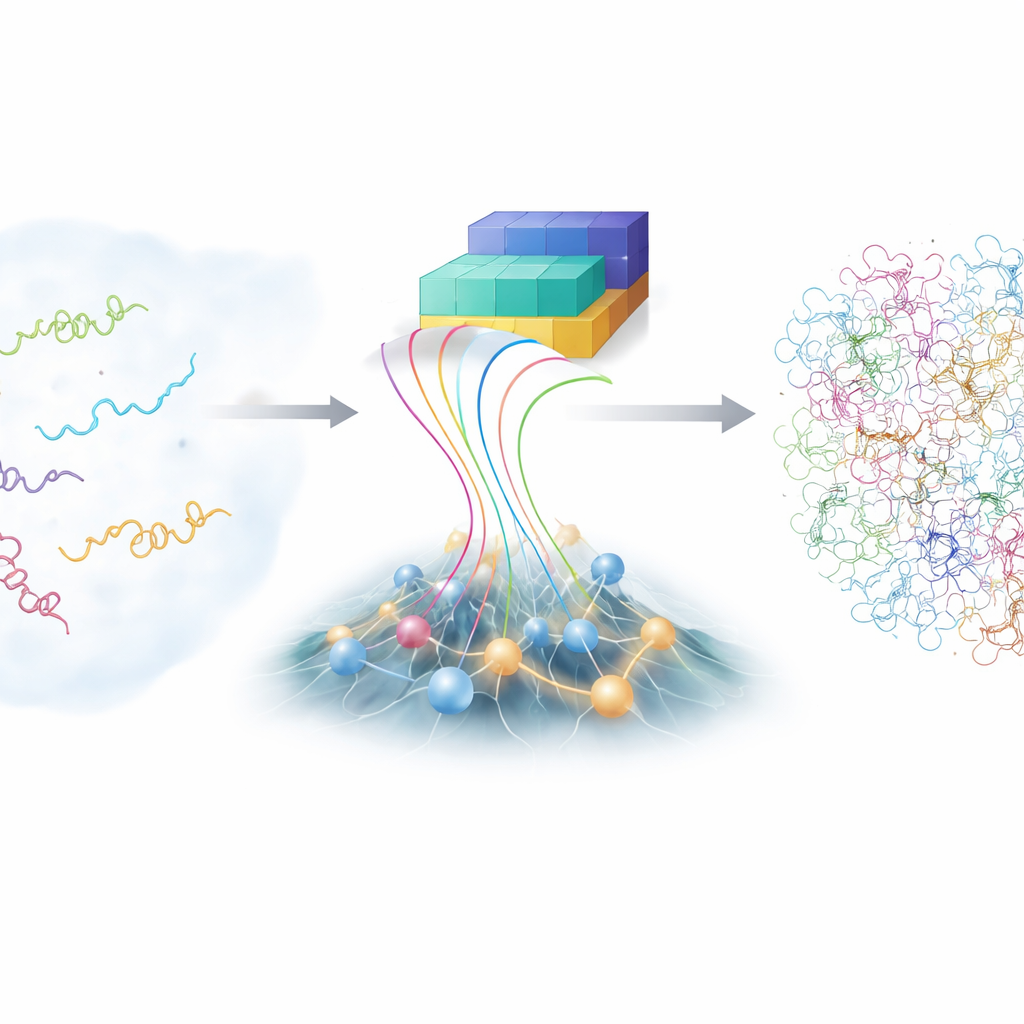
Wyzwanie niespokojnych cząsteczek
W przeciwieństwie do podręcznikowych modeli białek, które pokazują jedną uporządkowaną strukturę, białka wewnętrznie nieuporządkowane (IDP) przemierzają rozległy krajobraz możliwych kształtów. Ta elastyczność pomaga im rozpoznawać wielu różnych partnerów, ale jednocześnie utrudnia badania. Tradycyjne techniki laboratoryjne, takie jak zaawansowane spektroskopia rezonansu magnetycznego czy rozpraszanie rentgenowskie, dostarczają informacji uśrednionych po wielu konformacjach, lecz nie opisują każdej z osobna. Symulacje komputerowe w pełnych detalach atomowych mogą, przynajmniej w zasadzie, śledzić każdy atom w czasie ruchu IDP, jednak są bardzo kosztowne i zależą od precyzyjnie dopasowanych modeli fizycznych. W rezultacie społeczność naukowa dysponuje tylko ograniczonym zbiorem dokładnych, szczegółowych ensemble’i IDP do analizowania.
Łączenie inteligentnych przypuszczeń z zasadami fizyki
W ostatnich latach rodzina narzędzi AlphaFold z głębokim uczeniem zaskoczyła biologię przewidywaniem struktur białek na podstawie sekwencji aminokwasów. Dla białek nieuporządkowanych jednak zwykła siła AlphaFold — wskazywanie jednej najlepszej formy — jest mniej przydatna, ponieważ IDP nie mają jednej stałej struktury. AlphaFold dostarcza jednak bogatej informacji o tym, które fragmenty łańcucha mają tendencję być bliżej lub dalej od siebie. Autorzy opracowali nową ramę nazwaną bAIes, która traktuje te dane pochodzące z AI jako miękkie wskazówki i łączy je z szybkim, opartym na fizyce modelem, który celowo wychodzi od obrazu „losowej cewki”, gdzie łańcuch eksploruje wszystkie możliwe załamania i skręty bez preferowania konkretnej struktury.
Od losowych splotów do realistycznych ensemble’i
Pierwotnie badacze skonstruowali wydajny model fizyczny odwzorowujący zachowanie całkowicie nieustrukturyzowanego łańcucha białkowego, oparty na statystykach wyekstrahowanych z tysiąca znanych struktur białek. Model ten służy jako „priorytet” — punkt wyjścia zakładający, jak IDP porusza się, gdy nie wiemy nic więcej. Następnie bAIes odczytuje przewidywania AlphaFold dotyczące par reszt, które mają tendencję zbliżać się do siebie. Zamiast wymuszać jedną, sztywną strukturę, przekształca te wskazówki w łagodne ograniczenia odległości z wbudowaną niepewnością, pozwalając łańcuchowi uwzględniać sugestie AI tylko wtedy, gdy są zgodne z szerszym obrazem fizycznym.
Testowanie wobec rzeczywistych eksperymentów
Aby sprawdzić skuteczność podejścia, zespół zastosował bAIes do zestawu 21 białek, obejmujących warianty od niemal całkowicie losowych cewek po bardziej złożone systemy z przejściowymi helisami i wieloma domenami. Dla każdego z nich porównano wygenerowane komputerowo ensemble’e z szerokim zakresem pomiarów eksperymentalnych badających zarówno lokalne detale, jak i globalny rozmiar oraz kształt. Dla bardzo wiotkich białek, takich jak peptyd związany z chorobą Alzheimera Aβ40, prosty model losowej cewki był już zbliżony do rzeczywistości, a bAIes zachował tę dobrą zgodność. Dla częściowo ustrukturyzowanych białek bAIes poprawił dopasowanie do eksperymentów, prawidłowo odwzorowując miejsca, w których pojawiają się i znikają krótkie odcinki helikalne oraz zwartości. Kluczowe jest to, że metoda pozostała odporna nawet gdy AlphaFold był nadmiernie pewny siebie i błędnie przewidywał stabilne fałdowania tam, gdzie doświadczenia w roztworze wykazują bezład, ponieważ bAIes explicite dopuszcza błędy w danych wejściowych AI.
Pokonywanie lub dorównywanie istniejącym metodom
Autorzy porównali następnie bAIes z obciążającymi rozwiązaniami symulacjami wszystkich atomów uruchamianymi na wyspecjalizowanych superkomputerach, zaawansowanymi modelami grubopomiarowymi upraszczającymi białka do kulek oraz nowymi generatorami opartymi na głębokim uczeniu trenowanymi na danych z symulacji. W wielu testach bAIes konsekwentnie dorównywał lub przewyższał te podejścia w odtwarzaniu danych eksperymentalnych, przy jednoczesnym znacznie mniejszym zapotrzebowaniu obliczeniowym niż symulacje pełnoskalowe. Działał też poza prostymi IDP, obsługując białka z kilkoma sztywnymi domenami połączonymi elastycznymi łącznikami i odtwarzając ich ogólne kształty w roztworze. Gdy badacze dodatkowo dopracowali ensemble’e bAIes przy użyciu danych eksperymentalnych, zgodność poprawiła się jeszcze bardziej, pokazując, że metoda może służyć jako potężny punkt wyjścia do modelowania integracyjnego.
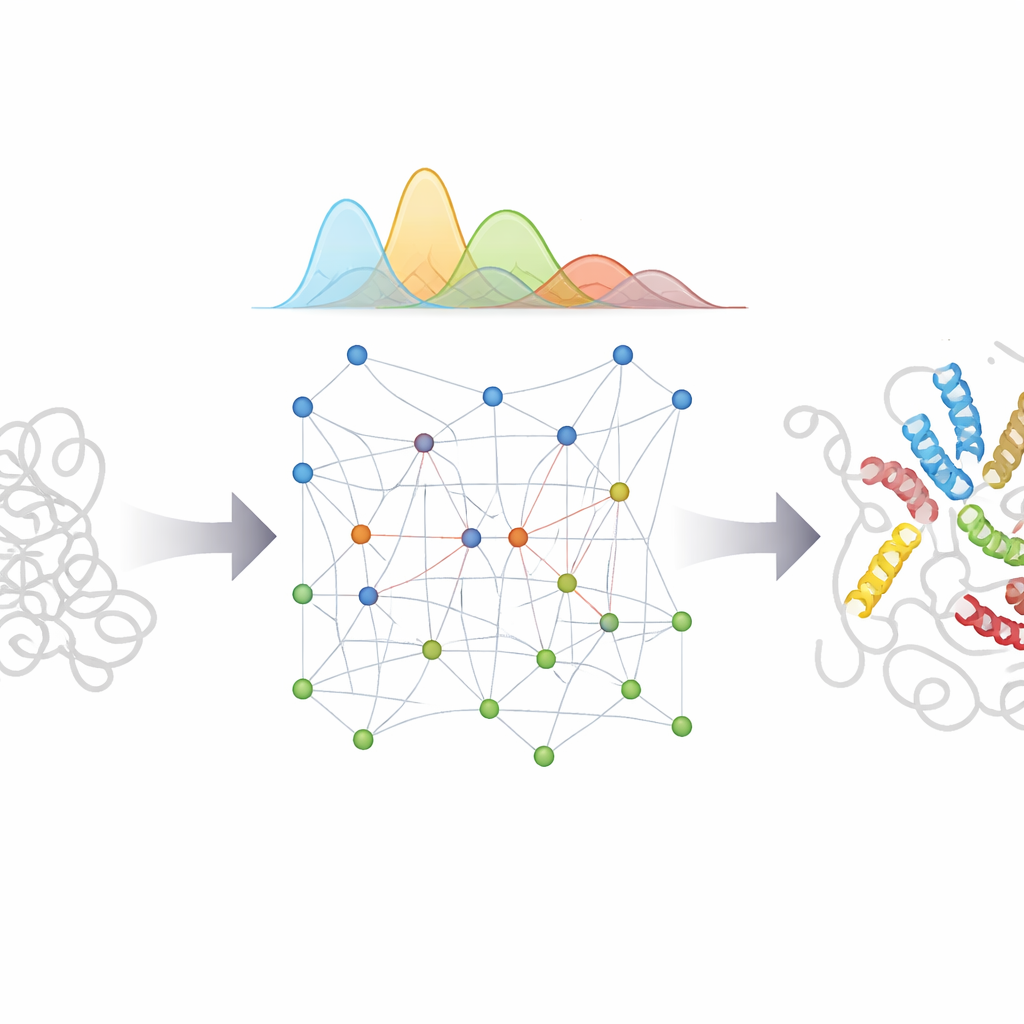
Co to oznacza dla biologii i medycyny
Łącząc zdolność AlphaFold do rozpoznawania wzorców z starannie zaprojektowanym modelem fizycznym i bayesowskim ujęciem niepewności, bAIes oferuje praktyczną drogę do szczegółowych „filmów” białek nieuporządkowanych zamiast pojedynczych migawkowych obrazów. Te zespoły o dokładności atomowej mogą pomóc naukowcom zrozumieć, jak elastyczne regiony rozpoznają partnerów, jak rozpoczyna się nieprawidłowe fałdowanie i agregacja w chorobach takich jak Parkinson i Alzheimer, oraz w jaki sposób małe cząsteczki mogą wiązać się z ulotnymi, zmiennymi celami. Ponieważ metoda jest wydajna i dostępna w otwartym oprogramowaniu, może być szeroko stosowana do generowania realistycznych ensemble’i dla wielu białek nieuporządkowanych, wspierając eksperymenty i przyszłe systemy AI, które będą dążyć do przewidywania nie jednej struktury, lecz pełnego spektrum kształtów, jakie mogą przyjmować najbardziej elastyczne cząsteczki życia.
Cytowanie: Schnapka, V., Morozova, T.I., Sen, S. et al. Atomic resolution ensembles of intrinsically disordered proteins with Alphafold. Nat Commun 17, 2399 (2026). https://doi.org/10.1038/s41467-026-69172-y
Słowa kluczowe: białka wewnętrznie nieuporządkowane, AlphaFold, modelowanie bayesowskie, zbiory konformacyjne białek, biologia strukturalna