Clear Sky Science · pl
Wpływ sił rozpuszczalnika i złamanej symetrii na samoorganizację zaprojektowanych białek na styku ciecz‑ciało stałe
Dlaczego ten mikroskopijny świat na powierzchni ma znaczenie
Od ogniw słonecznych po czujniki medyczne — wiele przyszłych technologii będzie polegać na tworzeniu precyzyjnych struktur tam, gdzie cząsteczki biologiczne stykają się z materiałami stałymi. W niniejszym badaniu analizowano, jak zaprojektowane „pręty” białkowe układają się na powierzchniach mineralnych w słonej wodzie. Zaskakujące wnioski pokazują, że woda bezpośrednio przy powierzchni oraz subtelne asymetrie kryształu leżącego pod nią mogą całkowicie zmieniać sposób, w jaki te białka się ustawiają — czasami generując wzory, które klasyczna teoria wskazywałaby jako niemożliwe.
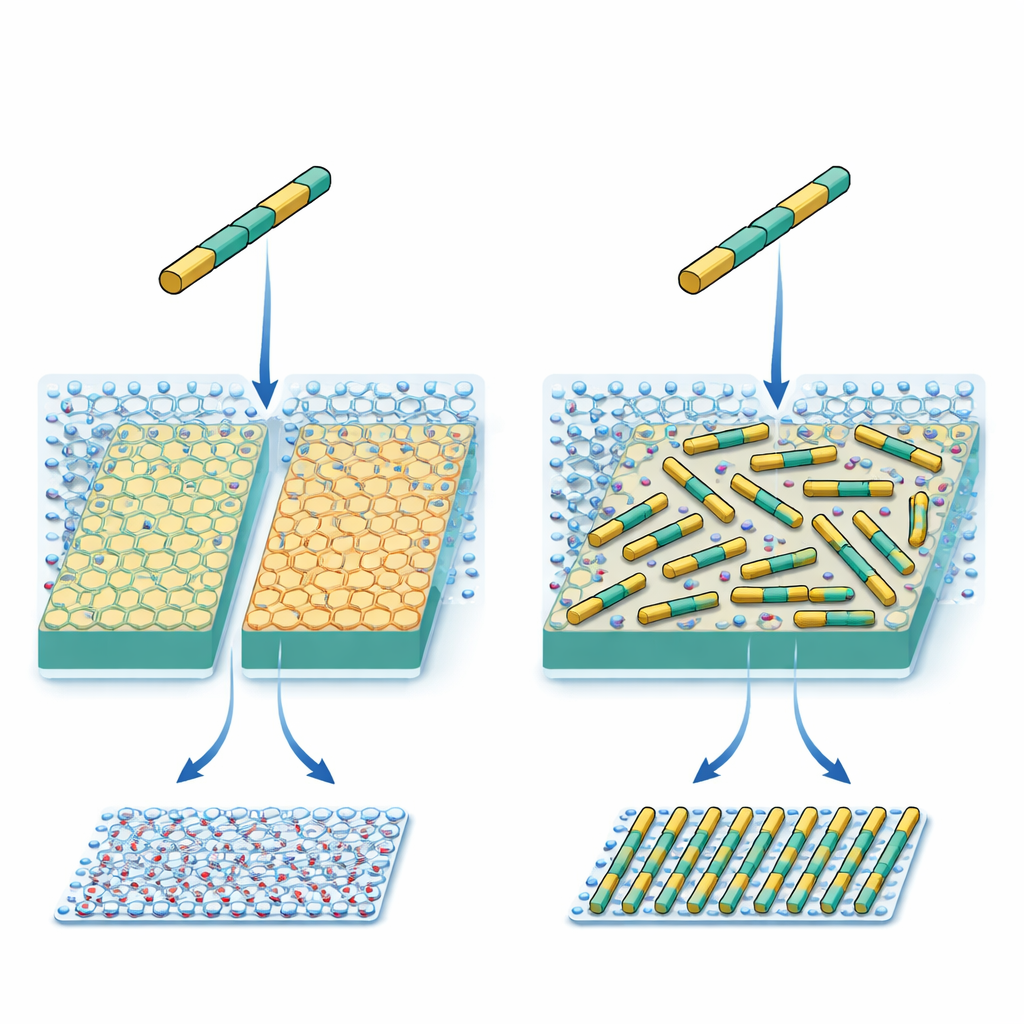
Projektowanie białek dopasowanych do kryształu
Naukowcy pracowali z syntetycznym białkiem o kształcie krótkiego, sztywnego pręta. Chemia powierzchni i rozmieszczenie grup naładowanych zostały starannie zaprojektowane tak, by pasować do wzoru jonów potasu na powszechnym minerale — mikach. W teorii każdy pręt białkowy powinien preferować trzy równoważne kierunki na powierzchni kryształu, jak ustawienie wzdłuż trzech szprych koła. Wcześniejsze badania wykazały jednak, że nawet przy takim precyzyjnym projekcie białka tworzyły kilka nieoczekiwanych układów zamiast jednego, przewidzianego przez inżynierów. Ta niezgodność sugerowała, że w obowiązujących zasadach projektowania brakuje istotnej siły.
Dwie niemal identyczne powierzchnie, dwa zupełnie różne wyniki
Aby ustalić, co się dzieje, zespół użył wysokorozdzielczej mikroskopii sił atomowych w czasie rzeczywistym, która pozwala obserwować pojedyncze pręty białkowe poruszające się i samoorganizujące na powierzchni. Porównano dwie bliskie formy mikrokrystalicznej miki. Obie mają tę samą odsłoniętą sieć jonów potasu, ale ich wewnętrzne struktury atomowe różnią się nieznacznie, co z kolei zmienia sposób, w jaki woda organizuje się w warstwach tuż nad powierzchnią. Przy umiarkowanym stężeniu soli pręty tworzyły gęsty, lecz lokalnie nieuporządkowany kobierzec na obu powierzchniach, z jedynie niewielkimi obszarami wyrównania. Gdy jednak stężenie soli bardzo wzrosło, zachowanie rozszczepiło się: na jednym typie miki pręty pozostały nieuporządkowane w trzech kierunkach, podczas gdy na drugim spontanicznie utworzyły długie, równoległe, równomiernie rozstawione rzędy na całej powierzchni.
Warstwy wody i złamana symetria
Modelowanie komputerowe minerałów i otaczającej je wody pomogło wyjaśnić tę dwoistość. Na bardziej symetrycznej formie miki pierwsza i druga warstwa cząsteczek wody zachowują regularny, sześciokątny wzór. Na mniej symetrycznej formie atomy wewnętrzne i ukryte grupy w kryształach łamią tę trójkową symetrię, a ten zaburzony wzór przenosi się do pobliskich warstw wody, które rozwijają pasmowe obszary. Białka nie stykają się wyłącznie z gołym kryształem; wchodzą też w interakcję z tą uporządkowaną wodą. W efekcie jedna orientacja prętów staje się nieznacznie bardziej korzystna niż pozostałe dwie, mimo że zaprojektowane dopasowanie białka do kryształu sugerowałoby równoważność wszystkich trzech.
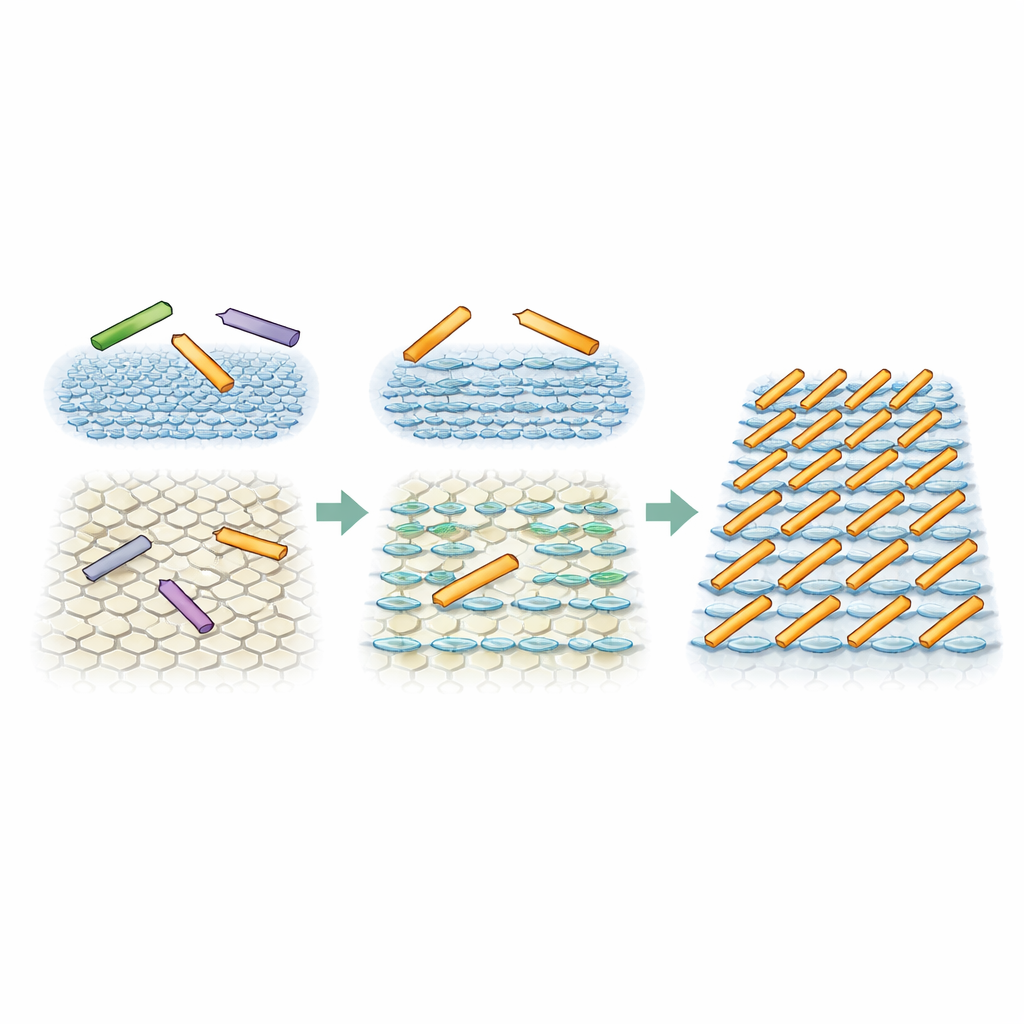
Symulacje ujawniają nieoczekiwaną fazę
Aby sprawdzić, czy subtelne ukierunkowanie ze strony środowiska powierzchniowego może rzeczywiście wyjaśnić obserwowane wzory, badacze przeprowadzili symulacje Monte Carlo z prostymi twardymi prostokątami reprezentującymi pręty białkowe. W jednym zestawie symulacji wszystkie trzy orientacje były równie prawdopodobne, naśladując w pełni symetryczną powierzchnię. W takim przypadku pręty pozostawały w stanie o dużej gęstości, lecz nieuporządkowanym, z jedynie tymczasowym lub ograniczonym wyrównaniem — dokładnie tak, jak zaobserwowano na jednym typie miki. W drugim zestawie jeden kierunek został uczyniony tylko nieznacznie bardziej korzystnym — około dwukrotnie bardziej prawdopodobnym niż pozostałe dwa — co miało obrazuje wpływ pasmowych warstw wody. W tych warunkach, i gdy pręty mogły się wystarczająco przemieszczać, układ naturalnie ewoluował w stan z równoległymi, równomiernie rozstawionymi rzędami. To tzw. faza smektyczna, której teoria długo utrzymywała, że nie powinna występować dla nieoddziałujących prętów w dwóch wymiarach, a mimo to niewielkie ukierunkowanie ze strony interfejsu uczyniło ją stabilną.
Ponowne przemyślenie projektowania materiałów bio‑inspirowanych
Krótko mówiąc, praca ta pokazuje, że precyzyjnie dobrana chemia białko–powierzchnia nie wystarcza, by przewidzieć, jak zaprojektowane białka ułożą się na prawdziwych materiałach. Woda znajdująca się między białkiem a ciałem stałym oraz sposób, w jaki kryształ subtelnie łamie symetrię, mogą kierować samoorganizacją w układy, których podręcznikowe modele by nie przewidziały. Łącząc mikroskopię w wysokiej szybkości, uczenie maszynowe do kwantyfikacji porządku oraz symulacje oparte na fizyce, badanie wytycza drogę, by uwzględnić te ukryte efekty rozpuszczalnika i symetrii w przyszłych narzędziach projektowania białek. Dla wszystkich, którzy chcą konstruować niezawodne, hybrydowe materiały bio‑anorgoniczne, przekaz jest jasny: trzeba projektować nie tylko dla białka i powierzchni, lecz także dla uporządkowanej warstwy wody, która je łączy.
Cytowanie: Yadav Schmid, S., Helfrecht, B., Stegmann, A. et al. Impact of solvent forces and broken symmetry on the assembly of designed proteins at a liquid-solid interface. Nat Commun 17, 2446 (2026). https://doi.org/10.1038/s41467-026-69170-0
Słowa kluczowe: samoorganizacja białek, styki ciecz‑ciało stałe, struktura wody przy powierzchni, uporządkowanie smektyczne, materiały inspirowane biologicznie