Clear Sky Science · pl
Mechanizm wielowartościowego adaptera napędza import proteasomów do jądra komórkowego
Jak komórki utrzymują swoje centrum dowodzenia w porządku
Wewnątrz każdej komórki jądro pełni rolę centrum dowodzenia, wypełnionego DNA i białkami kontrolującymi, które geny są włączane lub wyłączane. Aby to pomieszczenie kontrolne działało sprawnie, komórki polegają na potężnych molekularnych „niszczarkach” zwanych proteasomami, które rozkładają zużyte lub niewłaściwie funkcjonujące białka. Artykuł ten ujawnia, jak komórki radzą sobie z pozornie trudnym zadaniem transportu tych masywnych proteasomów przez wąskie bramki do jądra we właściwym momencie.
Wyzwanie przenoszenia dużych maszyn
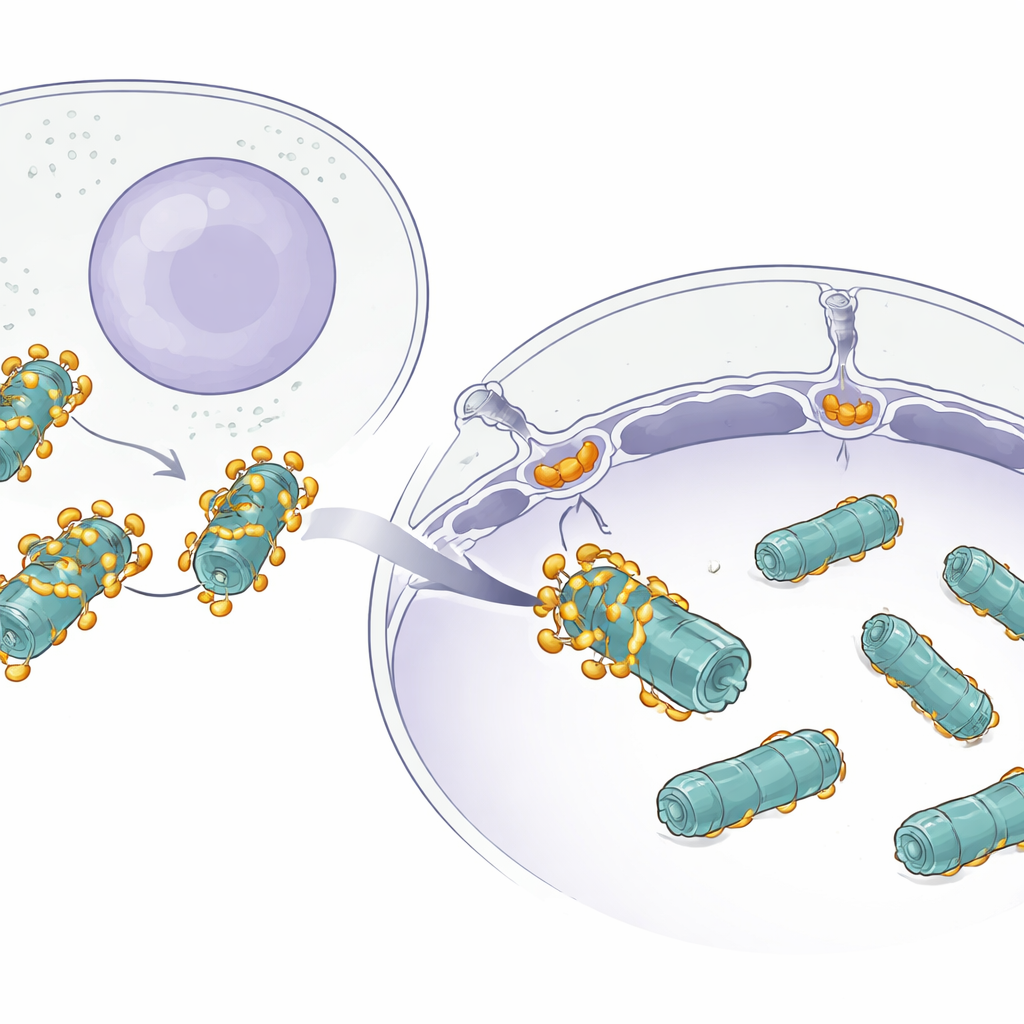
Wiele białek przemieszczanych jest między cytoplazmą a jądrem przez ogromne wejścia w otoczce jądrowej zwane porami jądrowymi. Małe białka przechodzą przez nie łatwo, ale duże maszyny, takie jak proteasomy, są inne: to masywne, baryłkowate kompleksy zbudowane z wielu części. Naukowcy wiedzieli już, że małe ładunki korzystają z białek pomocniczych zwanych importynami, by dostać się do jądra, ale nie było jasne, jak coś tak dużego jak proteasom przepycha się skutecznie bez zablokowania lub zagubienia.
Pomocnik zmieniający kształt wchodzi na scenę
Zespół skupił się na małym, elastycznym białku AKIRIN2, które wcześniejsze prace wskazywały jako absolutnie niezbędne do wejścia proteasomów do jądra. Komórki dzielące się bez AKIRIN2 nie potrafią wprowadzić proteasomów do jądra i szybko obumierają, ponieważ uszkodzone białka jądrowe się gromadzą. Stosując kombinację metod — w tym ogromne skanowanie mutacyjne obejmujące niemal każdy aminokwas AKIRIN2, wysokorozdzielczą kryo-elektronową mikroskopię do obserwacji kompleksu w 3D oraz staranne testy biochemiczne — badacze zmapowali, które części AKIRIN2 są istotne i jakie pełnią funkcje. Odkryli wcześniej niedoceniany segment przypominający „skrzydło” oraz skręcony region pozwalający AKIRIN2 tworzyć dimery (pary), z których oba odgrywają kluczowe role w chwytaniu proteasomów i innych partnerów.
Budowanie wieloręcznego uchwytu transportowego
Obrazy strukturalne ujawniły, że wiele kopii AKIRIN2 skupia się po jednej stronie proteasomu niczym liczne ręce chwytające ten sam obiekt. Każda para AKIRIN2 wiąże się z określonymi miejscami na zewnętrznej powierzchni proteasomu, jednocześnie angażując różne importyny. Jedna importyna, IPO9, trzyma AKIRIN2 w nietypowy sposób, obtaczając je i zmieniając swój kształt podczas składania kompleksu. Inne importyny, działające we własnych parach, rozpoznają krótkie sygnały wejścia do jądra przenoszone przez AKIRIN2. Ponieważ kilka cząsteczek AKIRIN2 osadza się na tym samym proteasomie, łącznie eksponują one wiele takich sygnałów jednocześnie. Ten wielowartościowy „uchwyt” pozwala tłumowi importyn przyczepić się równocześnie, dając ogromnemu proteasomowi wystarczającą siłę pociągnięcia, by przejść przez pora jądrową.
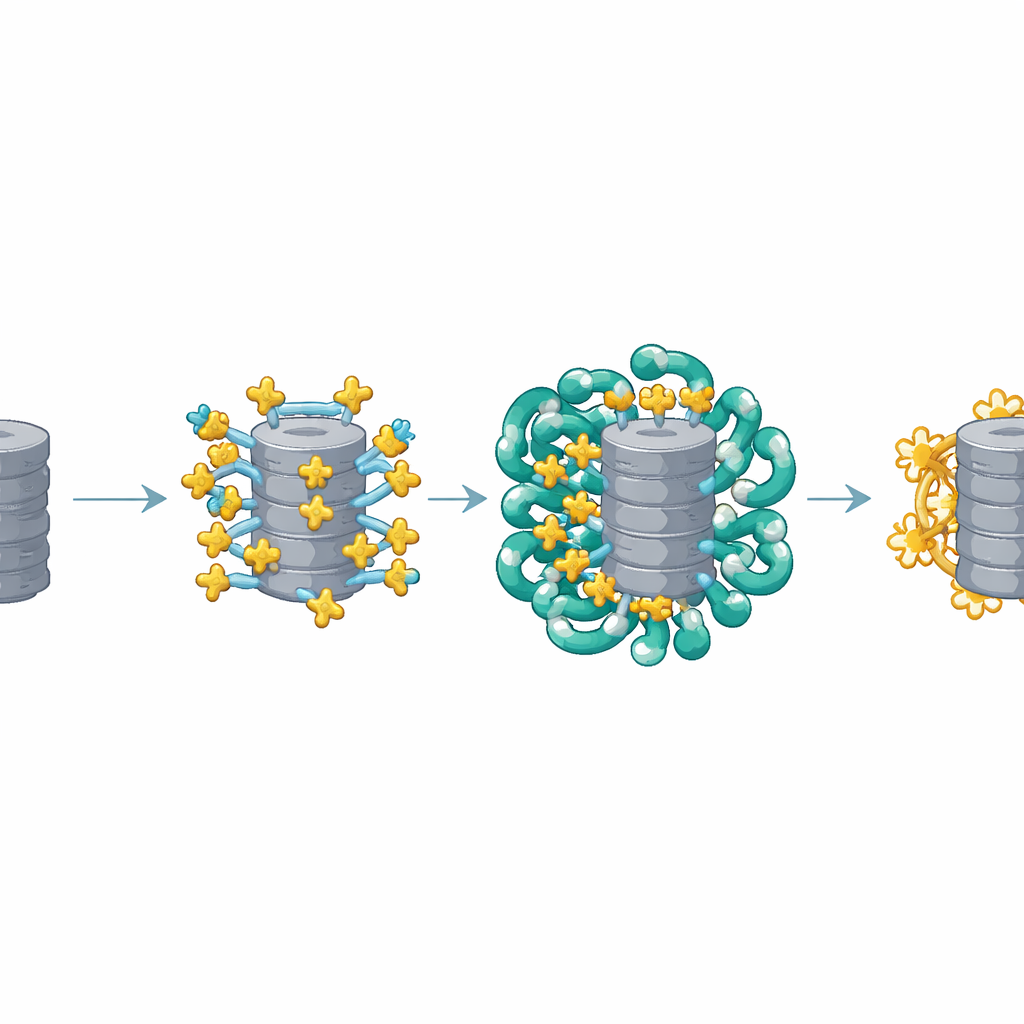
Sprytny cykl składania i uwalniania
Eksperymenty reconstitucyjne w uproszczonym układzie probówkowym wykazały, że proteasomy skutecznie wchodzą do jądra tylko wtedy, gdy obecne są jednocześnie AKIRIN2 i importyny. Im więcej AKIRIN2, tym silniejszy i szybszy import. Po dotarciu do jądra mechanizm transportowy musi zostać usunięty, aby proteasomy mogły działać. Komórka stosuje tu dwustopniowe uwalnianie. Małe białko przełącznikowe Ran, w formie związanej z GTP, zrzuca większość importyn z ich ładunku. AKIRIN2 i niektóre cząsteczki IPO9 trzymają się bardziej uporczywie, ale jądro ma plan awaryjny: proteasomy jądrowe bezpośrednio rozkładają same AKIRIN2, bez zwykłego znakowania ubikwityną. Pomiary w przebiegu cyklu komórkowego pokazują, że AKIRIN2 osiąga szczyt podczas podziału komórki, gdy formują się nowe jądra, a następnie spada we wczesnej fazie G1, co jest zgodne z tym ukierunkowanym porządkiem.
Znaczenie wykraczające poza jedno białko
Wszystko wskazuje, że AKIRIN2 działa jako elastyczny szkielet skupiający wiele importyn na jednym proteasomie, zamieniając trudny problem transportowy w skoordynowany wysiłek grupowy. Poprzez grupowanie sygnałów wejścia do jądra na adaptatorze zamiast na samym proteasomie, komórki mogą kontrolować, kiedy i z jaką siłą duże maszyny przemieszczają się do jądra, bez konieczności przeprojektowywania tych maszyn. Podobne strategie oparte na adapterach wydają się być wykorzystywane dla innych dużych zespołów białkowych, a nawet wirusy wykorzystują pokrewne triki, by wtargnąć do jądra. Zrozumienie tej ogólnej logiki transportu pogłębia nasze pojęcie o tym, jak komórki utrzymują równowagę białkową w swoim najbardziej wrażliwym przedziale, i może ostatecznie wskazać nowe sposoby interwencji, gdy degradacja białek lub funkcja jądra ulegają zaburzeniu.
Cytowanie: Brunner, H.L., Kalis, R.W., Grundmann, L. et al. A multivalent adaptor mechanism drives the nuclear import of proteasomes. Nat Commun 17, 2359 (2026). https://doi.org/10.1038/s41467-026-69162-0
Słowa kluczowe: transport jądrowy, proteasom, AKIRIN2, importyna, degradacja białek