Clear Sky Science · pl
Holistyczne podejście w biologii strukturalnej ujawnia dynamiczną organizację czwartorzędowego kompleksu chaperonowego R2SP
Jak komórki budują złożone maszyny molekularne
W każdej komórce wiele białek nie działa w pojedynkę — muszą połączyć się w rozbudowane maszyny, zanim będą mogły pełnić swoje funkcje. Poprawne przeprowadzenie tego etapu montażu jest kluczowe dla prawidłowego oddychania, ruchu, a nawet płodności. Artykuł bada jedno z takich wspomagających układów, molekularną „ekipę budowlaną” nazwaną kompleksem R2SP, i pokazuje, jak jest zorganizowana oraz jak działa. Zrozumienie R2SP ma znaczenie, ponieważ gdy jego składniki zawodzą, drobne, włoskowate wypustki na komórkach — rzęski — nie poruszają się prawidłowo, co prowadzi do przewlekłych problemów oddechowych i innych schorzeń.
Komórkowe ekipy budowlane R2TP i R2SP
Komórki polegają na zespołach pomocniczych białek, zwanych kompleksami chaperonowymi, które kierują inne białka ku prawidłowym, wieloczęściowym konformacjom. Jedna z długo badanych ekip, nazwana R2TP, występuje w wielu tkankach i pomaga składać duże maszyny, takie jak centra syntezy RNA czy czujniki uszkodzeń DNA. R2SP jest bliskim krewnym R2TP: oba oparte są na tym samym pierścieniowym silniku złożonym z dwóch białek partnerskich, RUVBL1 i RUVBL2, które zużywają energię w postaci ATP. Różnią się natomiast adapterami pomocniczymi, które wprowadzają klienty do tego silnika. R2TP używa adapterów o nazwach RPAP3 i PIH1D1, podczas gdy R2SP korzysta z SPAG1 i PIH1D2. Te drobne różnice w częściach determinują odmienne zestawy klientów i wiążą R2SP szczególnie z budową ruchomych rzęsek, które zamiatają śluz i płyny po powierzchniach tkanek.
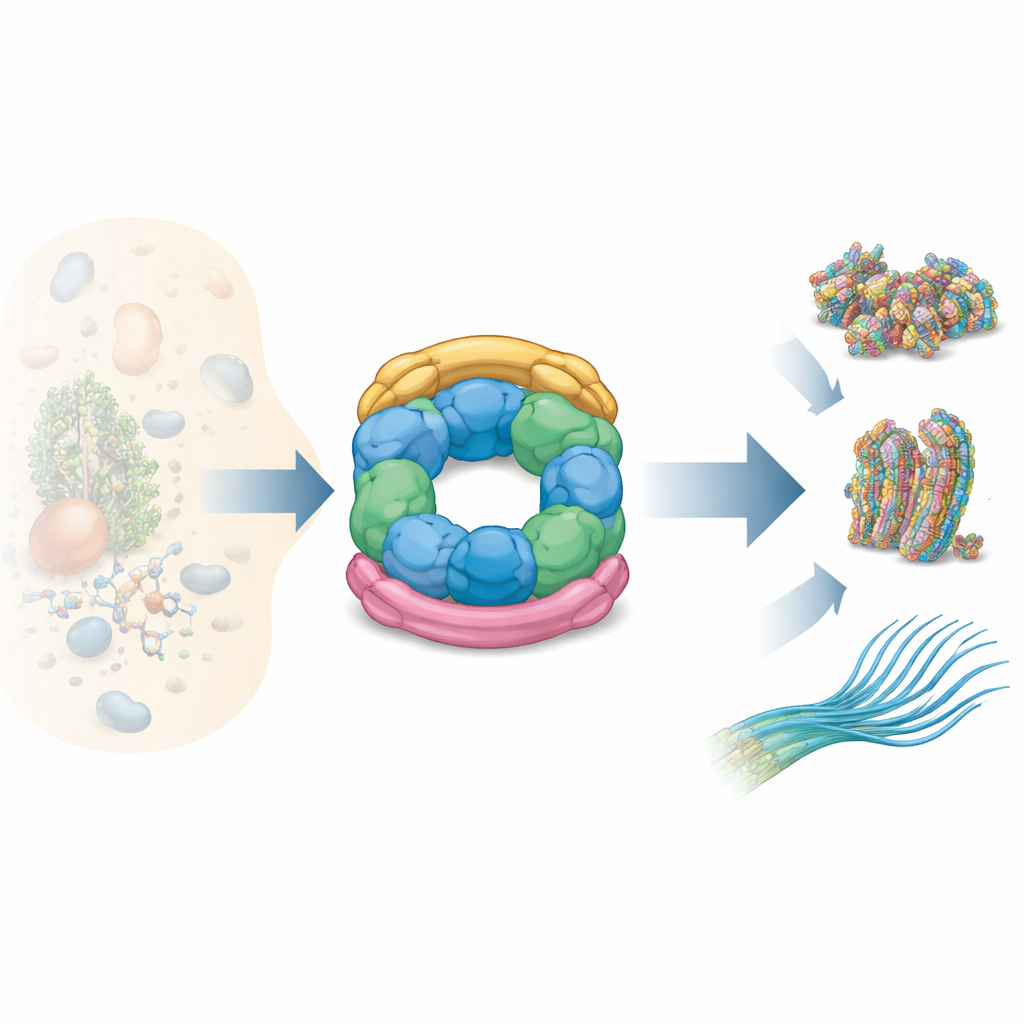
Jak elementy R2SP do siebie pasują
Autorzy połączyli kilka technik strukturalnych — spektroskopię magnetycznego rezonansu jądrowego, kriomikroskopię elektronową oraz spektrometrię mas połączoną z cross‑linkingiem — z testami biochemicznymi, aby odwzorować sposób budowy R2SP. Wykazali, że ogon SPAG1 chwyta pierścień RUVBL1/RUVBL2 w sposób przypominający wiązanie RPAP3 w R2TP, lecz z istotnymi zmianami w kształcie i punktach styku. Drugi adapter, PIH1D2, umiejscawia się pod pierścieniem i sięga również do elastycznych bocznych domen silnika. Te boczne domeny działają jak zawiasowe ramiona, które pomagają przekazywać ruchy z enzymatycznego rdzenia spalającego ATP do przyłączonych klientów. Dane pokazują, że SPAG1 i PIH1D2 nie przyłączają się niezależnie: współdziałają, tworząc sprzężoną jednostkę, która zaciska pierścień od góry i od dołu, stabilizując charakterystyczną trójwymiarową architekturę.
Dynamiczny pierścień, który zmienia biegi
Ponad statycznymi obrazami zespół zbadał, jak R2SP zachowuje się w ruchu. W pomiarach oddziaływań wykazano, że silnik RUVBL1/RUVBL2 może istnieć jako pojedynczy pierścień lub jako ułożone w stos podwójne pierścienie. Gdy wiążą się SPAG1 i PIH1D2, przesuwają one to równowagę zdecydowanie w stronę formy pojedynczego pierścienia i mogą go udekorować nawet trzema parami adapterów. Jednocześnie adaptery znacząco zwiększają aktywność hydrolityczną ATP silnika i zmieniają szybkość wiązania oraz odłączania cząsteczek podobnych do ATP z aktywnych miejsc. W porównaniu z systemem R2TP, SPAG1 i PIH1D2 faworyzują inne etapy uwalniania nukleotydu, co sugeruje, że R2SP dostraja cykl energetyczny rdzenia na swój sposób. Taka precyzyjnie kontrolowana gospodarka energetyczna prawdopodobnie napędza stopniowy montaż kompleksów‑klientów niezbędnych do budowy ruchomych rzęsek.
Elastyczna platforma do budowy składników rzęsek
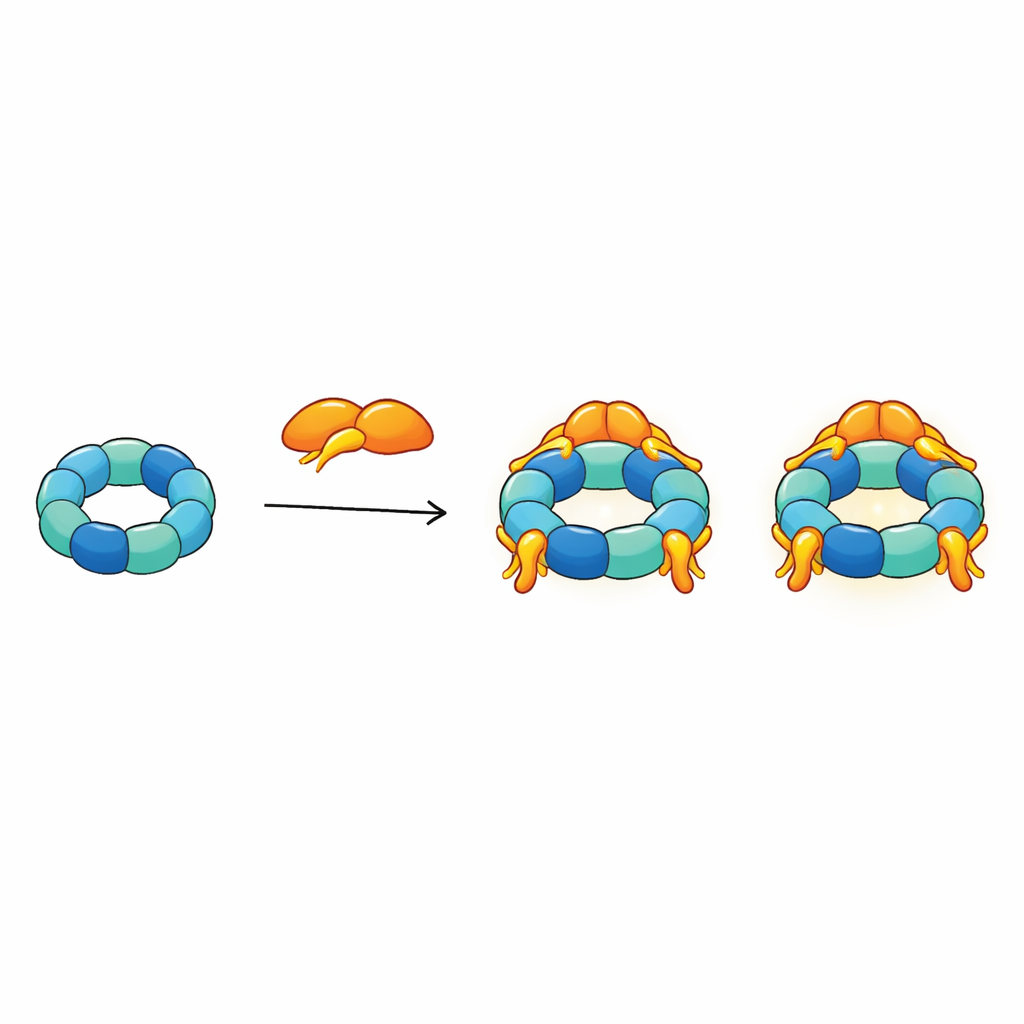
Integrując wszystkie ograniczenia strukturalne w jednym modelu, autorzy proponują, że R2SP działa jak elastyczna platforma o wielu ramionach. Ogon SPAG1 kotwiczy się mocno na szczycie pierścienia, podczas gdy inne jego regiony oraz dwie domeny PIH1D2 rozciągają się w kierunku bardziej otwartej, ramieniowej strony silnika. To właśnie po tej stronie najpewniej dokują białka‑klienci oraz pomocnicze chaperony, takie jak HSP70 i HSP90. Ponieważ do jednego pierścienia może przyłączyć się do trzech jednostek SPAG1–PIH1D2, a elastyczne ramiona nieustannie się poruszają, cały kompleks przypomina ośmiornicę, której macki mogą chwytać kilka elementów klienta jednocześnie, koordynować je i przekazywać do włączenia w większe struktury rzęskowe.
Co to oznacza dla zdrowia i chorób
Dla osób niebędących specjalistami główne przesłanie jest takie, że R2SP to wyspecjalizowana wersja ogólnej komórkowej maszyny budowlanej, przeprojektowana przez wymianę zaledwie dwóch adapterów. Ta wymiana zmienia zarówno kontrolę nad centralnym silnikiem, jak i pozycjonowanie klientów, wyjaśniając, dlaczego R2SP skupia się na budowie części dla ruchomych rzęsek, podczas gdy R2TP obsługuje inne komórkowe „fabryki”. Mutacje w SPAG1 są już znane jako przyczyna pierwotnej dyskinezy rzęsek, choroby objawiającej się przewlekłymi infekcjami i problemami z płodnością. Ujawniając szczegółowy układ i zasady działania R2SP, badanie to tworzy podstawy do zrozumienia, jak konkretne mutacje zakłócają montaż rzęsek i może w przyszłości wskazać ścieżki do ukierunkowanych terapii przywracających lub modulujących działanie tej kluczowej molekularnej ekipy budowlanej.
Cytowanie: Santo, P.E., Chagot, ME., Gizardin-Fredon, H. et al. An integrative structural biology approach reveals the dynamic organization of the R2SP quaternary chaperone complex. Nat Commun 17, 2605 (2026). https://doi.org/10.1038/s41467-026-69157-x
Słowa kluczowe: chaperony molekularne, montaż kompleksów białkowych, ruchome rzęski</keyword:r> <keyword>biologia strukturalna, RUVBL1 RUVBL2