Clear Sky Science · pl
Strukturalne podstawy wydajnej mitochondrialnej translacji zależnej od TACO1
Utrzymanie „elektrowni” komórki w sprawności
Mitrochondria nazywane są często elektrowniami komórek, ponieważ wytwarzają cząsteczkę energetyczną ATP. Aby to robić, muszą zbudować niewielki, lecz kluczowy zestaw białek przy użyciu własnych, wyspecjalizowanych fabryk białek — mitorybosomów. W tym badaniu odsłonięto, jak mało znane białko pomocnicze TACO1 dopracowuje te „fabryki”, by mogły działać płynnie, szczególnie gdy napotykają na „awkardowe” fragmenty łańcucha białkowego, które mają tendencję do powodowania zatorów maszynerii translacyjnej.
Fabryki energii z własnym sprzętem
W przeciwieństwie do większości produkcji białek, która zachodzi w wodnistym wnętrzu komórki, synteza białek w mitochondriach odbywa się na mitorybosomach zakotwiczonych w błonie wewnętrznej mitochondrium — tej samej, która gości liczne enzymy produkujące energię. Wykorzystując najnowocześniejszą krioelektronową mikroskopię elektronową na nienaruszonych ludzkich mitochondriach, autorzy uzyskali zdjęcia o niemal atomowej rozdzielczości tych mitorybosomów w ich naturalnym środowisku. Zaobserwowali, że wszystkie uchwycone mitorybosomy były przytwierdzone do błony wewnętrznej i ustawione tak, że nowo powstające łańcuchy białkowe mogą być bezpośrednio wprowadzane do inserazy błonowej — swoistego molekularnego gniazda, które przeciąga świeże białka do błony tam, gdzie są potrzebne do produkcji energii. 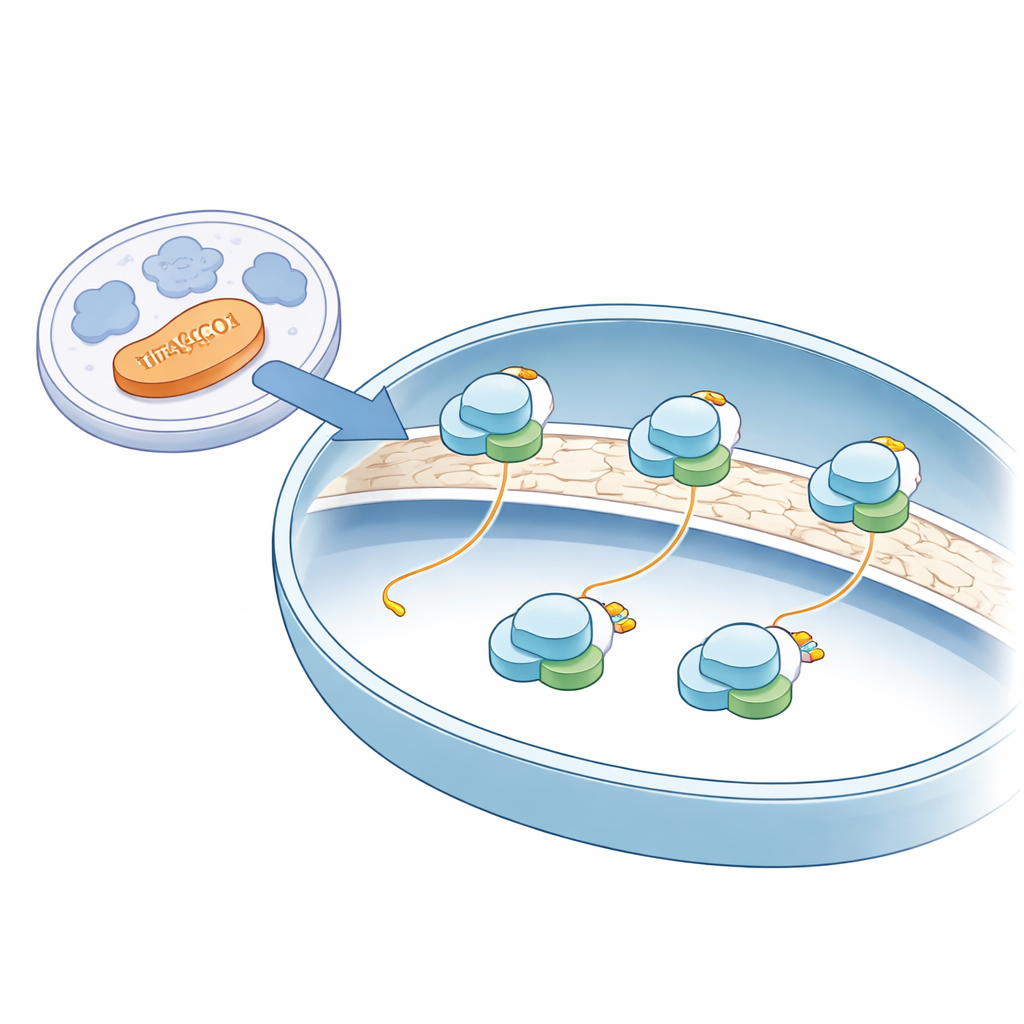
Ujawnienie ukrytego pomocnika
Wśród komponentów rybosomu, nici RNA i rosnących łańcuchów białkowych badacze zauważyli dodatkową plamę gęstości, która nigdy wcześniej nie była widoczna w wcześniejszych, bardziej sztucznych preparatach. Poprzez staranne udoskonalanie map i porównywanie kształtów z przewidywanymi strukturami białkowymi zidentyfikowali ten zagadkowy składnik jako TACO1 — białko wcześniej powiązane z ludzkimi chorobami mitochondrialnymi, którego fizyczna rola pozostawała niejasna. Obrazy wykazały, że TACO1 osadza się obok części rybosomu, gdzie przybywa następne tRNA niosące aminokwas (miejsce A), nawiązując kontakty zarówno z rRNA rybosomalnym, jak i z kilkoma białkami rybosomu. Takie umiejscowienie pozwala TACO1 działać niemal jak wspornik, podtrzymując nadchodzące tRNA, gdy rybosom tworzy nowe wiązanie wydłużające łańcuch białkowy.
Zapobieganie zatorom na linii montażowej białek
Synteza białka postępuje cyklicznie: czynnik elongacyjny (mtEF‑Tu) dostarcza załadowane tRNA, rybosom je sprawdza i wykorzystuje, a czynnik odchodzi, by mógł nastąpić kolejny krok. Autorzy odkryli, że TACO1 wiąże się mniej więcej w tym samym rejonie, którego używa mtEF‑Tu, i że oba czynniki nie mogą zajmować rybosomu jednocześnie. W normalnych komórkach wiele mitorybosomów występowało w stanie, w którym nowe tRNA jest w pełni na miejscu i elongacja postępuje. Gdy zespół zbadał mitochondria z komórek pozbawionych TACO1, zaobserwował nagromadzenie rybosomów utkniętych we wcześniejszym stanie, w którym mtEF‑Tu wciąż jest przyłączony, a nowe tRNA nie osiadło w pełni. Eksperymenty biochemiczne potwierdziły, że bez TACO1 mtEF‑Tu dłużej utrzymuje się na aktywnie tłumaczących rybosomach, a poddużyny duża i mała częściej się rozdzielają — co jest znamieniem zatrzymanej lub nieudanej translacji. 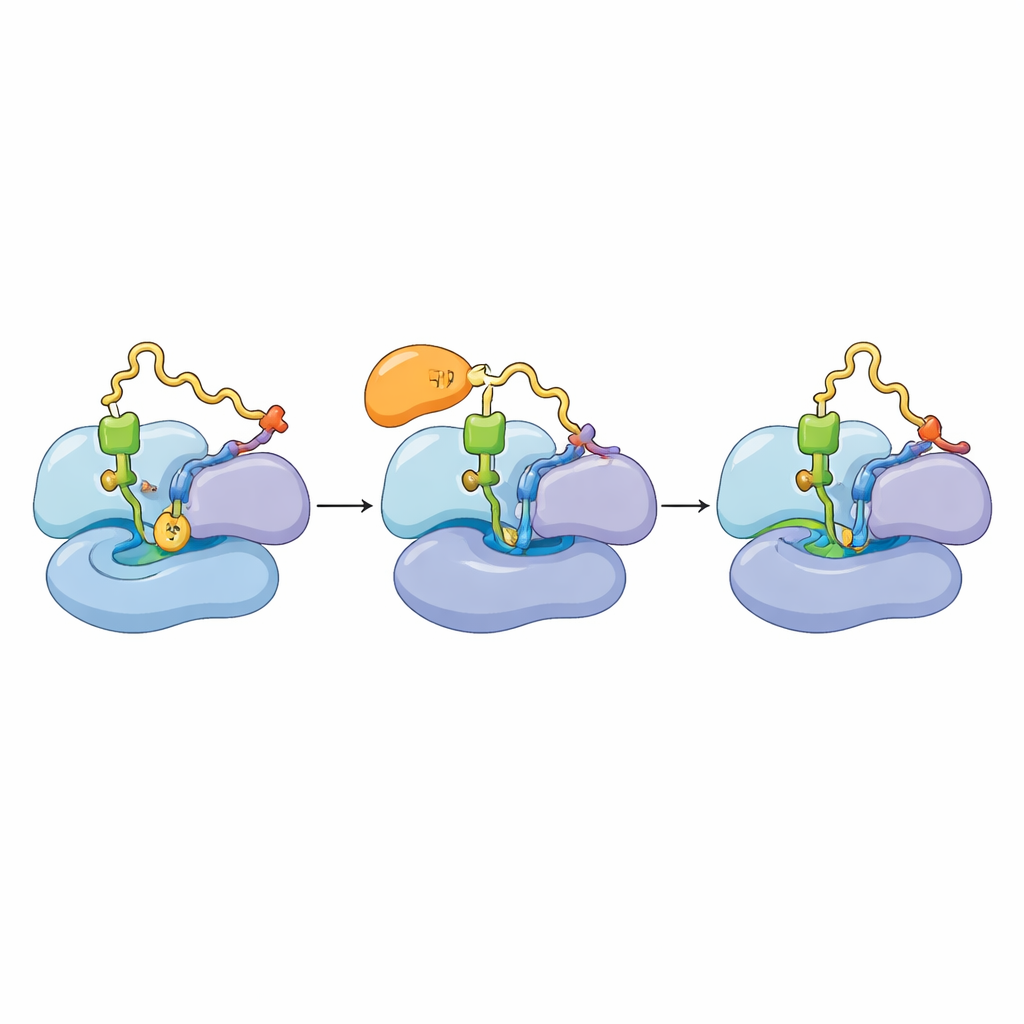
Dlaczego niektóre odcinki białka są tak kłopotliwe
Jednym z najważniejszych zadań TACO1 wydaje się być pomoc rybosomowi w przeprawie przez ciągi aminokwasu proliny, które naturalnie spowalniają tworzenie wiązań z powodu sztywnej struktury pierścienia proliny. Wcześniejsze prace wykazały, że TACO1 jest kluczowy dla produkcji podjednostki 1 oksydazy cytochromowej (cytochrom c oxidase subunit 1), rdzeniowego elementu łańcucha energetycznego zawierającego rzadki motyw z potrójną proliną, a jego utrata powoduje rozpad tego kompleksu energetycznego i chorobę mózgu u ludzi znaną jako zespół Leigha. W bakteriach i w głównym cytoplazmatycznym systemie komórkowym istnieją inne czynniki pełniące podobną funkcję przeciwdziałającą zatorom, ale mitochondria pozbawione są tych konwencjonalnych czynników. Nowe dane strukturalne pokazują, że TACO1 wyewoluował jako mitochondria‑specyficzne rozwiązanie: odsuwając mtEF‑Tu, stabilizując nadchodzące tRNA i wspierając tworzenie wiązania, pomaga mitorybosomowi przebić się przez te trudne sekwencje zamiast zatrzymywać się na amen.
Starożytna strategia o współczesnym znaczeniu dla zdrowia
Poza komórkami ludzkimi pokrewne białka do TACO1 występują w wielu bakteriach i innych organizmach, a niektóre z tych bakteryjnych wersji wykazano teraz, że także łagodzą zatrzymania rybosomów. To zachowanie wskazuje, że wykorzystanie czynnika podobnego do TACO1 do ratowania powolnych lub zatrzymanych rybosomów jest starożytną strategią utrzymania wydajnej syntezy białek. Dla ludzi praca ta daje konkretne, wizualne wyjaśnienie, dlaczego mutacje w TACO1 mogą tak poważnie upośledzać produkcję energii i układ nerwowy, oraz sugeruje, że manipulacja TACO1 lub jego krewniakami mogłaby pewnego dnia oferować sposoby regulacji mitochondrialnej translacji — albo w leczeniu chorób mitochondrialnych, albo w celowaniu w szkodliwe bakterie zależne od podobnych systemów łagodzących zatory.
Cytowanie: Wang, S., Brischigliaro, M., Zhang, Y. et al. Structural basis of TACO1-mediated efficient mitochondrial translation. Nat Commun 17, 2521 (2026). https://doi.org/10.1038/s41467-026-69156-y
Słowa kluczowe: translacja mitochondrialna, TACO1, mitorybosom, zatrzymanie rybosomu, zespół Leigha