Clear Sky Science · pl
Mechanizm molekularny importu fosforanu przez bakteryjny transporter PstSCAB
Dlaczego drobne składniki odżywcze mają dla nas znaczenie
Każda żywa komórka, od ludzkich neuronów po bakterie glebowe, funkcjonuje dzięki fosforowi. Ten pierwiastek pomaga magazynować energię, budować DNA i utrzymywać integralność błon komórkowych. Jednak w środowisku użyteczny fosforan — forma fosforu, którą komórki rzeczywiście mogą importować — jest często rzadki. Wiele chorobotwórczych bakterii polega na ultrawysoce wydajnej maszynie molekularnej, zwanej transporterem PstSCAB, która wyszukuje fosforan, gdy jest on w niedoborze. Zrozumienie dokładnego działania tej maszyny to nie tylko pytanie podstawowe; może też otworzyć drogę do nowych sposobów unieszkodliwiania infekcji przez pozbawienie bakterii tego niezbędnego składnika.
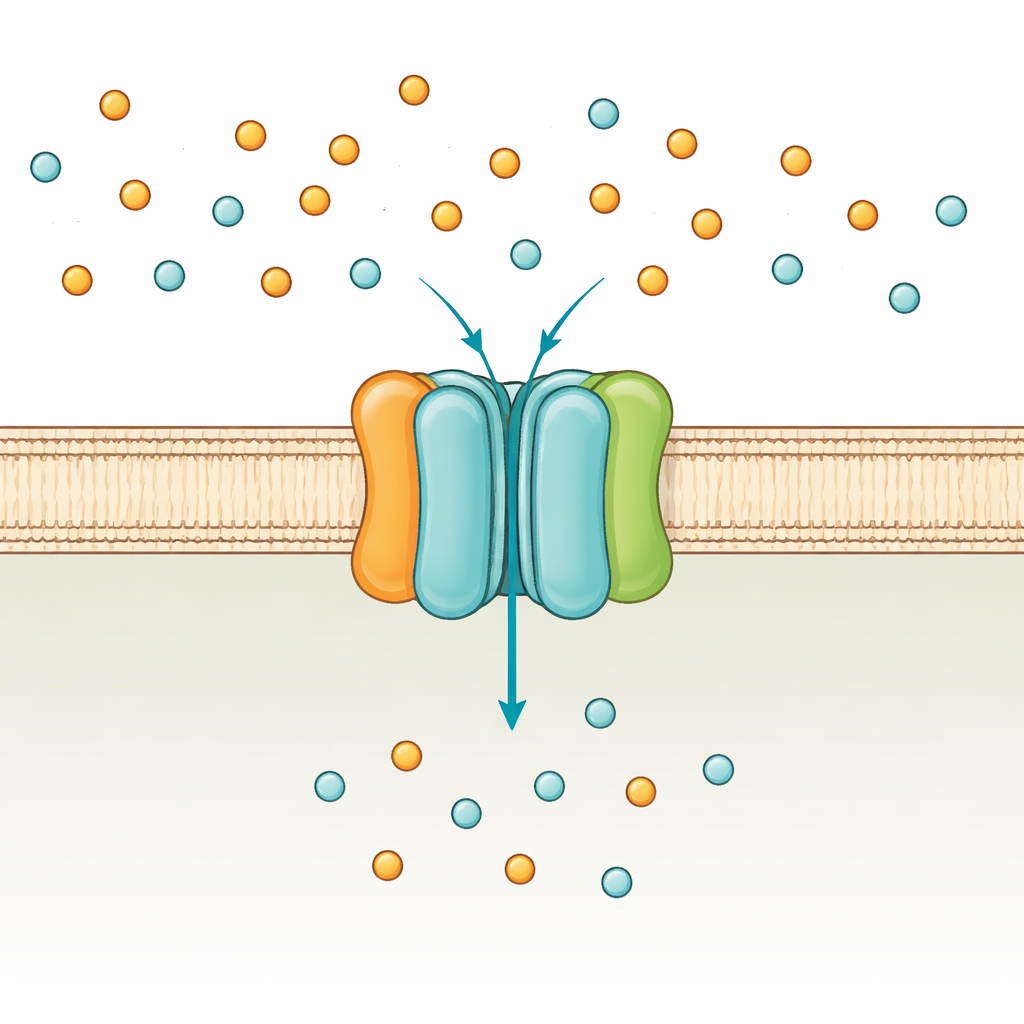
Bramkarz fosforanów komórki
Bakterie takie jak Escherichia coli wykorzystują dwie główne drogi pobierania fosforanu: system o niskim powinowactwie działający, gdy fosforan jest obfity, oraz system wysokiego powinowactwa PstSCAB, który uruchamia się przy niedoborach. PstSCAB osadzony jest w błonie komórkowej i napędzany przez ATP, uniwersalną walutę energetyczną komórki. Składa się z pięciu części: dwóch podjednostek osadzonych w błonie (PstA i PstC), które tworzą kanał, rozpuszczalnego „łapacza” zewnętrznego (PstS) chwytającego fosforan oraz pary wewnętrznych podjednostek (PstB), które rozkładają ATP, by napędzać transport. Ponieważ system ten pomaga także kontrolować wiele genów związanych z wirulencją bakterii, mutacje w PstSCAB mogą osłabić patogeny powodujące zakażenia układu moczowego, sepsę u zwierząt gospodarskich czy gruźlicę.
Uchwycenie maszyny w działaniu
Do tej pory naukowcy mieli tylko fragmentaryczne obrazy PstSCAB, głównie samego białka PstS. W tym badaniu badacze zastosowali krioelektronową mikroskopię o wysokiej rozdzielczości, aby zobrazować cały transporter w kilku kluczowych etapach cyklu pracy. Odtworzyli bakteryjne białka w sztucznych „nanodyskach” błonowych i zamrozili je tak szybko, że cząsteczki zostały uwiecznione w ruchu. Poprzez precyzyjne modyfikacje białek oraz dodawanie lub usuwanie ATP uzyskali struktury trzech głównych stanów: stanu spoczynkowego skierowanego do wnętrza komórki bez załączonego łapacza, stanu przedtranslokacyjnego, w którym PstS załadowany fosforanem dokuje do kompleksu błonowego, oraz pośredniego stanu katalitycznego związanym z ATP, w którym fosforan jest utrzymywany wewnątrz transportera.
Jak zmiany kształtu przesuwają fosforan
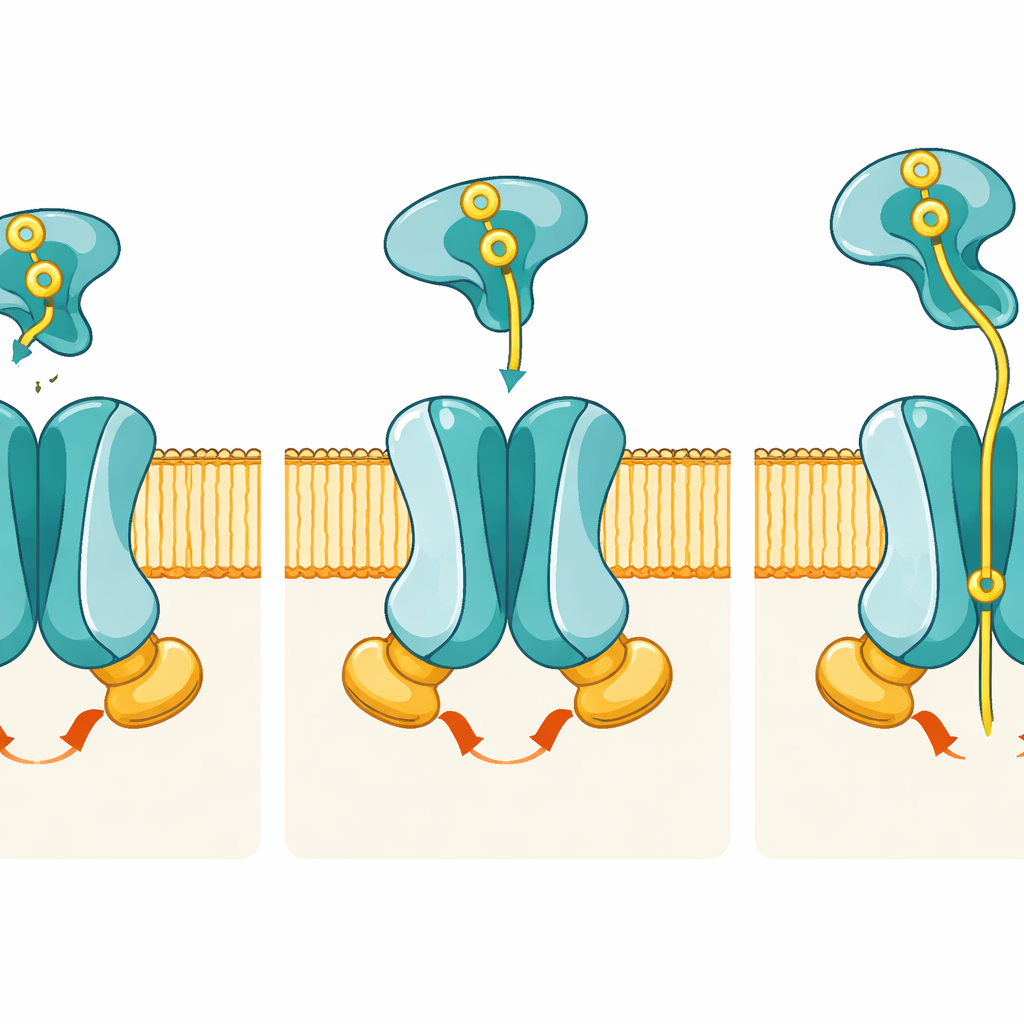
Obrazy ukazują, jak skoordynowane zmiany kształtu przesuwają fosforan z zewnątrz do wnętrza komórki. W stanie spoczynkowym kanał tworzony przez PstA i PstC jest otwarty tylko w kierunku wnętrza komórki; zewnętrzna strona jest zamknięta przez zestaw reszt „bramkowych”, co oznacza, że fosforan nie może jeszcze wejść z zewnątrz. Gdy PstS załadowany fosforanem dokuje w stanie przedtranslokacyjnym, osiada między elastycznymi pętlami PstA i PstC, ale co istotne, podjednostki błonowe ledwie zmieniają kształt. Prawdziwa zmiana następuje, gdy PstS zaczyna otwierać swoje dwie płaty, by uwolnić fosforan, a równocześnie dwie podjednostki PstB zbliżają się, aby związć ATP. To wiązanie ATP zaciska PstB w dimer i napina łączące helisy w PstA i PstC, odwracając cały kanał do konformacji skierowanej na zewnątrz i eksponując na zewnątrz specyficzną kieszeń wiążącą fosforan.
Specjalnie dopasowana kieszeń dla fosforanu
W strukturze skierowanej na zewnątrz, związanej z ATP, autorzy odnajdują gęstość w środku regionu membranowego odpowiadającą jonowi fosforanowemu. Jon ten jest podparty przez dodatnio naładowane aminokwasy — w szczególności przez dwie argininy, po jednej z PstA i PstC — które działają jak molekularne opuszki chwytające ujemnie naładowany fosforan. Symulacje komputerowe pokazują, że fosforan pozostaje stabilnie związany w tej kieszeni przez mikrosekundy, a eksperymenty genetyczne potwierdzają jego znaczenie: przy mutacjach tych kluczowych reszt transporter nadal zużywa ATP, lecz bardzo słabo importuje fosforan. To rozdzielenie „miejsca wydatkowania energii” od „miejsca rozpoznawania ładunku” podkreśla precyzyjne dostrojenie maszyny do fosforanu.
Od strukturalnych migawków do obietnicy medycznej
W sumie struktury i wspierające je testy biochemiczne opisują pełny cykl: PstS chwytają fosforan na zewnątrz, dokują do transportera skierowanego do wnętrza, następnie — sprzężone z wiązaniem i rozkładem ATP przez PstB — wywołują przewrócenie, które przekazuje fosforan do kieszeni w błonie, a ostatecznie do wnętrza komórki. Po hydrolizie ATP maszyna relaksuje się do stanu spoczynkowego, gotowa na kolejny cykl. Dla laików kluczowe przesłanie jest takie, że mamy teraz blueprint na poziomie atomowym pokazujący, jak wiele bakterii przetrwa w środowiskach ubogich w fosforan i jak regulują swoją wirulencję. Ten szczegółowy plan może poprowadzić projektowanie leków, przeciwciał lub peptydów, które zablokują transporter lub jego białko-łapacz, potencjalnie zamieniając bramę kluczową dla składnika odżywczego w wrażliwy cel terapeutyczny.
Cytowanie: Xiao, H., Li, S., Qi, R. et al. Molecular mechanism of phosphate import by the bacterial PstSCAB transporter. Nat Commun 17, 2294 (2026). https://doi.org/10.1038/s41467-026-69153-1
Słowa kluczowe: transport fosforanów, pobieranie składników odżywczych przez bakterie, transportery ABC, PstSCAB, cele antybakteryjne