Clear Sky Science · pl
Allergen oparty na mRNA wywołuje neutralizującą odpowiedź IgG przeciwko alergenom pokarmowym i pyłkowym
Dlaczego wiele alergii można leczyć jednocześnie
Dla osób reagujących nie na jedno, lecz na wiele powiązanych pokarmów lub pyłków codzienne życie może przypominać poruszanie się po polu minowym. Kęs brzoskwini, garść orzechów czy wiosenny podmuch powietrza pełen pyłków mogą wywołać ten sam niebezpieczny odczyn. W tym badaniu autorzy badają nowy sposób uspokojenia takich reaktywności krzyżowych przy użyciu pojedynczego, zaprojektowanego białka dostarczonego w postaci mRNA — tej samej podstawowej technologii, która była użyta w niektórych szczepionkach przeciw COVID-19 — aby wytrenować układ odpornościowy do blokowania całej rodziny powiązanych alergenów naraz.
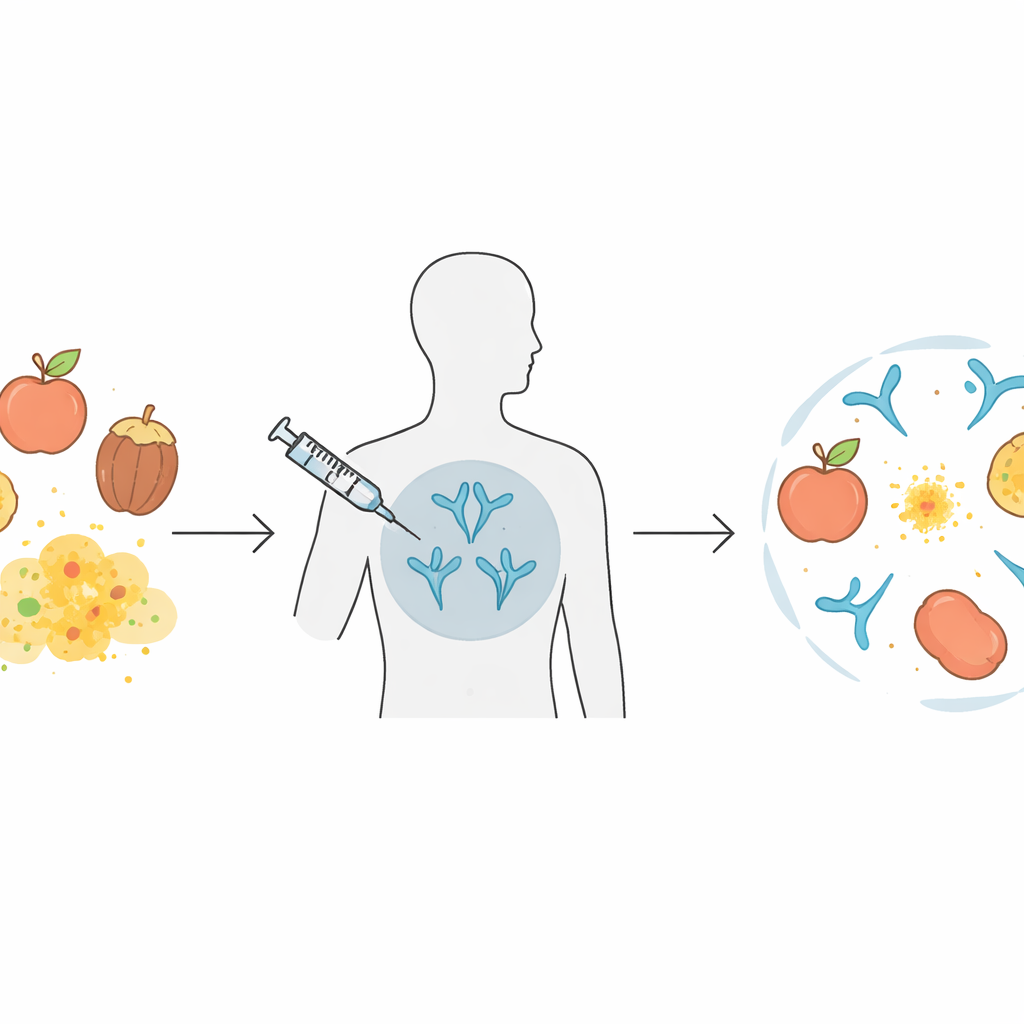
Jak jedna alergia może przekształcić się w wiele
Wiele osób z alergiami pokarmowymi nie jest uczulonych tylko na jeden składnik. Mogą reagować na kilka owoców, orzechów, warzyw, a nawet pyłków, ponieważ te źródła mają podobne białka. W tej pracy skupiono się na rodzinie białek roślinnych zwanych nieswoistymi białkami przenoszącymi lipidy (nsLTP), które występują w takich produktach jak brzoskwinie, jabłka, orzechy oraz w pyłkach niektórych drzew i chwastów. W krajach basenu Morza Śródziemnego tzw. „zespół LTP” może powodować u pacjentów reakcje na szeroką listę pokarmów, czasem prowadzące do zagrażającej życiu anafilaksji. Obecne immunoterapie alergenowe zazwyczaj celują w ekstrakty z jednego źródła i mogą nie obejmować wszystkich krzyżowo reagujących krewniaków, co oznacza długotrwałe leczenie i niepełną ochronę.
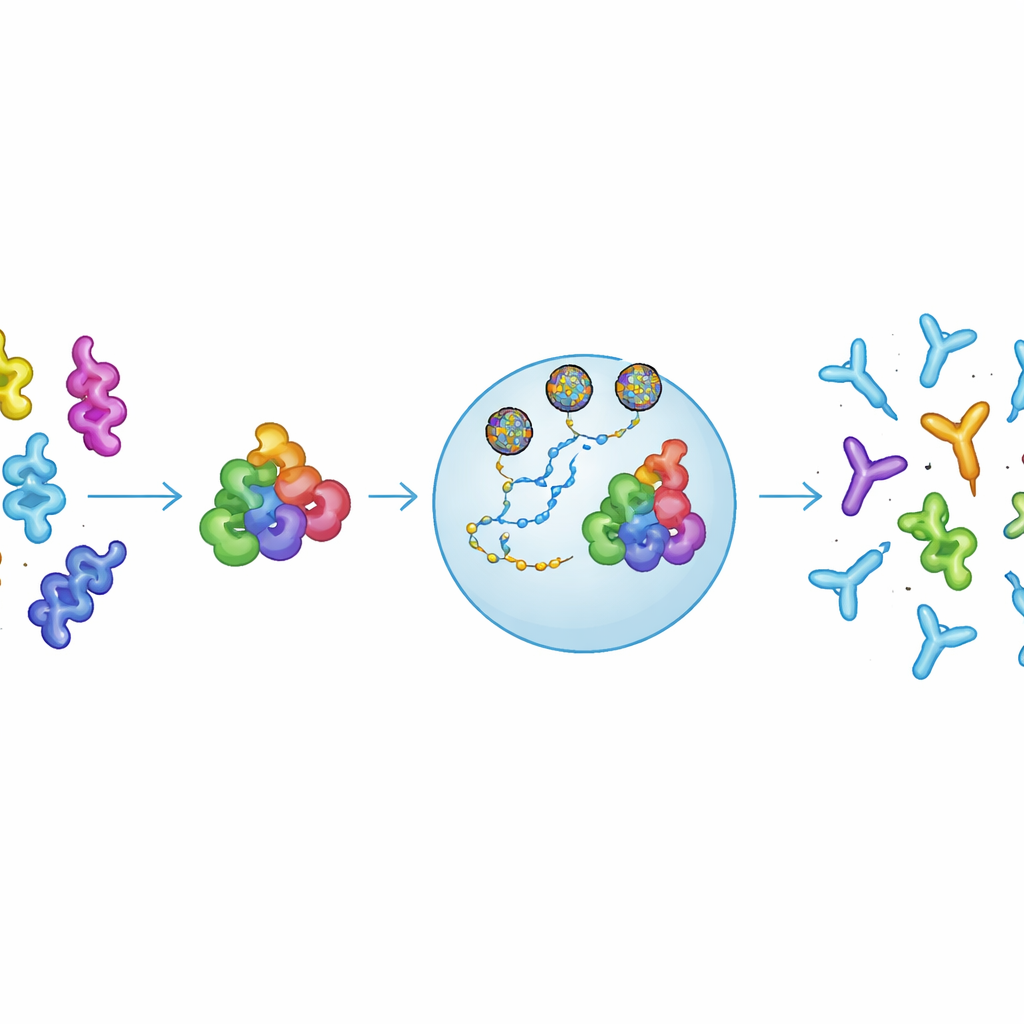
Projektowanie „konsensusowego” alergenu
Naukowcy postanowili zaprojektować pojedyncze białko, które naśladowałoby wiele różnych alergenów nsLTP jednocześnie. Porównali sekwencje aminokwasowe nsLTP występujących w pokarmach i pyłkach i skonstruowali wersję konsensusową, nazwaną cnsLTP1, która nie kopiuje żadnego naturalnego białka, lecz oddaje wspólne cechy strukturalne całej rodziny. Testy laboratoryjne wykazały, że to zaprojektowane białko fałduje się jak naturalne nsLTP, zachowuje stabilność po podgrzaniu i schłodzeniu oraz, co kluczowe, jest rozpoznawane przez przeciwciała IgE pobrane od pacjentów już uczulonych na nsLTP. To rozpoznanie wskazuje, że cnsLTP1 prezentuje te same kluczowe „miejsca wywołujące alergię” co alergeny występujące w rzeczywistości — co jest niezbędne, jeśli ma przeuczyć układ odpornościowy do innej reakcji.
Trening układu odpornościowego za pomocą mRNA i szczepionek białkowych
Zespół następnie przetestował cnsLTP1 u myszy, stosując dwie różne metody dostarczania: tradycyjną szczepionkę białkową zmieszaną z adiuwantami oraz szczepionkę mRNA zapakowaną w nanocząstki lipidowe, podobne pod względem składu do zatwierdzonych szczepionek mRNA. U myszy naiwnych obie metody wywołały silne odpowiedzi przeciwciał przeciw cnsLTP1, w szczególności podklasy IgG, które u myszy pełnią ochronną, blokującą alergię rolę. Szczepionka oparta na mRNA miała tendencję do wywoływania większej ilości pewnego typu IgG i robiła to po mniejszej liczbie dawek. Przeciwciała podniesione przeciw cnsLTP1 wiązały się nie tylko z zaprojektowanym białkiem, lecz także z szerokim panelem różnych nsLTP z pokarmów i pyłków, często szerzej niż przeciwciała podniesione przeciw pojedynczym naturalnym alergenom, takim jak nsLTP z brzoskwini czy parietaria. Oznacza to, że projekt konsensusowy skutecznie nauczył układ odpornościowy rozpoznawania wielu powiązanych alergenów.
Hamowanie reakcji alergicznych w laboratorium i testy na uczulonych myszach
Aby sprawdzić, czy te przeciwciała rzeczywiście mogą zakłócać reakcje alergiczne, badacze zmieszali surowicę myszy z alergenami, a następnie dodali surowicę ludzką od pacjentów z ciężkimi alergiami na nsLTP. Stwierdzili, że przeciwciała indukowane przez cnsLTP1 potrafiły blokować wiązanie IgE do wielu nsLTP oraz zmniejszały degranulację humanizowanych komórek bazofilopodobnych — komórkowy model aktywacji alergicznej. W trudniejszym teście zespół użył modelu myszy już uczulonej na nsLTP z brzoskwini i podatnej na anafilaksję. Szczepionka mRNA była dobrze tolerowana i zwiększała poziomy IgG przeciw kilku nsLTP, ale w warunkach zastosowanych w tym badaniu nie zmniejszyła wyraźnie objawów anafilaksji, takich jak spadek temperatury ciała czy markery aktywacji komórek tucznych. To sugeruje, że choć układ odpornościowy został przekształcony, stosowany schemat nie był jeszcze wystarczająco silny ani precyzyjnie dostrojony, by w pełni zapobiec ciężkim reakcjom.
Co to może oznaczać dla przyszłej opieki nad alergiami
Badanie dostarcza dowodu koncepcji, że pojedynczy, zaprojektowany „konsensusowy” alergen dostarczony w postaci mRNA może wywołać szerokie, krzyżowo reagujące i funkcjonalnie blokujące przeciwciała IgG przeciw całej rodzinie powiązanych białek pokarmowych i pyłkowych. Chociaż obecny protokół nie zabezpieczył jeszcze uczulonych myszy przed anafilaksją, wyniki wskazują na elastyczną platformę, którą można poprawić przez dostosowanie dawki, adiuwantów lub drogi podania. W dłuższej perspektywie terapie oparte na konsensusie i mRNA mogłyby umożliwić leczenie grup powiązanych alergii — takich jak te wywoływane przez nsLTP, inne rodziny białek roślinnych, a nawet szybko mutujące patogeny — krótszymi, bardziej precyzyjnymi i szerzej chroniącymi schematami terapeutycznymi.
Cytowanie: Møiniche, M., Johansen, K.H., Parrón-Ballesteros, J. et al. An mRNA-delivered consensus allergen induces a neutralizing IgG response against food and pollen allergens. Nat Commun 17, 2402 (2026). https://doi.org/10.1038/s41467-026-69134-4
Słowa kluczowe: alergia pokarmowa, alergia na pyłki, immunoterapia mRNA, reaktywność krzyżowa, białka przenoszące lipidy