Clear Sky Science · pl
Późnostopniowa, selektywna alkenylacja i alkynylacja N‑Me leków i nieaktywowanych trzeciorzędowych aminów z użyciem katalizy fotoredoks
Dlaczego modernizowanie starych leków wciąż ma znaczenie
Wiele współczesnych leków działa skutecznie, ale wciąż pozostawia pole do poprawy pod względem bezpieczeństwa, działań niepożądanych lub precyzji oddziaływania na cele biologiczne. Chemicy coraz częściej wolą delikatnie „dostroić” istniejące cząsteczki na późnym etapie rozwoju, zamiast tworzyć całkowicie nowe struktury od podstaw. W tej pracy pokazano, jak wiązki światła widzialnego można wykorzystać do przyłączenia nowych fragmentów do powszechnego typu elementu budulcowego leków, tworząc ulepszone kandydaty na leki przeciwdepresyjne i otwierając szybszą ścieżkę do udoskonalonych terapii.
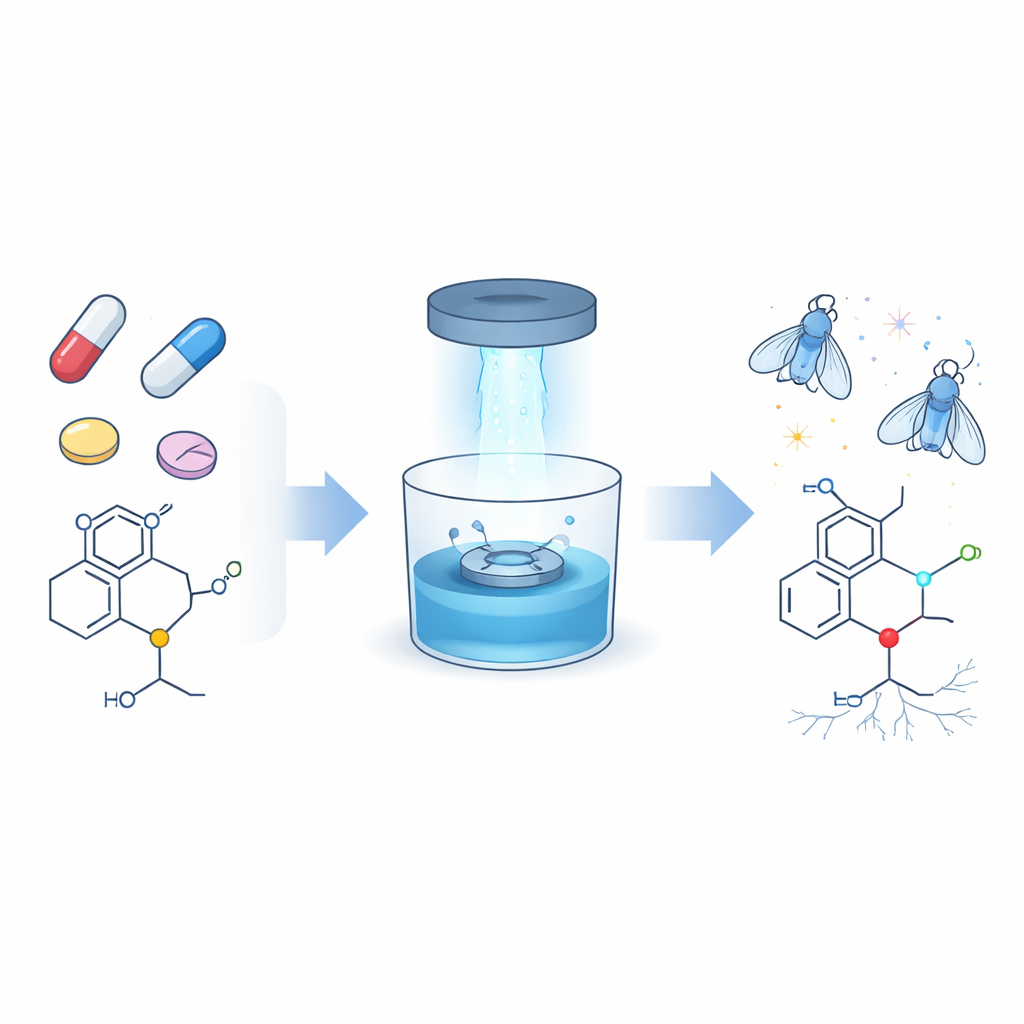
Ulepszanie powszechnego elementu w wielu lekach
Zaskakująco duża część współczesnych leków — ponad dwie na pięć — zawiera fragmenty bogate w azot, zwane aminami, z których większość to podtyp trzeciorzędowych amin. Występują w antybiotykach, lekach przeciwnowotworowych, preparatach przeciwalergicznych, środkach przeciwbólowych i lekach przeciwdepresyjnych. Dotąd chemicy mieli trudności z selektywną modyfikacją jednego, bardzo niewielkiego elementu tych grup — jednostki N‑metylowej — gdy znajduje się ona w otoczeniu kilku niemal identycznych wiązań węgiel–wodór. Autorzy postawili sobie za cel opracowanie łagodnej, niezawodnej metody przyłączania nowych „uchwytów”, konkretnie wiązań podwójnych węgiel–węgiel (alkenów) i potrójnych (alkinów), do pozycji N‑metylowej bez naruszania reszty cząsteczki leku.
Wykorzystanie światła do przekształcania jednego wiązania na raz
Zespół sięgnął po katalizę fotoredoks — technologię używającą światła widzialnego i fotoczułego katalizatora do przemieszczania pojedynczych elektronów i inicjowania reakcji w łagodnych warunkach. W ich systemie niebieskie światło wzbudza organiczny katalizator, który tymczasowo usuwa elektron z trzeciorzędowej aminy. Ten etap tworzy krótkotrwały rodnik w pozycji N‑metylowej, który może połączyć się z dobranymi partnerami zawierającymi grupy winylowe lub alkynylowe. Poprzez dostrojenie warunków reakcji — wyboru rozpuszczalnika, zasady i dodatków — badacze osiągnęli wysokie wydajności i doskonałą kontrolę, tak że nowa grupa przyłącza się niemal wyłącznie do pozycji N‑metylowej, nawet gdy obecnych jest kilka podobnych miejsc. Zademonstrowali to na szerokim panelu prostych amin, a następnie na rzeczywistych lekach, w tym przeciwhistaminowych, kardiologicznych, przeciwinfekcyjnych i kilku przeciwdepresyjnych.
Od chemicznej poprawki do lepszego działania przeciwdepresyjnego
Aby sprawdzić, czy te strukturalne modyfikacje mają znaczenie medyczne, autorzy skoncentrowali się na imipraminie, długo stosowanym trójpierścieniowym leku przeciwdepresyjnym. Zaprojektowali i przeanalizowali komputerowo ponad dwadzieścia wariantów imipraminy, w których nowe przedłużenie winylowe lub alkynylowe niosło pierścienie aromatyczne mogące dobrze wejść w hydrofobowe kieszenie ludzkiego transportera serotoniny — białka kontrolującego poziomy tego neuroprzekaźnika. Dokowanie komputerowe sugerowało, że wiele z tych zmodyfikowanych cząsteczek powinno wiązać się równie dobrze lub lepiej niż lek macierzysty. Najbardziej obiecujące kandydaty zostały następnie zsyntezowane nową metodą napędzaną światłem i przetestowane w układach biologicznych: w modelu depresji u muszki owocowej opartej na izolacji społecznej oraz, dla dwóch najlepszych związków, w komórkach nerwowych myszy aktywnie transportujących serotoninę.
Jak muszki i komórki ujawniły silniejsze leki
U izolowanych samców muszek owocowych zachowania przypominające depresję objawiają się zwiększoną agresją. Podawanie imipraminy zmniejsza tę agresję, odzwierciedlając jej działanie przeciwdepresyjne u ludzi. Co ważne, kilka pochodnych imipraminy otrzymanych nową metodą zmniejszało agresję równie skutecznie, a cztery kandydaty działały nawet lepiej niż sama imipramina. W hodowanych komórkach hipokampa myszy dwa wiodące związki silniej blokowały wychwyt zwrotny serotoniny niż imipramina, co potwierdzono zarówno bezpośrednim pomiarem chemicznym serotoniny, jak i barwnikiem fluorescencyjnym, który świeci po wniknięciu do komórek. Te testy wskazują, że subtelne późnostopniowe zmiany przy pozycji N‑metylowej mogą rzeczywiście zwiększyć potencję przeciwdepresyjną, a nie tylko zmienić strukturę cząsteczki na papierze.
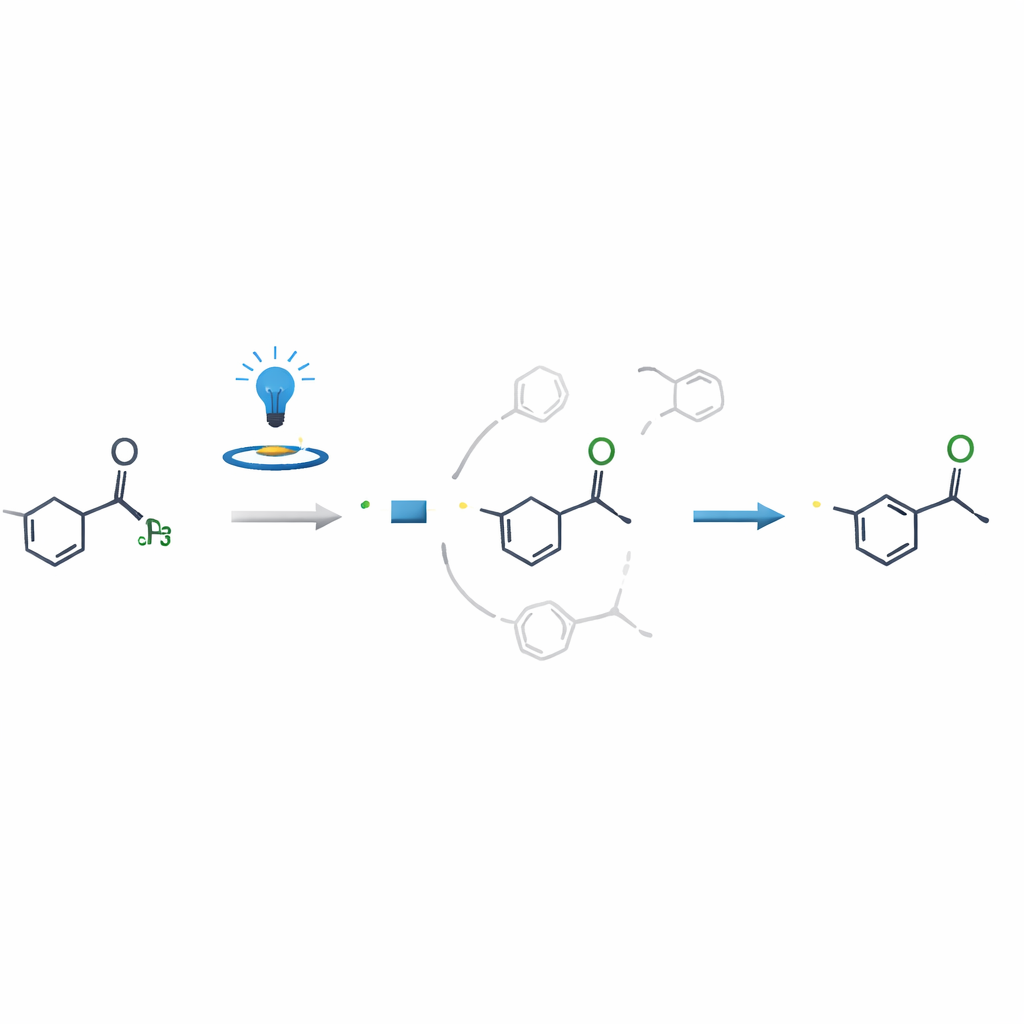
Dlaczego reakcja jest tak selektywna
Kluczowe pytanie naukowe brzmiało, dlaczego reakcja modyfikuje grupę N‑metylową tak czysto, skoro inne pobliskie pozycje wyglądają równie reaktywnie. Dzięki eksperymentom kontrolnym, pomiarom spinów elektronowych i szczegółowym obliczeniom komputerowym autorzy wykazali, że decydujący moment nie następuje w chwili powstawania rodnika, lecz gdy ten rodnik dodaje się do partnera winylowego lub alkynylowego. Ścieżka prowadząca od rodnika N‑metylowego do końcowego produktu jest zarówno energetycznie korzystniejsza, jak i znacznie szybsza niż konkurencyjne drogi, co skutecznie kieruje reakcję na jeden rezultat. To spostrzeżenie pomaga wyjaśnić wysoką selektywność i może naprowadzić na podobne strategie dla innych złożonych cząsteczek.
Co ta praca oznacza dla przyszłych leków
Podsumowując, badanie wprowadza praktyczny sposób chirurgicznego ulepszania istniejących leków zawierających trzeciorzędowe aminy, dodając zwarte chemiczne uchwyty, które mogą modulować ich interakcje z celami biologicznymi lub wiązać je z innymi składnikami. Pokazując, że takie późnostopniowe modyfikacje mogą przekształcić dobrze znany lek przeciwdepresyjny w jeszcze skuteczniejsze warianty w prostych modelach zwierzęcych i komórkowych, praca wskazuje na potężne połączenie nowoczesnej chemii syntetycznej, obliczeń i biologii. W miarę rozszerzania podejścia na inne leki może ono przyspieszyć udoskonalanie kandydatów na leki i pomóc odświeżyć starsze terapie poprzez poprawę ich skuteczności i bezpieczeństwa.
Cytowanie: Paul, S., Mahato, S., Mahapatra, S.K. et al. Late-stage N-Me selective alkenylation and alkynylation of drugs and unactivated tertiary amines using photoredox catalysis. Nat Commun 17, 2695 (2026). https://doi.org/10.1038/s41467-026-69131-7
Słowa kluczowe: kataliza fotoredoks, późnostopniowa funkcjonalizacja, trzeciorzędowe aminy, projektowanie leków przeciwdepresyjnych, transporter serotoniny