Clear Sky Science · pl
Zaplanowana terapia bakteryjna tłumi Enterohemorrhagic Escherichia coli poprzez konkurencję metaboliczną i wyciszanie czynników zjadliwości
Przyjazne bakterie jako żywe lekarstwo
Zatrucie pokarmowe wywołane przez niektóre szczepy Escherichia coli może powodować znacznie więcej niż tylko rozstrój żołądka. Niektóre tzw. enterohemoraginogenne E. coli (EHEC) wydzielają silne toksyny, które mogą wywołać niewydolność nerek, zwłaszcza u dzieci, a stosowanie standardowych antybiotyków może wręcz pogorszyć sytuację. W tym badaniu rozważono inny rodzaj terapii: użycie zaprojektowanego probiotyku i cukru występującego w mleku kobiecym, zamkniętych w inteligentnych mikrokapsułach, aby wyprzeć groźne bakterie i stłumić ich szkodliwe zachowania, nie zakłócając przy tym reszty ekosystemu jelitowego.
Dlaczego niektóre E. coli są tak groźne
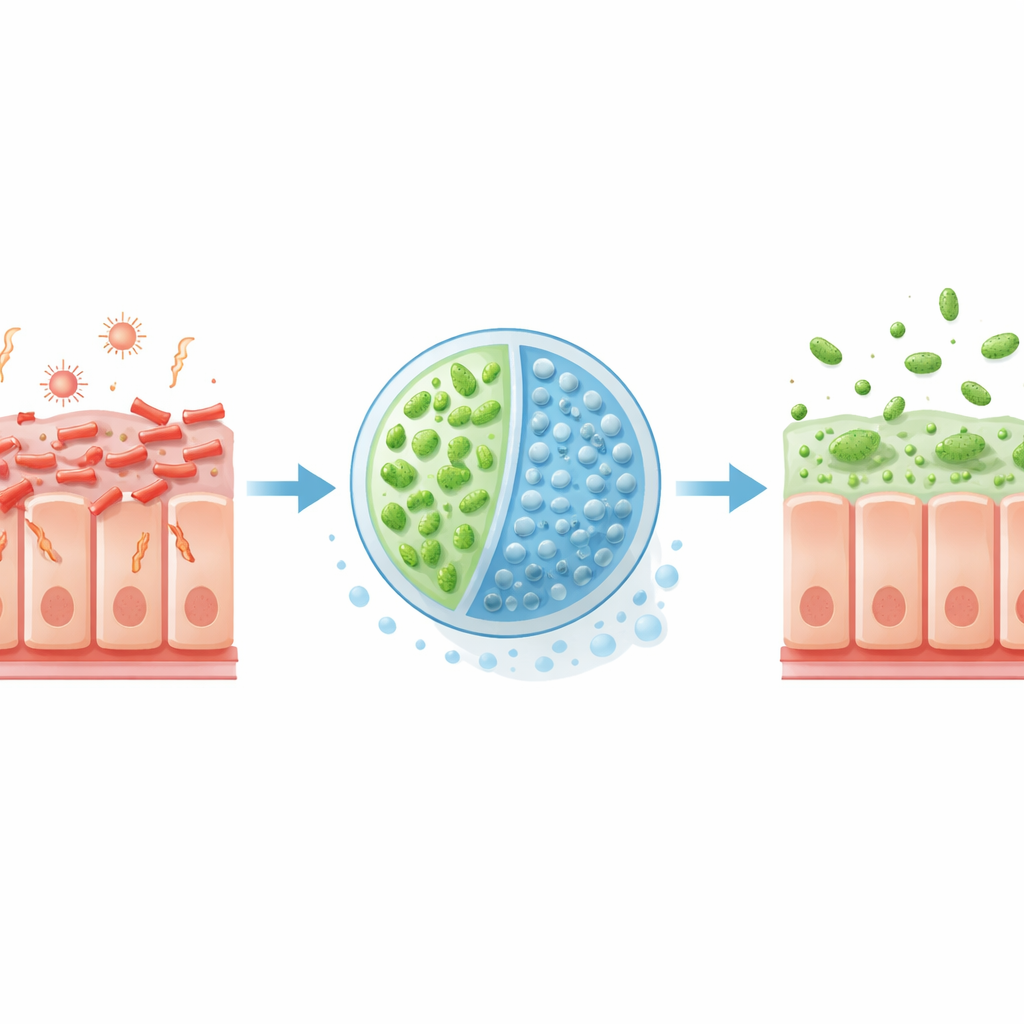
EHEC to zarazek przenoszony przez żywność, często pozyskiwany z niedogotowanego mięsa lub zanieczyszczonych warzyw. Po dostaniu się do jelita przylega mocno do komórek jelitowych i wstrzykuje białka, które przeobrażają powierzchnię komórki, tworząc zaczepy ułatwiające bakteriom przyleganie i rozprzestrzenianie się. Równocześnie EHEC produkuje toksyny Shiga, które mogą przedostać się do krwiobiegu i uszkodzić naczynia krwionośne, czasem prowadząc do zagrażającego życiu zespołu hemolityczno‑mocznicowego. Ponieważ wiele antybiotyków wywołuje u tych bakterii stres i indukuje większe uwalnianie toksyn, lekarze mają niewiele bezpiecznych opcji poza opieką wspomagającą, co sprawia, że nowe, celowane podejścia są bardzo pożądane.
Przeprogramowanie probiotyku, by zagłodzić i unieszkodliwić EHEC
Naukowcy zwrócili się ku Escherichia coli Nissle 1917, długo stosowanemu szczepowi probiotycznemu, i przeprojektowali go na mikroorganizmem terapeutycznym nazwanym EcN3. Wyposażyli EcN3 w dodatkowe geny pozwalające mu wydajniej rozkładać kwas glukuronowy — kwas cukrowy, który EHEC preferuje jako źródło pożywienia w jelicie grubym. Dodatkowo wprowadzili enzym rozdzielający cukier z mleka kobiecego 2′‑fukozylolaktozę na dwie części: laktozę i fukozę. Laktoza działa jak wewnętrzny „wyłącznik”, który uruchamia ulepszony system wykorzystania składników odżywczych w EcN3, pomagając mu pochłaniać kwas glukuronowy i pozbawiać EHEC tego paliwa. Fukosa natomiast pełni rolę sygnału, który nakłania EHEC do wyciszenia kluczowych genów zjadliwości, osłabiając jego zdolność do tworzenia silnych przylepień i wyrządzania szkód.
Inteligentne kapsuły uwalniające terapię we właściwym miejscu
Sam podanie zmodyfikowanych bakterii i cukru do jelita nie wystarcza: kwas żołądkowy może zabić probiotyk, a inne mikroby mogą zużyć cukier, zanim dotrze on do okrężnicy. Aby to rozwiązać, zespół skonstruował wielokomorowe mikrosfery — maleńkie kulki z żelu alginianowego z dwiema oddzielnymi komorami wewnętrznymi. Jedna komora przenosi EcN3, a druga 2′‑fukozylolaktozę, utrzymując je osobno aż do momentu dotarcia kulek do jelita grubego. Te mikrokapsuły opierają się rozkładowi w symulowanym płynie żołądkowym, ale rozpuszczają się w warunkach przypominających okrężnicę, uwalniając zarówno zmodyfikowane bakterie, jak i cukier dokładnie tam, gdzie są potrzebne. U myszy system z kapsułkami zwiększył przeżywalność EcN3 i silniej aktywował wprowadzone geny niż podanie tych samych składników bez kapsułek.
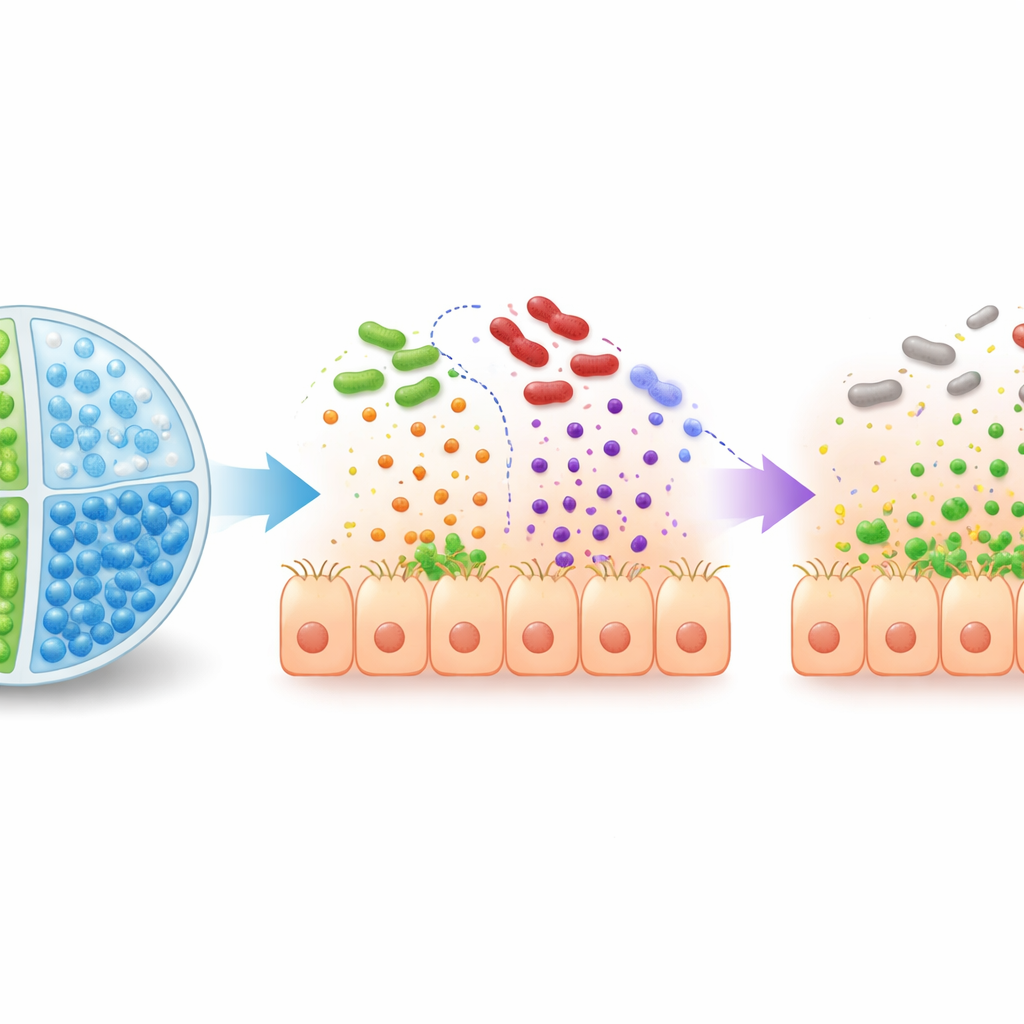
Testy ochrony w modelach zwierzęcych
Zespół przetestował swoją strategię na młodych królikach zakażonych EHEC oraz na myszach zakażonych Citrobacter rodentium, blisko spokrewnionym patogenie odzwierciedlającym wiele aspektów choroby u ludzi. Po leczeniu po zakażeniu kombinacją EcN3 i 2′‑fukozylolaktozy zwierzęta wykazywały mniejszą liczbę patogenów w jelicie, niższą ekspresję genów odpowiedzialnych za przyleganie bakterii oraz mniejsze uszkodzenia tkanki jelitowej — wszystko bez zwiększenia produkcji toksyny Shiga. Jako środek zapobiegawczy wolna (niezamknięta) kombinacja działała słabo, ponieważ cukier był szybko zużywany przez istniejący mikrobiom. W przeciwieństwie do tego, gdy EcN3 i 2′‑fukozylolaktoza były dostarczane razem w mikrosferach z dwiema komorami, zarówno króliki, jak i myszy wykazywały wyraźnie zmniejszone kolonizowanie przez patogeny, łagodniejszy przebieg choroby i lepsze przeżycie.
Pomaganie dobrym mikrobom i odbudowa bariery jelitowej
Analiza sekwencjonowania DNA profilu bakteryjnego jelit wykazała, że zakażenie zaburza normalną równowagę mikrobiologiczną, zwiększając udział szkodliwego Citrobacter przy osłabieniu korzystnych grup. Leczenie za pomocą zmodyfikowanych mikrokapsuł nie tylko zmniejszyło poziomy patogenów, ale też przywróciło społeczność ku zdrowszemu stanowi, w szczególności zwiększając liczebność gatunków Lactobacillus znanych ze wspierania zdrowia jelit. Wskaźniki funkcji bariery jelitowej pokazały podobny obraz: zwierzęta otrzymujące terapię w kapsułkach miały wyższe poziomy genów związanych ze śluzem i połączeniami ścisłymi, grubsze warstwy ochronnego śluzu oraz mniejsze przeciekanie znakowanego fluorescencyjnie śladu z jelita do krwiobiegu, co wskazuje na szczelniejsze, mniej zapalne ściany jelitowe.
Przedsmak przyszłej opieki nad infekcjami bez antybiotyków
Podsumowując, praca ta demonstruje dwutorową, celowaną strategię przeciwko notorycznie trudnej do leczenia infekcji przenoszonej przez żywność. Łącząc zmodyfikowany probiotyk, który konkuruje o pożywienie i wyczuwa nieszkodliwy sygnał cukrowy, z mikrokapsułami dostarczającymi oba składniki do okrężnicy, terapia osłabia EHEC, zmniejsza jego liczebność i chroni jelito bez polegania na tradycyjnych antybiotykach. Choć potrzebne są dalsze badania nad bezpieczeństwem i badania kliniczne, podejście ilustruje, jak żywe leki i inteligentne materiały mogą pewnego dnia zapewnić precyzyjne, przyjazne dla mikrobiomu sposoby radzenia sobie z ciężkimi zakażeniami jelitowymi i zmniejszać zależność od konwencjonalnych leków.
Cytowanie: Ma, G., Liu, R., Li, X. et al. Engineered bacterial therapy suppresses Enterohemorrhagic Escherichia coli through metabolic competition and virulence silencing. Nat Commun 17, 2307 (2026). https://doi.org/10.1038/s41467-026-69126-4
Słowa kluczowe: zmodyfikowane probiotyki, terapia infekcji jelitowych, EHEC, mikrobiom, mikrosfery do dostarczania leków