Clear Sky Science · pl
Dynamiczny domieszka chromu wspomaga aktywację wody na granicy faz na tlenku kobaltu typu spinel dla wydajnej ewolucji tlenu w środowisku kwaśnym
Dlaczego to badanie ma znaczenie dla czystej energii
Produkcja paliwa wodorowego z wody mogłaby zasilać przemysł i transport bez emisji dwutlenku węgla, lecz obecnie najwydajniejsze urządzenia opierają się na rzadkich i kosztownych metalach szlachetnych. To badanie pokazuje, jak starannie zaprojektowany, tani materiał oparty na kobalcie i chromie może zastąpić te metale w jednym z najtrudniejszych etapów rozdzielania wody: wytwarzaniu tlenu w warunkach kwaśnych, stosowanych w komercyjnych membranowych elektrolicach z wymianą protonów (PEMWE). 
Wyzwanie wytwarzania tlenu z wody
Nowoczesne PEMWE są atrakcyjne, ponieważ mogą szybko przekształcać energię elektryczną z paneli słonecznych czy turbin wiatrowych w wodór, nawet gdy dopływ mocy jest niestabilny. Jednak po stronie, gdzie powstaje tlen, reakcja jest powolna i agresywna. Zachodzi w środowisku kwaśnym i wymaga jednoczesnego przemieszczania protonów i elektronów w sposób silnie sprzężony. Obecnie etap ten zwykle katalizują tlenki irydu i ruten, metale rzadkie i drogie. Tlenek kobaltu (Co3O4) wyłania się jako obiecująca alternatywa, ale w kwasie ma skłonność do korozji: atomy kobaltu rozpuszczają się w cieczy, powierzchnia nadtlenia się do niestabilnych form i katalizator stopniowo się rozpada.
Sprytna modyfikacja: dodanie atomów chromu
Autorzy pokazują, że wprowadzenie niewielkiej ilości chromu do tlenku kobaltu typu spinel zmienia zarówno wewnętrzną strukturę elektronową ciała stałego, jak i cienką warstwę wody na jego powierzchni. Syntezują drobne, jednorodne nanocząstki domieszkowanego tlenku kobaltu z chromem (Cr‑Co3O4) i potwierdzają za pomocą dyfrakcji i mikroskopii elektronowej, że materiał zachowuje pierwotną strukturę spinelową. Zaawansowane techniki spektroskopowe wykazują, że atomy chromu wnikają na określone tetraedryczne pozycje w sieci i są rozproszone jako pojedyncze atomy, a nie tworzą oddzielnych cząstek tlenku chromu. Takie usytuowanie tworzy lokalne środowisko chrom‑tlen‑kobalt, które nieco obniża średni ładunek na atomach kobaltu, zmniejszając ich podatność na nadtlenianie.
Lepsze osiągi w trudnych warunkach kwaśnych
W testach w kwasie siarkowym katalizator domieszkowany chromem wymaga znacznie mniejszego dodatkowego napięcia niż niedomieszkowany tlenek kobaltu, aby osiągnąć ten sam prąd, co wskazuje, że przyspiesza produkcję tlenu. Przewyższa też komercyjne tlenki rutu i irydu przy wyższych gęstościach prądu i, co kluczowe, utrzymuje aktywność przynajmniej przez 160 godzin, podczas gdy inne katalizatory ulegają degradacji. Pomiary elektryczne pokazują, że ładunek przemieszcza się łatwiej przez granicę między domieszkowanym katalizatorem a cieczą. Gdy zastosowano go w pełnym urządzeniu do rozdziału wody z membraną PEM, Cr‑Co3O4 użyty po stronie tlenowej w parze ze standardowym katalizatorem platynowym po stronie wodorowej działa stabilnie ponad 750 godzin przy przemysłowo istotnym prądzie, wykazując praktyczną trwałość.
Jak chrom przekształca warstwę wody
Aby wyjść poza proste liczby wydajności, badacze zbadali, jak powierzchnia katalizatora i pobliskie cząsteczki wody zmieniają się podczas pracy. Pomiary in situ rentgenowskie i Ramana pokazują, że w czystym tlenku kobaltu atomy kobaltu ulegają silnemu nadtlenianiu przy wysokich napięciach, co jest zapowiedzią rozpadu struktury. W domieszkowanym materiale stan utlenienia kobaltu pozostaje niemal stały, podczas gdy chrom stopniowo się przesuwa, co wskazuje, że chrom działa jako „bufor” elektronów chroniący kobalt. Pomiary wrażliwe na powierzchnię ujawniają ponadto, że pod napięciami roboczymi atomy chromu coraz bardziej wiążą grupy hydroksylowe (OH). Te powierzchniowe hydroksyle zmieniają strukturę warstwy wody styku z elektrodą: spektroskopia w podczerwieni pokazuje osłabienie sieci wiązań wodorowych i wzrost udziału bardziej ruchliwych, „wolnych” cząsteczek wody. Ponieważ te molekuły wody łatwiej dysocjują, reakcja przekształcająca wodę w tlen przyspiesza. 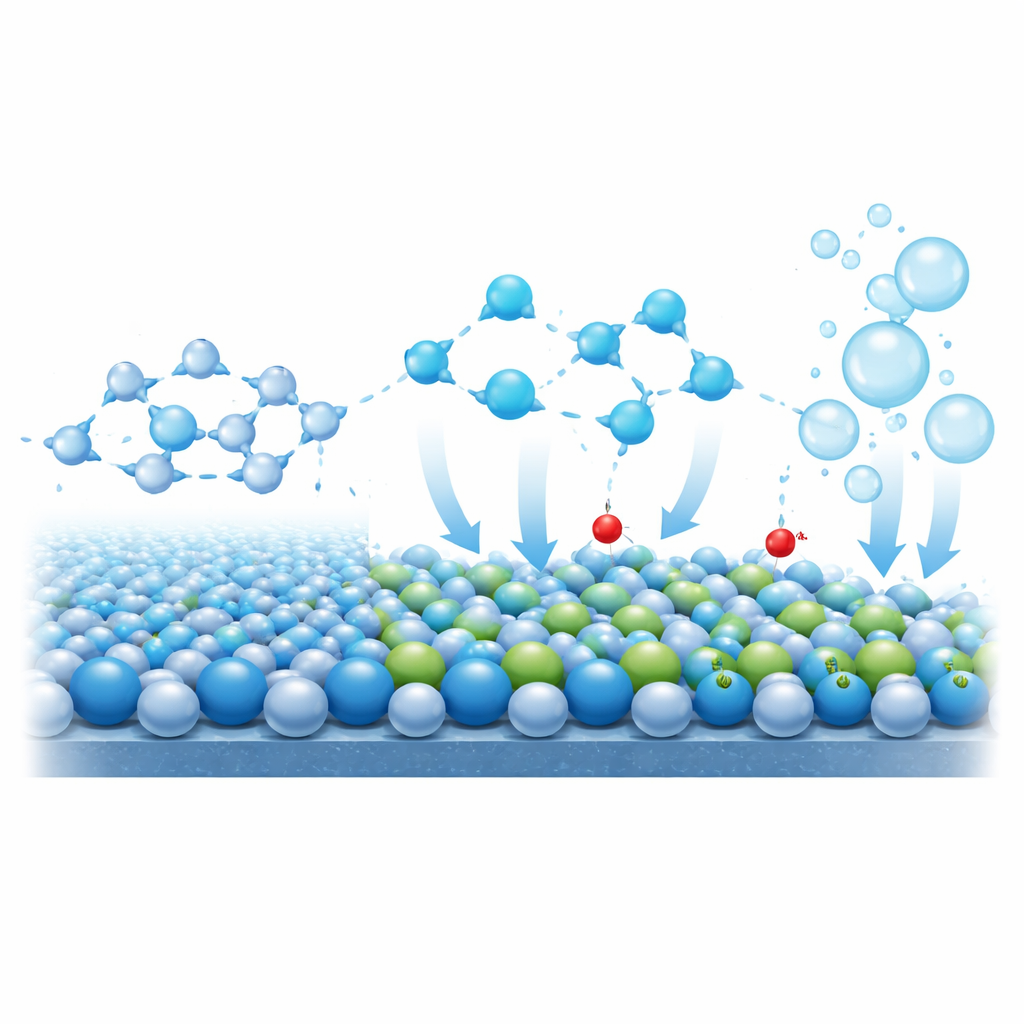
Powiązanie teorii z eksperymentem
Symulacje komputerowe potwierdzają ten obraz. Obliczenia pokazują, że chrom preferuje te same miejsca sieciowe zidentyfikowane eksperymentalnie i ma tendencję do przekazywania gęstości elektronowej ku sąsiednim atomom kobaltu. Energia potrzebna do rozbicia cząsteczki wody na domieszkowanej powierzchni jest mniejsza niż na czystym tlenku kobaltu, zwłaszcza gdy na miejscu chromu jest już obecny hydroksyl, co odzwierciedla eksperymentalne ustalenie, że powierzchnie bogate w hydroksyle są bardziej aktywne. Symulacje wskazują także, że wyrwanie atomu kobaltu z domieszkowanej powierzchni wymaga więcej energii, wyjaśniając poprawioną odporność na rozpuszczanie. Ogólne diagramy energetyczne reakcji potwierdzają, że najtrudniejszy krok w sekwencji tworzenia tlenu staje się łatwiejszy po wprowadzeniu chromu.
Co to oznacza dla przyszłych urządzeń do rozdziału wody
W sumie wyniki te pokazują, że niewielka ilość właściwego domieszki może dramatycznie zmienić zachowanie zarówno elektronów, jak i cząsteczek wody na powierzchni katalizatora. Poprzez użycie chromu do stabilizacji kobaltu i do kształtowania warstwy łatwo aktywowanej, słabo związanej wody, zespół stworzył trwały katalizator z nie‑metalu szlachetnego, który dorównuje tlenkom metali szlachetnych w wymagających warunkach kwaśnych. Dla czytelnika nie‑specjalisty kluczowy wniosek jest taki, że sprytne inżynierskie rozwiązania na skali atomowej — kilka atomów chromu we właściwych miejscach — mogą sprawić, że niedrogie materiały wykonają trudną pracę rozdzielania wody, przybliżając produkcję zielonego wodoru na dużą skalę do realności.
Cytowanie: Wu, L., Zhao, B., Huang, W. et al. Dynamic chromium dopant promotes interfacial water activation on cobalt spinel oxide for efficient oxygen evolution in acid. Nat Commun 17, 2598 (2026). https://doi.org/10.1038/s41467-026-69124-6
Słowa kluczowe: zielony wodór, elektroliza wody, reakcja ewolucji tlenu, katalizator tlenku kobaltu, woda przygraniczna