Clear Sky Science · pl
Izolowalny fosfaalumen(3) zdolny do aktywacji małych cząsteczek poprzez unikalne tryby reaktywności
Łamanie silnych wiązań za pomocą nowego narzędzia chemicznego
Chemicy nieustannie poszukują sposobów, by skłonić oporne cząsteczki do reakcji. Wiele powszechnych substancji, od wodoru gazowego po dwutlenek węgla, jest niezwykle stabilnych, co utrudnia ich przekształcanie w użyteczne produkty. W artykule opisano nowo zaprojektowaną cząsteczkę zbudowaną z glinu i fosforu, która potrafi przyłączyć takie oporne związki i rozdzielić ich wiązania. Zrozumienie i kontrola tego rodzaju aktywacji wiązań mogą w przyszłości pomóc przekształcać gazy odpadowe w surowce lub oferować łagodniejsze, oszczędzające metale drogi syntezy związków i materiałów.
Zaprojketowane wiązanie między glinem a fosforem
W centrum badania znajduje się rzadki typ połączenia między dwoma pierwiastkami grup głównych: glinem i fosforem. Badacze zsyntetyzowali cząsteczkę oznaczoną w pracy jako „3”, w której te dwa atomy dzielą zwarte wiązanie podwójne. Aby zapobiec jego rozkładowi, otoczyli je masywnym ramieniem organicznym, które chroni je przed niezamierzonymi reakcjami. Korzystając z dwóch różnych dróg syntezy, uzyskali kompleks w formie izolowalnej i wyhodowali pojedyncze kryształy odpowiednie do dyfrakcji rentgenowskiej, potwierdzając, że fosfor jest związany z glinem krótkim, przypominającym wiązanie podwójne, podczas gdy każdy atom jest wspierany przez otaczające ligandy zawierające azot. Obliczenia wykazały nierównomierne dzielenie elektronów między glinem a fosforem, co sprawia, że wiązanie jest spolaryzowane i podatne na atak innych cząsteczek.
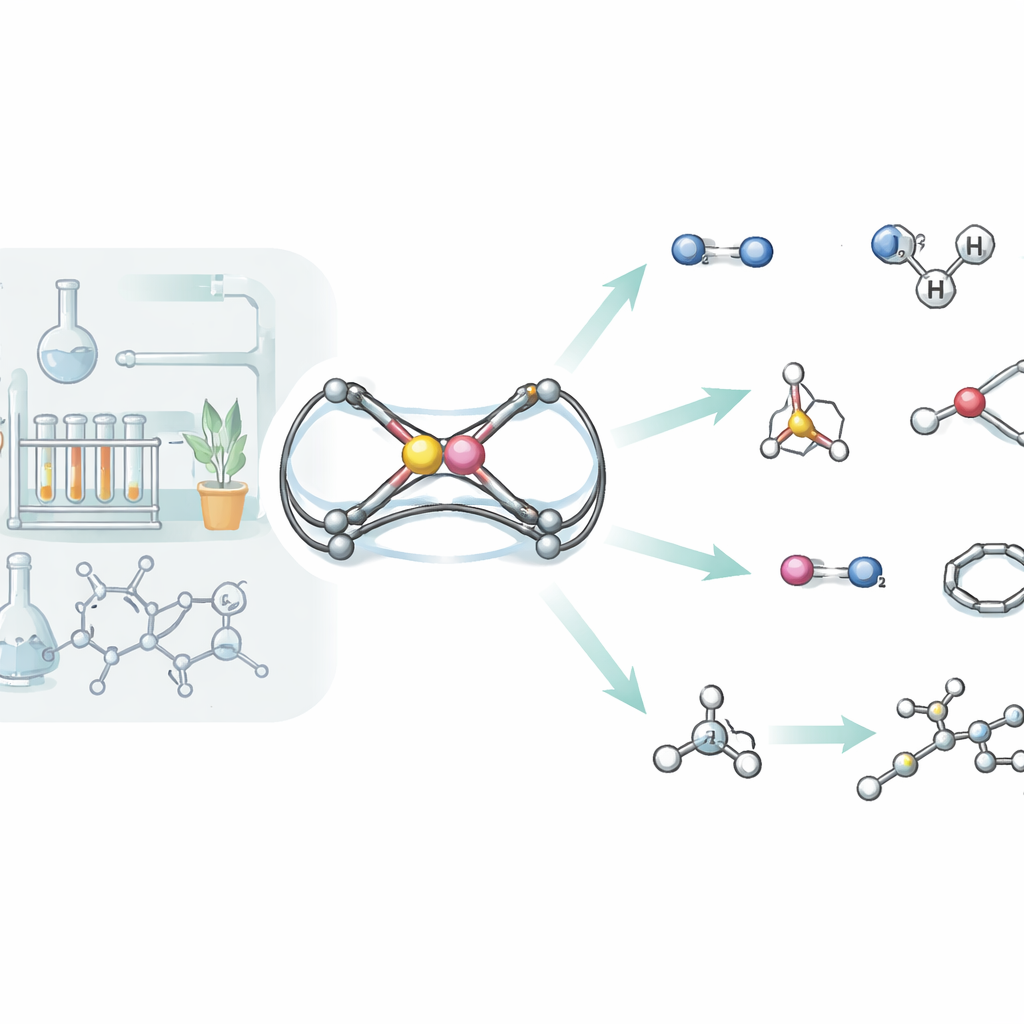
Jak nowa cząsteczka radzi sobie z wodorem gazowym
Wodór gazowy jest znany jako trudny do rozszczepienia bez zastosowania metali szlachetnych, a jednak nowa jednostka glin‑fosfor potrafi to zrobić. Po wystawieniu na działanie wodoru w łagodnych warunkach kompleks reaguje na dwa odmienne sposoby. W jednym z mechanizmów wiązanie H–H po prostu addycyjne przyłącza się do wiązania podwójnego glin–fosfor, przekształcając je w dwa wiązania pojedyncze i przyłączając po jednym atomie wodoru do każdego z atomów. W drugim mechanizmie cząsteczka wodoru jest rozdzielana kooperatywnie przez glin i sąsiedni atom azotu, zachowując się podobnie do tzw. „frustrowanych par Lewisa”, które aktywują wodór bez tradycyjnych katalizatorów metalicznych. Szczegółowe symulacje komputerowe odtworzyły obie ścieżki, wykazując podobne bariery energetyczne, co tłumaczy, dlaczego obydwa produkty powstają równolegle.
Rozbieranie całej gamy małych cząsteczek
Wodór to dopiero początek. Zespół systematycznie przetestował reakcje swojego szkieletu glin‑fosfor z szerokim zakresem małych cząsteczek, w tym białego fosforu, izocyjanidów, dwutlenku węgla, podtlenku azotu, azotku trimetylosylu, dimerów selenu, silanów, amin, styrenu i prostych alkinów. W wielu z tych reakcji pierwotne wiązanie Al=P ulega całkowitemu zerwaniu, a oba atomy kończą w większych strukturach typu klatkowego lub pierścieniowego, które włączają fragmenty nadchodzącej cząsteczki. Na przykład biały fosfor (P4) jest rozbijany i rekonstruowany w klatkę glin‑fosforową, podczas gdy dwutlenek węgla wstawia się dwukrotnie, tworząc sześcioczłonowy pierścień łączący glin i fosfor przez dwie nowe mostki węglowo‑tlenowe. W przypadku silanów i amin cząsteczka zachowuje się bardziej jak klasyczne wiązanie podwójne: wchodzące Si–H lub N–H przyłącza się czysto do Al=P, ponownie demonstrując „charakter π‑wiązania” tego nietypowego połączenia.
Dlaczego otaczające ramy mają znaczenie
Jedną z kluczowych lekcji pracy jest to, że masywny, bogaty w azot szkielet wokół jednostki Al=P nie jest jedynie podporą; kieruje on, jak i gdzie zachodzą reakcje. Porównując swoje wyniki z wcześniejszymi, krócej żyjącymi systemami glin‑fosfor, autorzy pokazują, że drobne zmiany w ligandach wspierających zmieniają równowagę między różnymi ścieżkami, takimi jak proste addycje do wiązania podwójnego a bardziej złożone rozrywanie wiązań i tworzenie pierścieni. Zaawansowane analizy rozkładu elektronów ujawniły silną polaryzację wiązania Al=P i podkreśliły, jak sąsiednie atomy azotu mogą współdziałać z glinem, zwłaszcza przy aktywacji wodoru. Objętość steryczna — fizyczne tłoczenie dużych grup — również skłania nadchodzące cząsteczki ku jednemu lub drugiemu miejscu reaktywnemu.
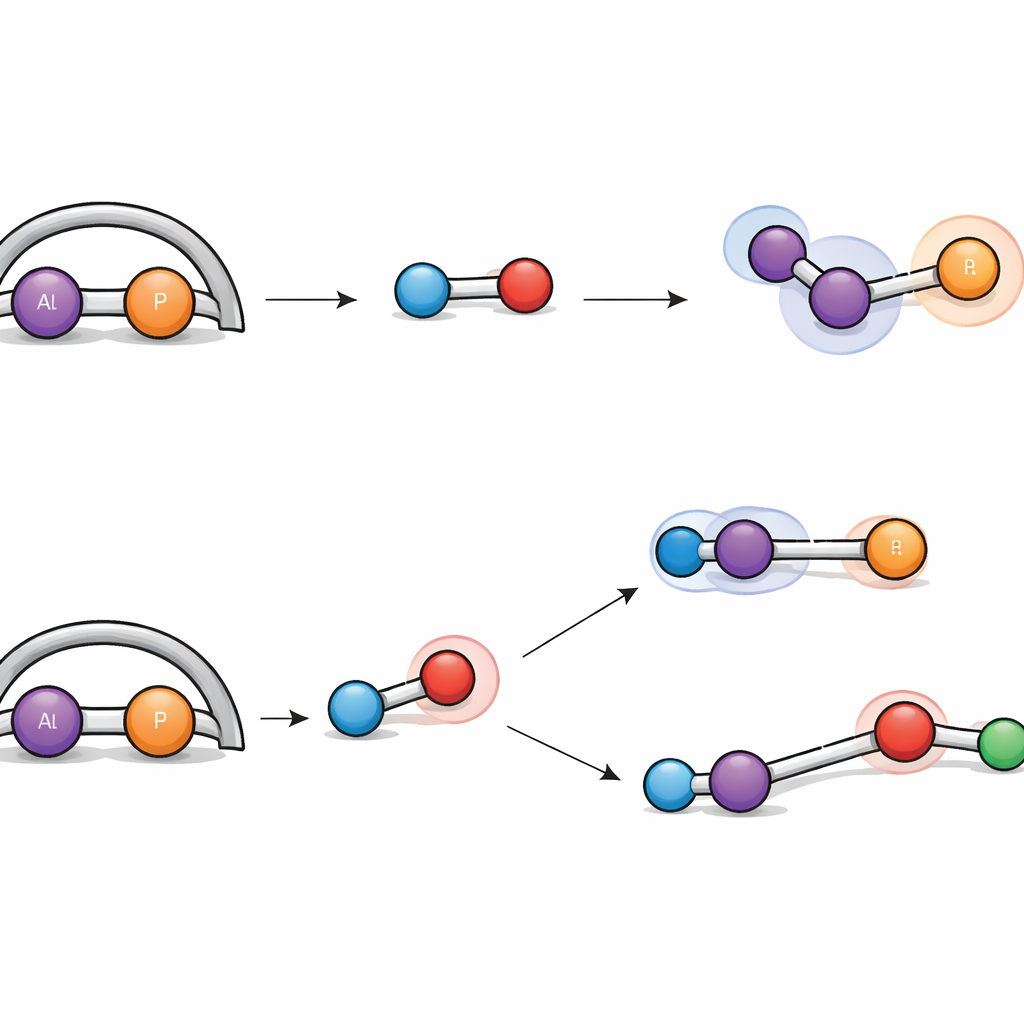
Co to znaczy dla przyszłej chemii
Dla laików alfabet reagentów w tym badaniu może wydawać się odległy, lecz przesłanie jest jasne: poprzez staranne dostrojenie zarówno wiązań, jak i kształtu wokół pierwiastków grup głównych, chemicy mogą tworzyć zwinne narzędzia, które dorównują lub uzupełniają tradycyjne katalizatory metaliczne. Ten izolowalny kompleks glin‑fosfor nie tylko przeżywa w butelce, lecz także radzi sobie z szerokim zestawem trudnych małych cząsteczek w łagodnych warunkach — rozszczepia wodór, przestawia biały fosfor i chwyta dwutlenek węgla. Praca pokazuje, że subtelne zmiany w „uchwycie” cząsteczki mogą głęboko przekierować jej reaktywność, oferując plan działania do projektowania przyszłych katalizatorów, które pomogą precyzyjnie i wydajnie przekształcać proste, stabilne cząsteczki w produkty o większej wartości.
Cytowanie: Cha, Y., Yang, Z., Zhuang, X. et al. An isolable phosphaalumene(3) capable of small molecule activation via unique modes of reactivity. Nat Commun 17, 2390 (2026). https://doi.org/10.1038/s41467-026-69118-4
Słowa kluczowe: aktywacja małych cząsteczek, chemia grup głównych, podwójne wiązanie glin‑fosfor, frustrowana para Lewisa, mechanizmy aktywacji wiązań