Clear Sky Science · pl
Mechanizm hamowania grzybowych syntez glukanu β−1,3 przez triterpenoidowe leki przeciwgrzybicze
Dlaczego zatrzymanie zakażeń grzybiczych ma znaczenie
Zakażenia grzybicze cicho zabijają ponad milion ludzi rocznie i zagrażają plonom oraz ekosystemom na całym świecie. Lekarze dysponują już ogranicowaną listą leków przeciwgrzybiczych, a niektóre groźne grzyby ewoluują, by się przed nimi uchylić. W tym badaniu ujawniono w szczegółach molekularnych, jak nowa klasa leków przeciwgrzybiczych przyczepia się do kluczowego enzymu, którego grzyby potrzebują do budowy ochronnej ściany komórkowej, i jak go unieruchamia. Zrozumienie tego procesu daje mapę drogową do projektowania lepszych terapii, które poradzą sobie z opornymi szczepami.
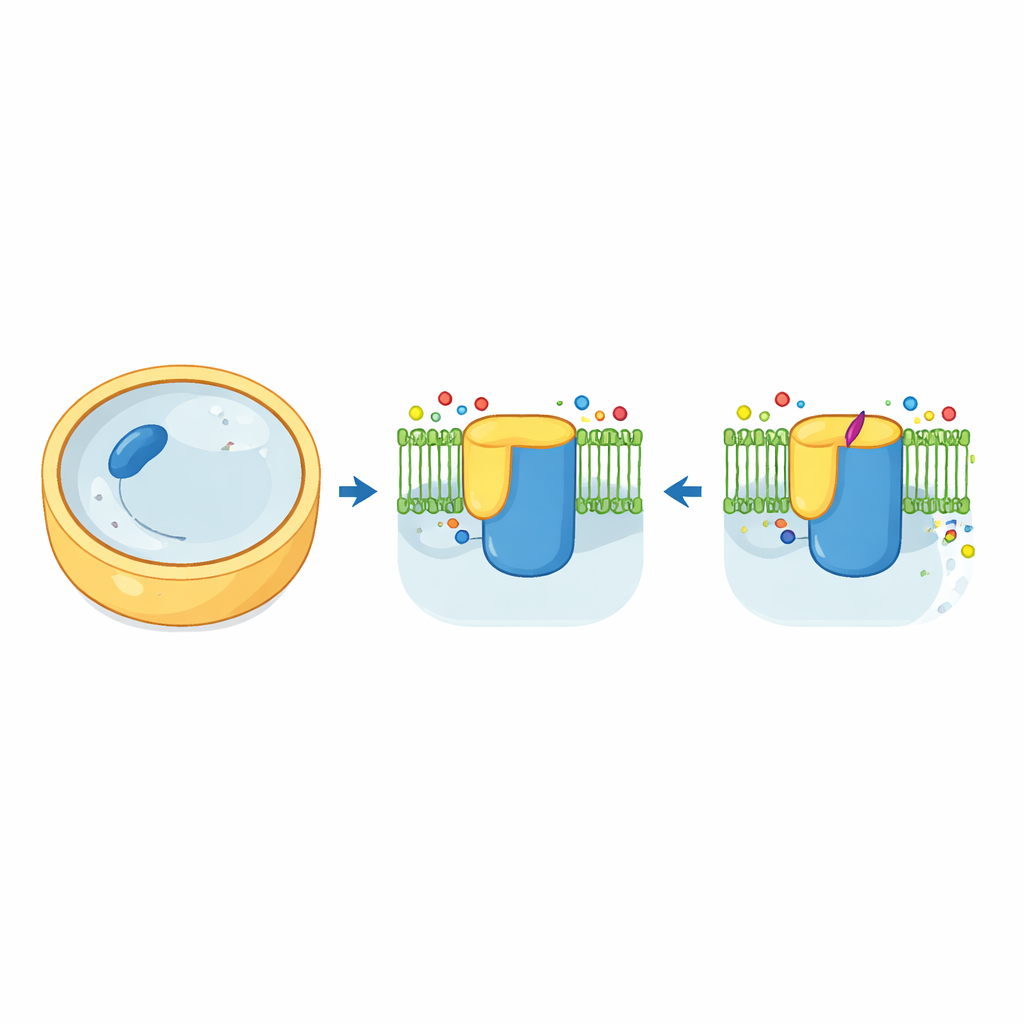
„Cegielnik” ściany komórkowej grzyba
Komórki grzybów otoczono wytrzymałą ścianą zbudowaną głównie z polisacharydu beta-1,3-glukanu. Enzym syntetyzujący i eksportujący ten polimer, znany jako syntezaza beta-1,3-glukanu, działa jak połączenie cegielnika i taśmy transportującej. W drożdżach piekarniczych maszyneria ta składa się z dwóch bardzo podobnych wariantów, Fks1 i Fks2, każdy osadzony w błonie komórkowej i kontrolowany przez mały białkowy pomocnik Rho1. Dzięki kriomikroskopii elektronowej autorzy uzyskali wysokorozdzielcze trójwymiarowe obrazy zarówno Fks1, jak i Fks2 w ich naturalnej postaci. Struktury ujawniają dużą cytosolową „ławę roboczą” połączoną z gęstwiną helis przechodzących przez błonę, z centralną wnęką, która prawdopodobnie służy jako tunel, przez który rosnący łańcuch glukanu opuszcza komórkę.
Jak naturalny lek chwyta enzym
Klinicznie istotne leki triterpenoidowe, w tym doustny ibrexafungerp, wywodzą się od naturalnego związku zwanego enfumafunginą. Do tej pory nie było jasne, gdzie dokładnie na syntezazie glukanu te leki się wiążą. Badacze rozwiązali struktury zarówno Fks1, jak i Fks2 związane z enfumafunginą. Ku zaskoczeniu, lek nie klinuje się w miejscu aktywnym, gdzie łączone są jednostki cukrowe. Zamiast tego osiada na zewnętrznej części pojedynczej helisy błonowej zwanej TM5, znajdując się w warstwie błonowej około trzech nanometrów od centrum katalitycznego i blisko prawdopodobnego kanału wyjścia glukanu. Kluczowe aminokwasy w tym fragmencie obejmują hydrofobowe jądro leku i kontaktują się z jego kwaśnym ogonem, podczas gdy przyłączona cukrowa część leku ledwie styka się z białkiem — co wyjaśnia, dlaczego chemicy mogli modyfikować tę część bez utraty aktywności.
Leki, które zamrażają ruchomą maszynę
Z pozoru ogólny kształt enzymu z i bez enfumafunginy wygląda niemal niezmieniony. Kluczowa różnica leży w organizacji otaczających lipidów i elastyczności niektórych helis. Po związaniu leku pobliska aromatyczna boczna grupa rotuje, zaciskając enfumafunginę na miejscu i razem z innym resztą stabilizuje uporządkowany lipid w sąsiedztwie leku. Dodatkowe lipidy przypominające sterole układają się porządnie wokół zestawu helis poziomych, które pomagają wyznaczyć ścieżkę eksportu glukanu. Te lipidy działają jak kliny i podpory, blokując helisy i wejście kanału w określone „podstawowe” ułożenie. Testy genetyczne pokazują, że zmiany wielu punktów styku dla leku lub tych steroli osłabiają wiązanie leku lub niszczą funkcję enzymu, a mutacje w tych miejscach odpowiadają znanym mutacjom oporności u patogenów ludzkich i roślinnych.
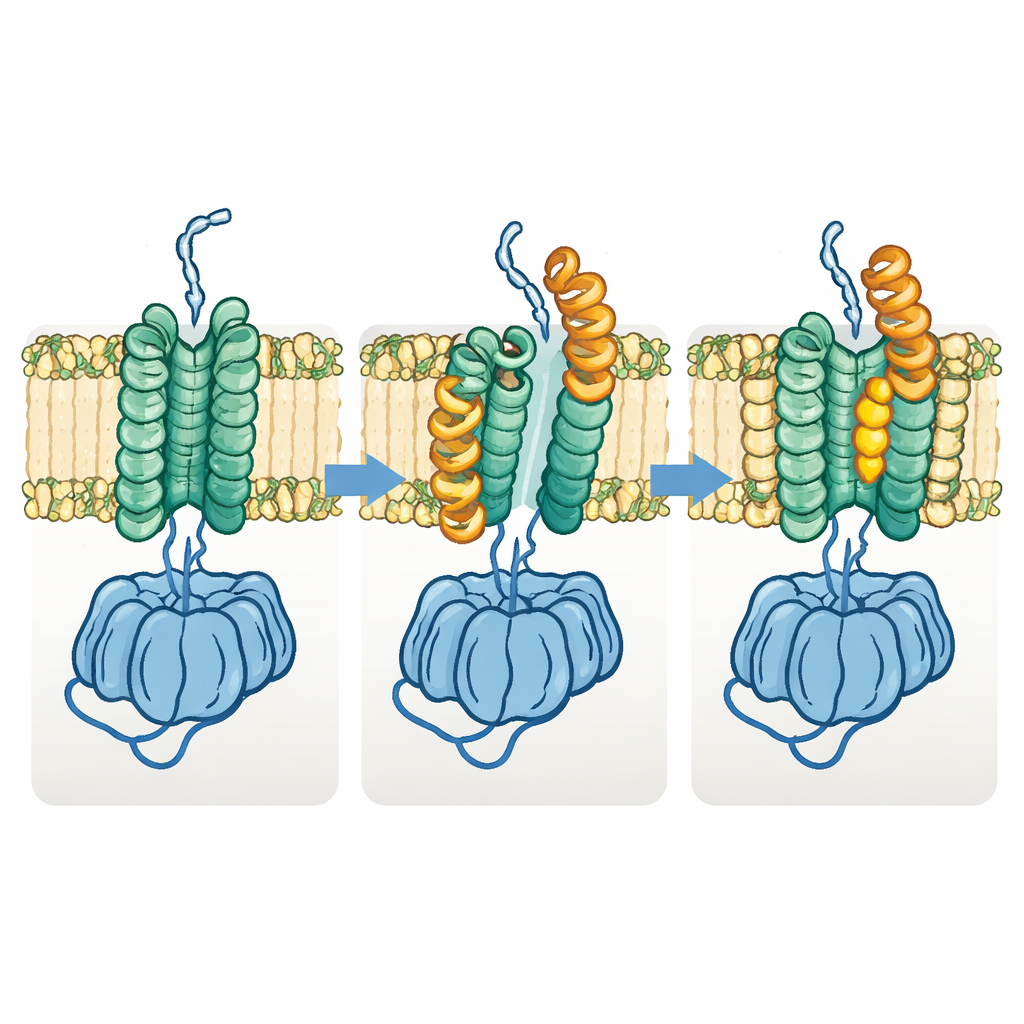
Nieodzowna zmiana kształtu dla transportu polimeru
Zespół odkrył także odrębną „otwartą” formę Fks1. W tym stanie jedna połowa regionu błonowego przesuwa się na bok, a kluczowe helisy poziome wychylają się na zewnątrz, rozchylając przestrzeń między dwoma wiązkami błonowymi i poszerzając widoczny tunel glukanowy. Porównanie wielu struktur sugeruje, że enzym cykluje między stanami podstawowym i otwartym podczas normalnej pracy: stan podstawowy przygotowuje i inicjuje tworzenie polimeru, natomiast stan otwarty pozwala rosnącemu łańcuchowi przemieszczać się bocznie przez błonę na zewnątrz. Gdy autorzy wprowadzili mostki disiarczkowe mające na celu trwale zablokowanie enzymu w jednym z tych stanów, obie zmodyfikowane wersje w dużej mierze utraciły aktywność, co wspiera tezę, że ta zmiana kształtu jest niezbędna do funkcji.
Co to oznacza dla przyszłych leków przeciwgrzybiczych
Pokazując, że enfumafungina i związane z nią leki nie działają przez blokowanie kieszeni katalitycznej, lecz przez przekształcanie lokalnego środowiska błonowego i zamrażanie syntezazy glukanu w stanie podstawowym, badanie ujawnia niekonwencjonalny sposób działania leków. Demonstruje też, że Fks1 i Fks2 mają niemal identyczne struktury i reakcje na lek, co wyjaśnia, dlaczego oba warianty trzeba brać pod uwagę przy zwalczaniu oporności. Szerzej rzecz biorąc, praca pokazuje, jak małe cząsteczki mogą kontrolować „nielakowalne” białka błonowe, wiążąc płytkie powierzchnie i rekrutując lipidy, dając koncepcyjny szkic do projektowania kolejnej generacji leków przeciwgrzybiczych, które pozostaną skuteczne nawet w miarę ewolucji grzybów.
Cytowanie: You, ZL., Sun, L., Wang, LX. et al. Inhibition mechanism of the fungal β−1,3-glucan synthases by triterpenoid antifungal drugs. Nat Commun 17, 2347 (2026). https://doi.org/10.1038/s41467-026-69114-8
Słowa kluczowe: leki przeciwgrzybicze, ściana komórkowa grzybów, syntezator glukanu, oporność na leki, kriomikroskopia elektronowa